Characterization of the sensitizing potential of chemicals by in vitro analysis of dendritic cell activation and skin penetration
Dr. Carsten Goebel, Wella AG, Abteilung Produktsicherheit und Toxikologie, Darmstadt
The development of in vitro models to identify sensitizing chemicals received
public interest since animal testing should be avoided whenever possible. We introduced
a new approach, analyzing two essential properties of sensitizing chemicals: skin
penetration and dendritic cell (DC) activation (J Invest Dermatol 122:1154 –1164,
2004). Immature DCs derived from human peripheral blood monocytes were pooled
from different donors to reduce interindividual variation. DC activation was evaluated
by flow cytometric analysis of CD86 highly positive cells and quantitative measurement
of interleukin-1ß (IL-1ß) and Aquaporin P3 gene expression. The sensitizer
2,4,6-trinitrobenzenesulfonic acid (TNBS) induced a dose dependent response for
all three parameters, whereas the irritant sodium lauryl sulfate (SDS) did not.
When two related aromatic amines, p-toluylenediamine (PTD) and hydroxyethyl-p-phenylenediamine
(HE-PPD), were tested, both induced a substantial DC activation indicating their
potential sensitizing properties. However, the in vitro findings contrasted with
the in vivo sensitizing potential: in murine local lymph node assays (LLNA) PTD,
but not HE-PTD,was identified as sensitizing using acetone/aqua/olive oil (AAOO)
as vehicle. Skin penetration measurement revealed that the bioavailability of
PTD from AAOO was significantly higher than that of HE-PPD. An enhanced skin penetration
of HE-PPD was found when dimethysulfoxide (DMSO) was used as vehicle. On retesting
HE-PPD in the LLNA using DMSO as vehicle, HE-PPD induced a specific response reflecting
its activating properties on DCs in vitro. We conclude that in vitro analysis
of DC activation capability allows prediction of the skin sensitizing potential
provided that skin penetration data demonstrate a sufficient bioavailability of
the test compound.
Background
Allergic contact dermatitis (ACD) is a delayed-type hypersensitivity reaction
induced by small reactive chemicals (haptens). In pharmaceutical and cosmetic
industry it is mandatory to identify chemicals that are potential ACD inducers
before they become part of a new product. Currently, the sensitizing potential
of chemicals is usually identified on the basis of animal studies, such as the
LLNA. There is, however, an increasing public concern regarding the use of animal
testing for the screening of new chemicals. The development of in vitro models
for predicting the sensitizing potential of new chemicals is therefore receiving
widespread interest. In vitro sensitization tests are furthermore needed to identify
the relevant aspects of the complex interactions of a chemical with the different
compartments of the immune system.
To date, no a reliable prediction
of the sensitizing potential based on DC activation in vitro was achieved because
the in vitro results did not reflect the actual ability to induce contact hypersensitivity
in vivo.
We assume that the lack of the skin barrier and the difficulties
in obtaining relevant DC activation data are responsible for this discrepancy.
Therefore, we propose to integrate in vitro skin penetration analysis using pig
skin, the most suitable model of human skin, and to use pooled immature DCs obtained
from different donors to reduce inter-individual variability which limit the interpretation
of DC activation data. The suitability of this approach was tested with two aromatic
amines, a class of chemicals comprising several known sensitizers. The in vitro
findings for the two compounds were compared with their potential to induce sensitization
in vivo as measured by the LLNA in mice.
Charakterisierung von Trägersystemen und Einfluss auf die kutane Resorption
Prof. Dr. Monika Schäfer-Korting, Institut für Pharmazie, Freie Universität Berlin
Der große Vorteil einer topischen Arzneimitteltherapie besteht in der Passage der gesamten resorbierten Arzneistoffmenge zum Wirkort, ehe der Wirkstoff sich – den Gesetzen der Pharmakokinetik folgend – im Körper verteilt. Zwar kann damit die Dosis niedrig gehalten werden, doch stehen die Barriereeigenschaften der Hornschicht einer guten Penetration in die Haut entgegen. Eine ausreichende Aufnahme des Wirkstoffs bei gleichzeitig geringen inter- und intraindividuellen Schwankungen ist somit ein wichtiges Ziel der Dermatotherapie.
Angesichts der extremen Lipophilität der Hornschicht sollte diese vor allem von Lipid-basierten Dermatika gut überwunden werden. Unter dieser Vorstellung wurden unterschiedliche Arten von Zubereitungen entwickelt und ex vivo bzw. am Tier oder im Humanversuch geprüft. Neben klassischen Topika sind dies heute vor allem nanostrukturierte partikuläre Carriersysteme. Liposomen-basierte Präparationen fördern insbesondere bei kleiner Partikelgröße und bei Zusatz von Tensiden die kutane Resorption. Aber auch mit rigiden Systemen, wie festen Lipidnanopartikeln (SLN) und Mischungen aus bei Raumtemperatur festen und flüssigen Lipiden (NLC), ist eine erhöhte kutane Aufnahme, bisweilen sogar eine bevorzugte Anreicherung in der lebenden Epidermis möglich. Voraussetzung für das Targeting ist eine Assoziation des Arzneistoffs mit dem Partikel. Um diese zu zeigen und um zwischen einer Adsorption des Wirkstoffs an die Partikeloberfläche und einem Einschluss in die Lipidmatrix zu unterscheiden, wurde die parelektrische Spektroskopie an die speziellen Bedürfnisse der Partikelcharakterisierung angepasst. Unsere Untersuchungen zeigen, dass eine unzureichende Adsorption an die Lipidoberfläche durch Ester-Produgs überwindbar ist.
Der
klinische Versuch muss nun zeigen, ob sich die in In-vitro-Experimenten aufgezeigten
Eigenschaften dieser Konstrukte auch in einer Verbesserung der topischen Therapie
von Dermatosen niederschlagen.
nach oben
Das immunkompetente Epidermismodell
Dr. Andreas Emmendörffer, Euroderm GmbH, Leipzig
unter Mitarbeit von H. Weigt, M. Müller, M. Weimar, S. Thude, Th. Graeve, K. Müller, A. Limat und Th. Hunziker
Die Haut stellt eine der wichtigen Barrieren des Organismus gegenüber der Umwelt dar. Sie setzt sich aus einer Vielzahl verschiedener Zelltypen zusammen, die eng abgestimmt regulatorische Funktionen ausüben und wesentliche Funktionen im Organismus ausüben. Eine bedeutende Rolle spielt in diesem Zusammenhang die Epidermis mit den in unterschiedlichen Differenzierungsstadien befindlichen Keratinozyten. Diese Zellen aktivieren über die Synthese löslicher Mediatoren (z. B. Interleukin-1, Chemokine und Lipidmediatoren) die Rekrutierung von Immunzellen in Antwort auf den Kontakt mit Mikroorganismen, Antigenen oder Xenobiotika. Epidermale Langerhanszellen und dermale dendritische Zellen bilden eine weitere wichtige zelluläre Komponente der Haut, indem sie nach Antigenkontakt über die Blut- oder Lymphgefäße in die drainierenden Lymphknoten wandern und dort die spezifische Immunantwort einleiten.
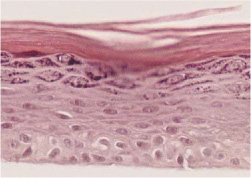
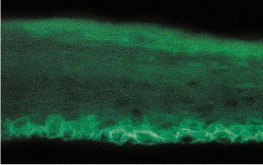
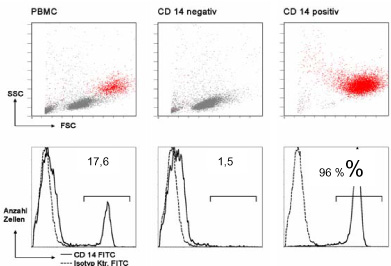
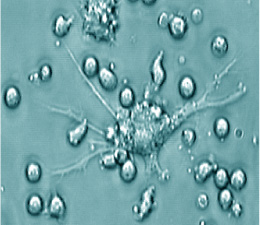
In dem Vortrag beim GD-Symposium wurden die Arbeiten zum Aufbau eines immunkompetenten Hautmodells vorgestellt. Ausgehend von ersten Studien zur Integration von Monozyten in ein Modell mit dermalen Fibroblasten und Keratinozyten und über ein Vollhautmodell mit dendritischen Zellen wurde über Arbeiten zur Entwicklung eines Epidermismodells berichtet, das mit dendritischen Zellen ausgestattet ist. Zu diesem Zweck wurden parallel Methoden entwickelt, die eine GMP-konforme Herstellung von Epidermis aus Zellen der äußeren Haarfollikelscheide (ORS) und dendritischen Zellen erlauben. Die jeweils eingesetzten Technologien wurden vorgestellt und anhand von immunhistochemischen und immunologischen Parametern (Durchflusszytometrie, Zytokinsekretion) illustriert (Abbildungen 1 bis 5).
Für die Aktivierung der jeweiligen zellulären Komponenten wurden Standardstimuli eingesetzt. Da die Arbeiten zu dem Modell noch nicht abgeschlossen sind, endete der Vortrag mit einem Ausblick auf die künftigen Arbeiten und offenen Fragen. So sind Studien mit Einsatz von bekannten irritierenden bzw. sensibilisierenden Substanzen in Vorbereitung.
Abb. 1: Humane Epidermis
Abb. 2 : Beta-1-Integrin-Expression
Abb. 3: Aufreinigung von Monozyten
Abb. 4: Dendritische Zellen
Abb. 5: Antigenexpression auf Monozyten und unreifen dendritischen Zellen
Das Psoriasis-SCID-Maus-Modell als Ansatz für die Medikamentenentwicklung
Prof.
Dr. med. Wolf-Henning Boehncke, Zentrum der Dermatologie und Venerologie, Klinikum
der Johann-Wolfgang-Goethe-Universität, Frankfurt am Main
Die Psoriasis ist durch einen komplexen Phänotyp, eine polygenetische
Determinierung und eine multifaktorielle Genese charakterisiert. Mehrere so genannte
Psoriasis-Tiermodelle konnten bislang lediglich einzelne Aspekte dieser Erkrankung
reproduzieren. Erst ein xenogener Transplantationsansatz, wobei Haut von Patienten
auf Mäuse mit einem schweren kombinierten Immundefekt (SCID) übertragen
wird, erfüllte die Anforderungen an ein Psoriasis-Modell. Dieses so genannte
Psoriasis-SCID-Maus-Modell hat sich in den letzten 10 Jahren nicht nur als aussagekräftiger
Ansatz für Pathogenese-Studien, sondern auch als Instrument zur Medikamentenentwicklung
erwiesen, dem ein hoher prädiktiver Wert zukommt.
| Substanz | Therapieprotokoll | Ergebnis SCID-Modell | Klinische Erfahrung |
| Dexamethason | 4 Wochen oral | Gute Effektivität | Selten eingesetzt |
| Clobetasol-17- propionat | 3 Wochen topisch | Moderat effektiv | Etabliert für milde bis mittelschwere Psoriasis |
| Ciclosporin | 2
Wochen intraperitoneal 4 Wochen intrakutan | Gute Effektivität | Etabliert für schwere Psoriasis |
| 1-alpha, 25-Dihydroxychole-calciferol (Calcitriol) | 4 Wochen intrakutan | Gute Effektivität | Topisch bei milder bis mittelschwerer Psoriasis |
| Efalizumab | 2 Wochen intraperitoneal | Gute Effektivität | Effektiv bei mittelschwerer bis schwerer Psoriasis |
| Troglitazon | 6 Wochen oral | Signifikante Reduktion der epidermalen Hyperplasie | 5 Patienten erfolgreich therapiert (wegen Lebertoxizität vom Markt genommen) |
| PS 519 (Blockade der CLA-Expression) | 4 Wochen intraperitoneal | Gute Effektivität | Analoge Substanzen in Phase III (nicht Psoriasis) |
| Efomycin M (CLA-Analogon) | 4 Wochen subkutan | Gute Effektivität | Bimosiamose effektiv in Phase I/II |
Der lokale Lymphknoten-Test: Modifikationen und ihre Validierung
Prof. Dr. Hans-Werner Vohr, Bayer Healthcare AG, Toxikologie, Wuppertal
Der lokale Lymphknotentest (LLNA), wie er in der OECD-Richtlinie 429 beschrieben ist, basiert auf einer Messung der Proliferation durch radioaktive Markierung der Zellen (3H-Thymidineinbau). Andere Endpunkte für die Aktivierung der Lymphknotenzellen werden durch die Richtlinie zugelassen, sofern sie wissenschaftlich vernünftig belegt und zitiert sind und die Methode beschrieben wurde. In dem Vortrag wurden die Ergebnisse einer sogenannten Catch-Up-Validierung alternativer Endpunkte vorgestellt. An dieser Validierung haben insgesamt 9 Labors (5 der Industrie, 3 von Auftragsinstituten und eines einer Behörde) aus Europa teilgenommen. Die Ringstudie wurden beaufsichtigt durch die Schweizer Behörde für Heilmittel (Swissmedic) in Bern. Die Gewichte und Zellzahlen der die Ohren drainierenden Lymphknoten wurden anstelle der radioaktiven Methode zur Bestimmung der Proliferation eingesetzt. Zusätzlich wurde die akute Hautreaktion durch Bestimmung des Ohrgewichts gemessen (8mm ? Stanze). Dieser Parameter ist ein Maß für die irritierenden Eigenschaften einer Substanz. Die statistische Auswertung der Studie wurde durch einen unabhängigen Statistiker der Berner Universität durchgeführt.
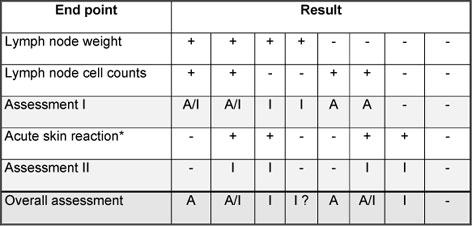
Ähnlich wie bei den EC3-Werten der radioaktiven Methode, wurden auch für die Parameter des modifizierten LLNA vergleichbare Grenzwerte berechnet. Für die Studie wurde ein Auswerteschema festgelegt, welches die Kombination ermittelter Effekte berücksichtigt, um das sensibilisierende Potenzial zu ermitteln (Tabelle 1). Dieses Schema erwies sich als sehr große Hilfe, um das Potenzial der Testsubstanzen vernünftig zu bewerten.
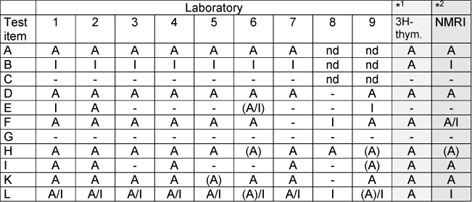
Insgesamt wurden HCA sowie 11 geblindete Substanzen NMRI- (nur erste Runde der Validierung) und BALB/c-Mäusen appliziert. Die Ergebnisse wurden über den Koordinator an den Statistiker geschickt. Die Ergebnisse bestätigten die Sensitivität und Zuverlässigkeit der untersuchten Parameter. Ebenso bestätigen sie den Wert der Einbeziehung des Ohrgewichts (oder der Ohrdick) als Maß für die akute Hautreaktion, wodurch eine Abgrenzung von reinen Irritanzien zu sensibilisierenden Substanzen möglich wird. Außerdem wurden unterschiedliche Parameter gefunden, die auch einen Einfluß auf die Stärke der Reaktion haben. All diese Parameter müssen für eine exakte Kategorisierung von Substanzen gemäß ihrem relativen Potential berücksichtigt werden. Durch das o.a. Bewertungsschema gelang es allen Labors, die Irritanzien, die kein sensibilisierendes Potential besitzen, aus den Testsubstanzen herauszufinden (Tabelle 2).
Table 1: Assessment of results
A = Allergen
I = Irritant
A/I = Allergen with pronounced irritating
potential or strong irritant
* = measured by ear swelling or ear weight
Table 2: Overall classification of test items A to L
(A):
cell count index just near the „positive level“ of 1.5 without being
significant or exceeding it, i.e. between 1.4 and 1.5
nd: not done; two labs
participated only in the second part of the validation
*1: one lab did the
radioactive method in addition
*2: one lab used NMRI outbred mice in addition.
In this case assessment of irritating properties were solely based on ear swelling
data instead of ear weights.
[Both
Tables are taken from G. Ehling et al., Toxicology, submitted 2004]
Die ECVAM Validierungsstudie von In-vitro-Tests zur Klassifizierung hautirritierenden Potenzials
Dr. Manfred Liebsch, Zentralstelle zur Erfassung und Bewertung von Ersatz- und Ergänzungsmethoden zum Tierversuch (ZEBET), Bundesinstitut für Risikobewertung (BfR), Berlin
Im
Jahr 2002 wurde die OECD-Prüfrichtlinie 404 zur Bestimmung hautirritierenden
und hautätzenden Gefährdungspotentials, der In-vivo-Test am depilierten
Kaninchen, durch eine stufenweise Test- und Bewertungsstrategie ergänzt,
die es erlaubt, vorliegende Erfahrungen am Menschen, validierte (Q)SAR Vorhersagen,
und validierte In-vitro-Tests für hautätzende und hautirritierende Eigenschaften
so einzusetzen, dass nur noch wenige In-vivo-Prüfungen am Kaninchen erforderlich
sind.
Sowohl die 7. Änderungsrichtlinie der EU-Kosmetikverordnung,
als auch die Prüfanforderungen in der Grundstufe nach der geplanten neuen
EU-Chemikalienpolitik (REACH) sieht eine tierversuchsfreie Bewertung des akuten,
lokalen Gefährdungspotentials an Haut und Auge vor. Die dafür neu entwickelten
Prüf- und Bewertungsstrategien können nur dann den erwarteten Arbeits-
und Verbraucherschutz bieten, wenn für beide Endpunkte („ätzend“
und „reizend“) wissenschaftlich validierte und anerkannte In-vitro-Testsysteme
existieren. Im Bereich der Vorhersage ätzender Eigenschaften (R34/R35) liegen
diese Tests seit 2004 als weltweit anerkannte OECD-Methoden vor. Seit dem Jahr
1998 laufen Bemühungen, auch die nach Gefahrstoffverordnung als „hautreizend“
(R38) zu kennzeichnenden Stoffe sicher von den nicht reizenden Stoffen zu unterscheiden.
Eine dazu mit fünf verschiedenen In-vitro- Tests (zwei Tests mit menschlichen
Hautmodellen sowie je ein Test mit menschlicher, exzedierter Haut, dem isolierten
Schweineohr und Mäusehaut) durchgeführte ECVAM-Prävalidierungsstudie
ergab leider im Jahr 2000, dass keines der Testsysteme weit genug entwickelt war,
um formal validiert werden zu können.
Nach erfolgreicher Testverbesserung
(2001-2003) werden nun drei In-vitro-Tests für akute Hautirritation in einer
vom EU-Validierungszentrum ECVAM geförderten Studie formal validiert. Zwei
kommerzielle humane Epidermis-Modelle, EPISKIN (EPISKIN SNC, Lyon, Frankreich)
und EpiDerm (MatTek, Ashland, USA), werden dabei erstmalig mit einem gemeinsamen
Testprotokoll geprüft, das aus einer Kooperation zwischen l’Oréal
und ZEBET hervorgegangen ist. Zusätzlich wird der „Skin Integrity Function
Test“ an exzedierter Mäusehaut evaluiert. Das Management der gesamten
Studie hat ZEBET im BfR übernommen. Jedes der Testsysteme wird in 3 Laboratorien
unter blinden Bedingungen geprüft. Die Stoffauswahl erfolgte durch unabhängige
Experten unter Federführung des Europäischen Chemikalienbüros in
Ispra (Italien). Das Primärziel der Studie ist eine akzeptable Unterscheidung
zwischen solchen Stoffen, die nach Gefahrstoffverordnung mit R38 oder nicht mit
R38 gekennzeichnet werden müssen. Ein sekundäres Ziel ist dann die mögliche
Unterscheidung von den drei Klassen nach dem zukünftigen, global harmonisierten
System (GHS), die eine Klasse „mild reizend“ vorsieht.
Eine
kürzlich durchgeführte Analyse der ersten Phase der Studie hat gezeigt,
dass beide Hautmodelle exzellente (und übereinstimmende) Vorhersagen innerhalb
der vorher definierten Akzeptanzkriterien geliefert haben. Da alle Fehlklassifikationen
nur im Übergangsbereich zwischen „nicht reizend“ und „reizend“
lagen, wird in der zweiten Phase ein weiterer Endpunkt neben der Hautviabilität
geprüft, die Freisetzung von IL-1?. Der SIFT an Mäusehaut schnitt überraschend
schlecht ab, so dass er nicht in die zweite Phase übernommen wird, sondern
statt dessen die Limitierungen des Tests im Entwicklerlabor genauer charakterisiert
erden. Das Konzept der Studie und die derzeit verblindet vorliegenden Ergebnise
der Phase 1 wurden beim GD-Symposium dargestellt.
Epidermale Barriere und Resorption
Dr. Ulrich F. Schäfer, Universität des Saarlandes, Fachrichtung Biopharmazie und Pharmazeutische Technologie, Saarbrücken
Allgemein wird für die dermale Resorption das Stratum corneum (SC) als Permeationsbarriere angenommen, dessen makroskopischen Struktur durch das so genannte „brik-and-mortar-Modell“ gut wiedergeben wird. Die Barriere kommt dabei vor allem durch das Wechselspiel zwischen den Korneocyten und den dazwischen liegenden Lipidbilayern zustande. Beim GD-Symposium wurden die Strukturen des SC vorgestellt und hinsichtlich ihrer Beteiligung an der Barrierefunktion gewichtet.
Prinzipiell stehen zur Überwindung des Stratum corneum der parazelluläre, der transzelluläre und der follikuläre/transglanduläre Penetrationsweg zur Verfügung. Hinsichtlich der Beeinflussung des parazellulären Weges konnten Jaeckle, Schäfer und Loth (J. Pharm. Sci. 92, 2003, 1396-1406) für Ketoprofen durch humane Epidermis zeigen, dass durch eine Vorbehandlung humaner Epidermis mit halbfesten Triglyceriden die Permeation erhöht wird während eine Vorbehandlung mit Vaseline bzw. Wollwachsalkoholsalbe die Permeation erniedrigt. Diese Effekte wurden der Invasion von Vehikelbestandteilen bzw. der Extraktion von Lipidbestandteile des SC zugeschrieben.
Des weiteren konnten Wagner et. al. (EJPB 58, 2004, 121-129) für Flufenaminsäure zeigen, dass für die verschiedensten Formulierungen ein direkter Zusammenhang zwischen der Konzentration im SC und den tieferen Hautschichten (lebende Epidermis und Dermis) besteht. Im Rahmen einer Diplomarbeit (Madlova, 2003, Charles University Prague) wurde der Einfluss des Wassergehaltes bei nichtionischer hydrophiler Creme (DAB) und wasserhaltiger hydrophiler Salbe (DAB) auf die Permeation von Flufenaminsäure durch humane Epidermis untersucht. Hierbei konnte gezeigt werden, dass ein reduzierter Wassergehalt bei der nichtionischen hydrophilen Creme zu einer Erhöhung des Fluxes führte, während bei der wasserhaltigen hydrophilen Salbe eine Reduktion zu beobachten war. Der Grund für dieses unterschiedliche Verhalten dürfte in unterschiedlichen Wechselwirkungen zwischen den Grundlagen und dem SC liegen.
Im Vergleich zum parazellulären Weg wird dem transzellulären Weg im allgemeinen eine geringere Rolle für die Gesamtpermeation zugewiesen. Heisig, Feuchter und Wittum (WiR Preprint 04/2004; Lehrstuhl Technische Simulation, Universität Heidelberg) konnten jedoch durch Modellrechnungen nachweisen, dass diese Wichtung sehr stark vom Verhältnis der Diffusionskoeffizienten in den Korneozyten und im Lipidbilayer abhängig ist. Durch Einsatz von Substanzen, die die Struktur der Korneocyten auflockern (zum Beispiel Harnstoff), gewinnt der transzelluläre Weg zunehmend an Bedeutung.
Dem follikulären/transglandulären Weg wird auf Grund des geringen Anteils an der Diffusionsfläche keine praktische Bedeutung zugemessen. Neuere Ergebnisse haben jedoch gezeigt, dass insbesondere für nanopartikuläre Systeme gerade dieser Weg von Bedeutung ist.
Zusammenfassend ist festzustellen, dass für eine dermale/transdermale Therapie das Überwinden der SC-Barriere nach wie vor eine wissenschaftliche Herausforderung darstellt, aber auch vielversprechende Ansätze bereits vorhanden sind, dieses wichtige Ziel zu erreichen.
Prüfung der dermalen Penetration von Pflanzenschutzmitteln an menschlicher und tierischer Haut
Armin O. Gamer, BASF AG, Experimentelle Toxikologie und Ökologie, Ludwigshafen
Hautkontakt ist wahrscheinlich der bedeutendste Expositionsweg des Menschen für Industriechemikalien und Pflanzenschutzmittel. Für letztere wird der Anteil der dermalen Dosis, der sich Anwender beim Umgang aussetzen, auf über 90 Prozent der Gesamtdosis geschätzt. Zur Extrapolation des Anwenderrisikos dienen Daten zur Toxizität und zur dermalen Penetration von Pflanzenschutzmitteln an Ratten. Vergleichende Untersuchungen zur in vitro dermalen Penetration an Haut von Ratten und Menschen tragen zur syInterspezies-Extrapolation bei der Risikobewertung bei.
Im Rahmen der Anwender-Risikobewertung wurden für eine Reihe von Pflanzenschutzwirk-stoffen vergleichende Prüfungen der Hautpenetration an Ratten und Humanhaut in vitro ge-mäß der Prüfrichtlinie der OECD sowie der Guidance Dokumente von OECD und EU durchgeführt (van Ravenzwaay & Leibold 2004a+b). Die Molekulargewichte der Substanzen lagen zwischen 231 und 466, ihre Wasserlöslichkeit zwischen 0,06 mg/l und 600 g/l und der Oktanol/Wasser Verteilungskoeffizient (logP) zwischen 0,7 und 4,5. Es wurden mit Epidermispräparaten von Ratten- oder menschlicher Vollhaut bestückte Diffusionszellen verwendet. Als Rezeptormedium wurde, je nach Löslichkeit der Wirkstoffe, Wasser oder 50% Ethanol eingesetzt. Die Experimente wurden mit finiter Dosierung (10 µl/cm²) von mit radioaktiv markierten Wirkstoffen versetzten Prüfsubstanzzubereitungen unter statischen Bedingung über eine Expositionszeit von maximal 24 Stunden durchgeführt. Es wurden die Wiederfindungsrate, der prozentuale Anteil der Radioaktivität in den verschiedenen Kompartimenten einer Diffusionszelle sowie die Absorptionsrate ermittelt.
Epidermale Membranen von menschlicher Haut waren grundsätzlich weniger permeabel als solche von Rattenhaut. Die Absorptionsraten durch Rattenepidermis waren zwischen 2,3- und 36,5-fach höher als die durch menschliche Epidermis. Die zeitliche Verzögerung (lag time) bis zur Penetration der Prüfsubstanzen ins Rezeptormedium war für Rattenepidermis meistens geringer als für Humanepidermis. Es zeigten sich keine klaren Abhängigkeiten der Hautpenetrationsraten vom Molekulargewicht, der Wasserlöslichkeit oder der Lipophilie der Substanzen. Andeutungsweise führte ein höheres Molekulargewicht bei Substanzen gleicher Lipophilie zu einer geringeren Penetration. Es ist davon auszugehen, dass andere Faktoren, zum Beispiel die Zusammensetzung der Prüfsubstanz-Formulierung, die Verdünnung der Formulierungen und Unterschiede der Rezeptormedien für die Penetration in vitro eine bedeutende Rolle spielen.
Die Daten zeigen jedoch klar, dass im Rahmen der Risikobewertung der geringeren dermalen Penetration durch Humanhaut Rechnung getragen werden sollte. Dies kann im Rahmen einer Korrektur gemäß folgender Formel geschehen:
Eine kürzlich veröffentlichte Ringstudie zeigt eine hohe Variabilität der In-vitro-Penetration durch Humanhaut zwischen verschiedenen Labors (van Sandt et al. 2004). Der Interspeziesvergleich kann deshalb nur anhand von Daten, die innerhalb eines Labors unter Verwendung identischer Prüfbedingungen erhalten wurden, erfolgen. Auch innerhalb eines Labors kann die Schwankungsbreite der Daten beachtlich sein. Dies hat die in der EU für die Zulassung von Kosmetikinhaltsstoffen zuständige Kommission dazu veranlasst, den Variationskoeffizienten als Qualitätskriterium einzusetzen (SCCNFP 2003). Derzeit wird die Frage untersucht, ob der Einsatz künstlicher humaner Hautmodelle die Variabilität vermindert.
Literatur
EU 2004, Guidance Document on Dermal Absorption, Sanco/222/2000 rev. 7
OECD Guideline 428 Skin Absorption in vitro Method, final Draft 2002
OECD Guidance Document 28 for the conduct of skin absorption studies, March 2004
SCCNFP Opinion concerning basic criteria for the in vitro assessment of dermal absorption of cosmetic ingredients, 2003
Van Ravenzwaay & Leibold, Toxicology in Vitro 18, 219-225, 2004
Van Ravenzwaay & Leibold, Hum. Exp. Toxicol. 23, 1-10, 2004
Van de Sandt et al., Regul. Toxicol. Pharmacol. 39, 271 – 281, 2004
Regulatorische Anforderungen an Validierungsstudien
Prof.
Dr. Horst Spielmann, Zentralstelle zur Erfassung und Bewertung von Ersatz- und
Ergänzungsmethoden zum Tierversuch (ZEBET), Bundesinstitut für Risikobewertung
(BfR), Berlin
Die Zentralstelle zur Erfassung und Bewertung von Ersatz-
und Ergänzungsmethoden zum Tierversuch (ZEBET) hat insbesondere die Aufgabe,
aktiv dazu beizutragen, dass die international standardisierten, behördlich
vorgeschriebenen sicherheitstoxikologischen Tierversuche vermindert werden. Alle
neuen Prüfmethoden müssen experimentell validiert werden, bevor sie
international, d.h. weltweit, als Prüfmethoden anerkannt werden können.
1990 wurde von ZEBET in Kooperation mit dem EU-Validierungszentrum ECVAM ein einfaches
Konzept für die experimentelle Validierung erarbeitet, das sich in der Praxis
nicht bewährte, weil wichtige Elemente fehlten. In Kooperation mit Kollegen
in Japan und den USA wurde 1996 von der OECD, die für die internationale
Harmonisierung sicherheitstoxikologischer Prüfmethoden zuständig ist,
ein Validierungskonzept verabschiedet, das als wesentliches Element jeder Methode
ein biostatistisch fundiertes Prädiktionsmodell (PM) enthält, mit dem
die Gefährlichkeit der Prüfsubstanz für Mensch oder Umwelt vorhergesagt
werden kann.
Das verbesserte ECVAM/OECD-Validierungskonzept hat sich
bei den anschliessenden internationalen Validierungsstudien bewährt, wie
z.B. bei den ECVAM-Studien zur Validierung von In-vitro-Phototoxizitätstests
und von drei In-vitro-Embryotoxizitätstests, die unter der Leitung von ZEBET
erfolgreich experimentell abgeschlossen werden konnten. Im Jahr 2000 hat die EU
den erfolgreich validierten 3T3 NRU In-vitro-Phototoxizitätstest offiziell
als ersten In-vitro-Toxizitätstest in die EU-Gefahrstoffverordnung zur Einstufung
und Kennzeichnung gefährlicher Stoffe aufgenommen. Inzwischen wurden nach
erfolgreicher experimenteller Validierung auch noch zwei In-vitro-Tests mit Humanhautmodellen
zur Prüfung auf Ätzwirkungen an der Haut und zur Prüfung auf Hautpenetration
von der EU und auch von den Behörden der USA akzeptiert. Schließlich
hat die OECD im Jahr 2004 erstmals vier experimentell validierte tierversuchsfreie
Prüfmethoden in den Katalog der offiziellen OECD-Prüfmethoden aufgenommen.
Im Vortrag wurden anhand der genannten erfolgreichen Beispiele die international
von EU und OECD verabschiedeten behördlichen Anforderungen an die experimentelle
Validierung neuer Prüfmethoden vorgestellt.
Transfer von dendritischen Zellen zum Lymphknoten
Prof. Dr. med. Heinfried H. Radeke, Pharmazentrum Frankfurt, Klinikum der Johann Wolfgang Goethe-Universität, Frankfurt am Main
Die
Haut stellt eine der wesentlichen Barrieren gegen Angriffe von Pathogenen dar
und vereinigt eine Reihe von Abwehrmechanismen des angeborenen Immunsystems, um
diese Aufgabe zu erfüllen. Als Epidermisspezifische Subpopulation der dendritischen
Zellen ist die Langerhanszelle (LZ) gekennzeichnet durch eine lokale Regeneration,
spezifische Marker und eine typische Immunfunktion. Anders als myeloide dendritische
Zellen (mDZ) in der Dermis sind die LC in der Epidermis positiv für Langerin,
S-100, Fascin, CD1a und regenerieren sich lokal (1). Durch eine entzündliche
Aktivierung werden die LC in der Keratinozytenschicht mobilisiert und verlassen
die Epidermis. Sie migrieren aktiv durch das dermale Kollagennetzwerk und treten
geführt durch ihre Chemokinrezeptoren, u.a. CCR7 und seine Liganden CCL19
und -21, in kleine drainierende Lymphbahnen über. Nur unter diesen inflammatorischen
Bedingungen erfolgt eine Auffüllung des epidermalen Kompartments mit LC Vorläuferzellen
aus dem Blut. Der Einwanderungs- und Differenzierungsprozess der LC ist abhängig
von CCR2, CCR4/10, CCR6 und TGFß.
Durch die Antigenaufnahme
und –prozessierung, dirigiert durch das Pathogen aber auch durch Faktoren
entzündlich-aktivierter, lokaler Zellen, durchläuft die LC ein Differenzierungsprogramm,
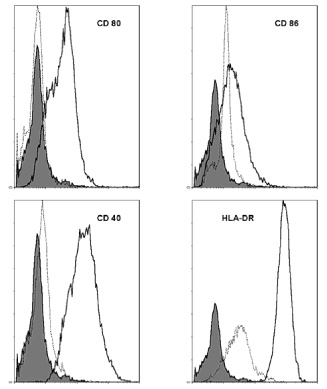
die Reifung. Reife LC werden positiv für CD80, -83, -86, MHC-Klasse II, DC-LAMP,
CCR7, und regulieren andererseits CCR6, Fc-gamma- und Antigenaufnahmerezeptoren
herunter, schalten also von der Antigenaufnahme zur –präsentation um.
Nicht nur aus pharmakologischer Sicht ist es interessant, dass z.B. Lipidmediatoren,
wie PGE2 oder PGD2, und auch Medikamente mit Wirkung auf ABC-Transporter einen
starken Einfluss auf die LC Differenzierung haben.
Das Ergebnis der Pathogen-induzierten
Reaktion kann eine allergische, Th2 Reaktion (Atopien), eine DTH-ähnliche
Th1 Reaktion (Psoriasis, Kontaktdermatitis)(2) oder eine anerge, bzw. aktive tolerogene
Reaktion sein (3,4). Als ein Beispiel für die richtungsgebenden Faktoren
aktivieren PAMPs („pathogen associated molecular pattern“) die „pattern
recognition“ Rezeptoren, z.B. die TLRs (Toll-ähnliche Rezeptoren) 4
oder 9, und führen zu stark proinflammatorischen Profilen mit erhöhter
IL12p70 oder IL-23 Freisetzung (5), während TLR2 PAMPs, z.B. Bestandteile
grampositiver Bakterien zu einer Th2 Reaktion führen können. Im Einklang
hiermit zeigen eigene Untersuchungen, dass bei einer durch GM-CSF /LPS /IFN-gamma
induzierten Reifung PGE2 die Freisetzung von IL-12p40 erhöht, während
PGD2 die Expression von IL12p40 vermindert. Aktuelle Experimente in unserem Labor
konzentrieren sich auf den relativen Beitrag von Prostaglandinen und verschiedenen
TLR-Liganden auf die Expression der Proteinuntereinheiten der IL-12 Zytokinfamilie
(IL-12p35, p40, IL-23p19, IL-27 (EBI3 und p28)). Darüber hinaus, zusammen
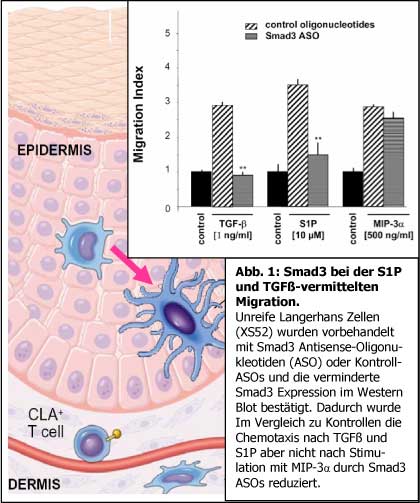
mit B. Kleuser (Inst. Pharmazie, FU Berlin), konnten wir zeigen, dass das Lysophospholipid,
Sphingosin-1-Phosphat (S1P), für seine migratorische Wirkung auf unreife
LC überraschend einen überlappenden S1P-Rezeptor-abhängigen, TGFß-Rezeptortransaktivierenden
und Smad-abhängigen Signalweg benutzt (6). Dies könnte bedeuten, dass
S1P freigesetzt aus Mastzellen und Thrombozyten und in hoher Konzentration im
Blut mit HDL transportiert zu einer Th2/tolerogenen Differenzierung von LC beiträgt.
Zurück zu den wandernden, antigenbeladenen LC: Diese gereiften und hochaktiven
Zellen erreichen 6-8 Stunden nach dem Eindringen des Pathogens den regionalen
Lymphknoten (LN). Obwohl das lösliche Antigen schon nach 30 min über
drainierende Lymphbahnen den LN erreicht, wird ein effektives ‚priming’
von naïven T-Lymphozyten mit differenzierender Wirkung nur durch die aus
dem Gewebe kommenden, stark aktivierten LC induziert. Naïve T-Zellen, die
auf solche antigenbeladenen LC treffen, halten deutlich länger Kontakt als
residente LN-DC, wobei in spätestens 48 Std. das vollständige antigenspezifische
Repertoire der TCR durchlaufen ist (7). Am Ende führt auch der anfangs beschriebene,
gewebespezifische Reifungsprozess der LC dazu, dass die aktivierte und differenzierte
T-Zelle ausgestattet mit CLA, CCR4, CCR6, etc. präferenziell zur Haut zurückwandern
wird (8). Auf diesem Hintergrund, der kontinuierlich voranschreitenden Aufklärung
der Details dieses Prozesses, wurden und werden weiter neue pharmakologische „targets”
identifiziert. Die rasch voranschreitende Entwicklung von Modulatoren dieser immunologischen
Abläufe wirkt sich nicht nur im Bereich der Dermatologie, sondern auch bei
der Entwicklung neuer Impfprotokolle, sowie in der Antikörper- und zellbasierten
Antitumortherapie aus.
(* unterstützt durch die DFG Ra 525/7-3 und die Dr.-Hans-Schleussner-Stiftung)
Literatur
1. Merad M, Manz MG,
Karsunky H et al.: Langerhans cells renew in the skin throughout life under steady-state
conditions. Nat Immunol 3:1135-1141, 2002
2. Lew W, Bowcock AM, Krueger JG:
Psoriasis vulgaris: cutaneous lymphoid tissue supports T-cell activation and „Type
1“ inflammatory gene expression. Trends Immunol 25:295-305, 2004
3. Geissmann
F, Dieu-Nosjean MC, Dezutter C et al.: Accumulation of immature Langerhans cells
in human lymph nodes draining chronically inflamed skin. J Exp Med 196:417-430,
2002
4. Kapsenberg ML: Dendritic-cell control of pathogen-driven T-cell polarization.
Nat Rev Immunol 3:984-993, 2003
5. Kopp T, Lenz P, Bello-Fernandez C et al.:
IL-23 production by cosecretion of endogenous p19 and transgenic p40 in keratin
14/p40 transgenic mice: evidence for enhanced cutaneous immunity. J Immunol 170:5438-5444,
2003
6. Radeke HH, von Wenckstern H., Stoidtner K et al.: Overlapping signaling
pathways of sphingosine 1-phosphate and TGF-ß in the murine Langerhans cell
line XS52. J Immunol-in revision, 2004
7. Mempel TR, Henrickson SE, von Andrian
UH: T-cell priming by dendritic cells in lymph nodes occurs in three distinct
phases. Nature 427:154-159, 2004
8. Dudda JC, Simon JC, Martin S: Dendritic
cell immunization route determines CD8+ T cell trafficking to inflamed skin: role
for tissue microenvironment and dendritic cells in establishment of T cell-homing
subsets. J Immunol 172:857-863, 2004
Untersuchung der Hautirritation am Menschen
Prof.
Dr. Klaus-P. Wilhelm,
proDERM Institut für Angewandte Dermatologische
Forschung GmbH, Schenefeld
Die lokale Verträglichkeit gehört zu den wichtigsten Eigenschaften topischer Präparate. Dies gilt sowohl für Kosmetika als auch für Dermatotherapeutika. In Abhängigkeit von der Produktkategorie und der vorgesehenen Anwendung werden verschiedene Methoden zur Untersuchung der lokalen Verträglichkeit eingesetzt (Tabelle). Am häufigsten werden die akute und die kumlative Irritation, die Sensibilisierung sowie die Phototoxizität und Photosensibilisierung untersucht. Darüber hinaus können die Augenverträglichkeit und die sensorische Irritation geprüft werden .
Im Vortrag beim GD-Symposium in Berlin wurden die verschiedenen Prüfverfahren mit ihren Möglichkeiten und Grenzen dargelegt. Außerdem wurde eine Strategie vorgestellt, wie die Prüfung der lokalen Verträglichkeit in den Entwicklungszyklus topischer Präparate einbezogen werden kann.
Untersuchung der regenerativen Wirkung von Emulsionen am 3D-Hautmodell
Dr. Jens-Olaf Eichler, Degussa Stockhausen GmbH, Laboratorium für Toxikologie und Ökologie, Krefeld
Häufiger
und langandauernder Hautkontakt zu mäßig hautreizenden Substanzen am
Arbeitsplatz kann zu beruflich bedingten Hauterkrankungen führen. Diese sind
die am häufigsten angezeigten Berufskrankheiten.
Mit den bekannten In-vivo-Nachweismethoden
wie dem repetitiven okklusiven Irritationstest (ROIT) am Menschen ist es möglich,
eine hautschützende Wirkung von Emulsionen nachzuweisen. Allerdings kann
mittels dieser Methode allein nicht nachgewiesen werden, wie dieser Effekt zustande
kommt.
3D-Hautmodelle sind vitale dreidimensionale In-vitro-Modelle
der menschlichen Haut, die eine rekonstituierte Spenderepidermis mit funktionalem
Stratum corneum besitzen. 3D-Hautmodelle können wichtige Komponenten der
Haut selbst synthetisieren und somit auf äußere Einflüsse reagieren.
Ziel der Studie war es, die regenerative Wirkung von Emulsionen mit
Hilfe eines 3D-Hautmodells nach einer leichten Schädigung zu untersuchen.
Als Modellirritans wurde Natriumlaurylsulfat (SDS) verwendet.
Die Reaktion
des 3D-Hautmodells wurde über verschiedene biochemische Parameter, zum Beispiel
Lactat-Dehydrogenase-Freisetzung (LDH), Interleukin 1a (IL-1 alpha), Prostaglandin
E2 (PGE2) und Zusammensetzung der Hautlipide, nachgewiesen.
Die beispielhaft
untersuchten Emulsionen verstärken die Hautbarriere und vermindern Zelllyse
sowie die Ausschüttung des Entzündungsmediators PGE2 bzw. IL-1-alpha
nach Hautschädigung durch SDS. In beiden Fällen wird die Hautbarrierereparatur
nach einer Hautschädigung durch SDS über drei unterschiedliche Mechanismen
unterstützt.
Es ist nahe liegend, dass diese biochemischen Prozesse
für die in den Probandentests nachgewiesene hautschützende Wirkung der
Emulsionen verantwortlich sind.
Im Gegensatz zu anderen In-vitro-Methoden
können im 3D-Hautmodell biochemische Reparaturprozesse menschlicher Haut
über einen längeren Zeitraum untersucht werden, daher ist das 3D-Hautmodell
eine neue Methode zum Wirksamkeitsnachweis von Hautpflege- und Hautschutzprodukten.
Im Vergleich zu In-vivo-Tests bietet diese Methode den Vorteil, dass
auch zugrunde liegende Mechanismen für kosmetische Produkte untersucht werden
können.
nach oben