Teil
1 Wissenschaftliches Hauptprogramm
Teil
2: Workshop der GD-Fachgruppe Dermokosmetik: Reinigung und Pflege der zur Akne
neigenden Haut
Teil
3: Symposium der GD-Fachgruppe Dermatotherapie: Innovative Dermatika — Vom
Molekül zur Zulassung
Teil
4: Workshop: Topische Immunmodulatoren (TIMs). Etablierte und zukünftige
Indikatoren
Veranstalter: Fujisawa Deutschland GmbH, München
1, 25-Hydroxy-Vitamin D3 schützt menschliche Keratinozyten durch die Bildung von Sphingosin-1-phosphat vor Apoptose
Freie Universität Berlin, Institut für Pharmazie
1,25-Dihydroxyvitamin D3 (1,25-(OH)2D3) inhibiert das Zellwachstum von Keratinozyten und fördert deren Differenzierung, daher werden 1,25-(OH)2D3 und seine Analoga für die Behandlung der Psoriasis erfolgreich eingesetzt. Dabei wird diskutiert, dass 1,25-(OH)2D3 die Bildung von Ceramiden induziert und hierüber der differenzierungsfördernde Effekt vermittelt wird. Allerdings sind Ceramide auch wirkungsvolle Induktoren der Apoptose, so dass die Behandlung mit 1,25-(OH)2D3 auch mit einer Erhöhung der Apoptoserate von Keratinozyten verknüpft sein sollte. Interessanterweise führt 1,25-(OH)2D3 in physiologischen Konzentrationen, trotz der Bildung von Ceramiden, nicht zum programmierten Zelltod. Vielmehr besitzt 1,25-(OH)2D3 einen gegenteiligen Effekt, das heißt, Keratinozyten werden vor der Apoptose geschützt. So ist die Anzahl apoptotischer Keratinozyten drastisch verringert, wenn man typische Apoptoseinduktoren wie Tumor Nekrose Faktor ? (TNF-?) oder UV einsetzt und die Zellen vorher mit 1,25-(OH)2D3 behandelt hat. Eine mögliche Erklärung für diesen unerwarteten Effekt stellt die weitere Metabolisierung von Ceramiden zu Sphingosin-1-phosphat (SPP) dar. Tatsächlich führt 1,25-(OH)2D3 zu einer verstärkten Bildung dieses Sphingolpipids. Im Gegensatz zu Ceramiden vermittelt SPP auch eine antiapoptotische Wirkung. Eine direkte Beteiligung von SPP an der zytoprotektiven Wirkung von 1,25-(OH)2D3 kann nachgewiesen werden, wenn man den Sphingosin Kinase Inhibitor N,N-Dimethylsphingosin (DMS) einsetzt. Dieser hemmt das entscheidende Enzym für die SPP-Synthese, so dass nach Gabe von 1,25-(OH)2D3 kein SPP gebildet werden kann. In der Tat verliert 1,25-(OH)2D3 in Gegenwart des Inhibitors vollständig seine antiapoptotischen Eigenschaften. Darüber hinaus besitzt SPP aber noch weitere wichtige Eigenschaften in dermalen und epidermalen Zellen. So fördert es migratorische Eigenschaften von Keratinozyten und induziert die Bildung von extrazellulären Matrixproteinen durch Fibroblasten. Ein entscheidender Punkt ist wie bei 1,25-(OH)2D3 aber auch eine Inhibierung des Zellwachstums von Keratinozyten.
Diese Ergebnisse zeigen erstmals, dass 1,25-(OH)2D3
antiapoptotische Eigenschaften in Keratinozyten besitzt und diese über die
Bildung von SPP vermittelt werden.

Dr.
Bernhard Homey
Bedeutung
der Chemokine in Dermatologie, Allergologie und Onkologie
Hautklinik der Heinrich-Heine-Universität, Düsseldorf
Chemokine sind kleine (8-11kD) Zytokin-ähnliche Proteine. Zur Zeit kennen wir 42 humane Liganden, die sich in 4 Unterfamilien (CC, CXC, C, CX3C) aufteilen lassen. Chemokine binden an G-Protein-gekoppelte Rezeptoren (n=18) und vermitteln die feste Adhäsion von Leukozyten an Endothelzellen sowie deren gerichtete Migration. Studien der letzten Jahre haben gezeigt, dass Chemokine wichtige Botenstoffe für das Organ-spezifische “Homing“ von Leukozyten in lymphatische sowie periphere Organe (z.B. Haut) unter homoöstatischen sowie entzündlichen Bedingungen sind. Darüber hinaus vermitteln Chemokine über ihre Interaktion mit Chemokinrezeptoren auf der Oberfläche von Tumorzellen Organ-spezifische Metastasierungsprozesse. Experimentelle sowie klinische Beobachtungen weisen darauf hin, dass chronisch entzündliche und autoimmune Erkrankungen der Haut, wie die atopische Dermatitis und Psoriasis, T-Zell-vermittelte Krankheiten darstellen. Kürzlich wurde ein haut-spezifisches homeostatisches Chemokin (CCL27), welches ausschließlich in epidermalen Keratinozyten gebildet wird, entdeckt. Dieses neue CC-Chemokin vermittelt über die Interaktion mit seinem spezifischen Rezeptor CCR10 die Rekrutierung von haut-infiltrierenden “Memory“ T-Zellen in vitro und in vivo. Weitere Studien zeigten, dass das homeostatische Chemokin CCL27 mit inflammatorischen Chemokinliganden von CCR4 kooperiert, um Zellen in entzündete Haut zu locken. Zusammenfassend weisen diese Beobachtungen darauf hin, dass Antagonisten gegen Chemokinrezeptoren interessante Kandidaten für die Entwicklung neuer Therapiestrategien zur Behandlung von chronisch entzündlichen und autoimmunen Erkrankungen der Haut darstellen.

Prof.
Dr. Alfred Fahr
unter Mitarbeit von Daya Dass Verma
Bedeutung
von Liposomen für die Verkapselung lipophiler Wirkstoffe in der Dermatologie
Friedrich-Schiller-Universität,
Institut für Pharmazeutische Technologie, Jena
Philipps-Universität,
Institut für Pharmazeutische Technologie und Biopharmazie, Marburg
Seit einigen Jahren wird besonders aus der Arbeitsgruppe um G.
Cevc in München berichtet, dass Liposomen mit relativ fluiden Membranen und
darin eingeschlossenen diversen Substanzen in die tieferen Schichten der Hornhaut
und noch tiefer wandern können, sofern sie in wässrigem Medium nicht-okklusiv
auf die Haut aufgetragen werden. Besonders hydrophile Arzneistoffe, die in dem
inneren wässrigen Kompartiment der beschriebenen Liposomen eingeschlossen
wurden (wie z.B. Insulin), können mit dem beschriebenen Trägersystem
in die tieferen Schichten der Haut wandern. Ebenfalls wurde in der neueren Literatur
von derselben Arbeitsgruppe berichtet, dass z.B. Insulin über diese Verabreichungsart
schlussendlich im systemischen Kreislauf auftauchen und dort entsprechende pharmako-dynamische
Effekte auslösen kann.
Wir konnten die Penetration hydrophiler Arzneistoffe
in tiefere Hautschichten durch Einschluss von leicht nachweisbaren Modellarzneistoffen
wie z.B. Carboxyfluorescein in Liposomen mit flexibler Hüllmembran an einem
Modellsystem messen. Das einfache Modell setzte sich zusammen aus exzisierter
Humanhaut aus der plastischen Chirurgie und einer Franz-Zellen-Apparatur. Die
verwendeten Methoden waren Filmabrisstechnik, Kryomikrotomie und konfokale Laserscanningmikroskopie.
Bei diesen Untersuchungen wurden auch spezifischere Parameter der liposomalen
Formulierung gefunden, die das Ausmaß dieser Penetration deutlich mitbestimmen.
Zu unserer Überraschung fanden wir mittels der eben beschriebenen Liposomen auch für besonders lipophile Arzneistoffe an unseren Modellsystemen eine Penetrationsverbesserung. Neben diesen Untersuchungen an der exzisierten Humanhaut stand uns auch ein Tiermodell für Alopecia areata (DEBR: Dundee experimental bald rats) zur Verfügung (Dr. R. Hoffmann, Hautklinik, Universität Marburg). An diesem Modell konnte durch topische nicht-okklusive Administration von Cyclosporin-A (einem Immunsuppressivum) in flexiblen Liposomen auf der felllosen Haut ein eindeutiger Therapieerfolg erzielt werden. Innerhalb weniger Wochen zeigte sich an den behandelten Stellen ein normales Fellwachstum. Klassische Penetrationsverstärker wie Alkohol zeigten hingegen keinerlei therapeutische Erfolge an dem Tiermodell. Eine Korrelation der In-vitro-Ergebnisse mit den Tierversuchen war möglich. Auch in dieser liposomalen Formulierung konnten Parameter bestimmt werden, die das Penetrationsvermögen der Liposomen modulieren.
Fluide Liposomen sind nach unseren experimentellen Ergebnissen eine brauchbare Darreichungsform zur topischen Verabreichung vieler hydrophiler und lipophiler Arzneistoffe in tiefere Hautschichten. Je nach Arzneistoff muss die Formulierung mittels pharmazeutisch-technologischer Methoden optimiert werden.

Studiengang Kosmetik
und Körperpflege, Universität Hamburg
Die
Frage, ob extern auf die Haut applizierte Grundlagen und die damit verbundene
Hydratation des Stratum corneum die UV-Durchlässigkeit der Haut und somit
die Wirkung von UV-Strahlung verstärken, ist bis heute nicht abschließend
beantwortet. So zeigten manche Studien eine Verstärkung der UV-Wirkung (1),
andere Studien hingegen zeigten keine Änderung der UV-Wirkung an der Haut
(2). Während die Frage, ob hydrierende Externa Durchlässigkeit und Empfindlichkeit
der Haut gegenüber UV-Strahlung steigern lange Zeit unter dem Gesichtspunkt
der Erhöhung der therapeutischen Effizienz von UV-Behandlungen gesehen wurde,
ist in jüngerer Zeit die Frage, ob durch eine Hydratation der Haut die UV-bedingte
Hautalterung beschleunigt werden kann, in den Vordergrund gerückt. Es sollen
daher im Folgenden die Ergebnisse einer Studie vorgestellt werden, in der der
Einfluss von Unguentum emulsificans mit unterschiedlichem Wassergehalt auf die
UVB-Empfindlichkeit der Haut untersucht wurde (3). Hierzu wurden 10 hautgesunde
Probanden in die Studie eingeschlossen. Bei jedem Probanden wurden 6 UVB-Lichttreppen
durchgeführt. Auf die Bestrahlungsfelder wurden jeweils vor UV-Exposition
in einem doppelblind randomisierten Design Unguentum emulsificans und 4 Verdünnungen
mit jeweils 30, 50, 70 und 90 % Wasser aufgetragen. Die Felder der sechsten Testreihe
blieben als Kontrolle unbehandelt. Es erfolgte eine UV-Bestrahlung mit UVB-Dosen
von 0,01, 0,03, 0,06, 0,09, 0,12 und 0,15 J/cm². Nach 24 h wurde die MED-UVB
abgelesen und ein Erythemsummescore (ESS) bestimmt.
Die Ergebnisse der Untersuchung
konnten keinen Einfluss der extern auf die Haut aufgetragenen Präparate auf
die UVB-Empfindlichkeit zeigen. Die mittlere MED betrug 0,087 ? 0,021, 0,087 ?
0,025, 0,087 ? 0,0225, 0,087 ? 0,022, 0,087 ? 0,016 und 0,0854 ? 0,012 für
das Kontrollfeld. Auch für den ESS ergaben sich keine signifikanten Unterschiede.
Zusammenfassend kann man festhalten, dass gemäß den Ergebnissen der
vorliegenden Untersuchung nicht auf eine erhöhte UVB-Sensitivität verbunden
mit einer erhöhten Gefahr der aktinischen Schädigung infolge Applikation
von Unguentum emulsificans geschlossen werden kann. Zur Bestätigung der Ergebnisse
dieser Pilotstudie sind allerdings Untersuchungen mit einer größeren
Zahl von Probanden und mit weiteren unterschiedlichen Galeniken erforderlich.
(1) Berne B., Blom I., Spangberg S. Enhanced response of psoriasis to
UVB therapy after pre-treatment with a lubricating base. A single-blind controlled
study. Acta Derm Venereol . 70, 474-7, 1990
(2) Lebwohl M., Martinez J., Weber P., DeLuca. Effects of topical preparations on the erythemogenicity of UVB: implications for psoriasis phototherapy. J Am Acad Dermatol. 32, 469-71, 1995
(3)
Behrens-Williams S.C., Kraus D., Reuther T., Kerscher M.J. Do we alter ultraviolet
sensitivity in vivo with stratum corneum rehydration? A pilot study and review
of the literature. Br J Dermatol. 146, 280-284, 2002

Prof.
Dr. Manfred Kietzmann
Das
isoliert perfundierte Kuheuter: Modell der kutanen Absorption
Institut für Pharmakologie, Toxikologie und Pharmazie, Tierärztliche Hochschule Hannover
Der Untersuchung der transdermalen Penetration, Permeation und Resorption von Stoffen kommt bei der Entwicklung von topisch applizierbaren Arzneimitteln (einschließlich transdermaler therapeutischer Systeme) und von Kosmetika große Bedeutung zu. Auch sind Daten zur transdermalen Resorption toxikologisch relevanter Stoffe, mit denen der Organismus in Kontakt kommen kann, zu erarbeiten. Um aussagekräftige Ergebnisse bezüglich der dermalen Resorption (der Aufnahme in das Gefäßsystem) zu erzielen, erscheint die Verwendung perfundierter Hautmodelle gegenüber In-vitro-Modellen mit nicht perfundierter Haut grundsätzlich vorteilhaft.
So wurde das isoliert perfundierte Rindereuter als In-vitro-Modell für die Untersuchung der transdermalen Resorption von Stoffen eingeführt (Kietzmann et al., J. Pharmacol. Toxicol. Methods 30, 75 84, 1993), da es eine gut zugängliche arterielle und venöse Gefäßversorgung besitzt, die in vitro eine Perfusion mit unterschiedlichen Perfusionsmedien (z.B. Tyrodelösung, Blut) ermöglicht. Anhand während der Perfusion erfasster Vitalitätsparameter wurde gezeigt, dass das Gewebe in funktionsfähigem Zustand bleibt. Die große Applikationsfläche sowie die Menge von etwa 100 ml Perfusionsflüssigkeit, die das isolierte Organ pro Euterhälfte in einer Minute durchströmt, erlauben es, auch geringe Wirkstoffmengen nach entsprechender Anreicherung aus dem Perfusat ohne Verwendung radioaktiv markierter Stoffe nachzuweisen.
Als Beispiel für die Verwendungsmöglichkeit werden im Vortrag Ergebnisse aus Untersuchungen zur perkutanen Resorption von Betamethason aus verschiedenen Formulierungen, von Estradiol aus transdermalen therapeutischen Systemen sowie von Nonylphenol und Bisphenol A als toxikologisch relevante Stoffe dargestellt. Betamethason 17,21 dipropionat wurde topisch als Lösung, Creme sowie Salbe ohne Propylenglykolzusatz sowie als Salbe und Gel mit Propylenglykolzusatz auf die Euterhaut aufgebracht. Zusätzlich wurde die Resorption aus den genannten Versuchsmustern nach Schädigung der Barrierefunktion der Hornschicht durch wiederholte Applikation von Aceton untersucht. Nach Behandlung mit der Salbenformulierung ohne Propylenglykol wurde Betamethason 17,21 dipropionat in einem größeren Ausmaß als nach Applikation als Lösung oder Creme resorbiert. Für die Salbe mit Propylenglykolzusatz war eine gegenüber der Salbe ohne Propylenglykol geringgradig gesteigerte Resorptionsrate nachweisbar. Die Resorptionsrate war bei geschädigter Hornschicht nach Applikation von Salbe, Creme und Gel signifikant erhöht. Beim Vergleich der Freisetzung und Resorption von Estradiol aus verschiedenen Pflasterformulierungen konnten prädiktive Aussagen zur Bioverfügbarkeit beim Menschen gemacht werden. In diesen Untersuchungen wurde neben der resorbierten Menge (Konzentration im Perfusat) auch die Konzentration in der Hornschicht (Tesafilmabrisse) und in Gefriermikrotom-Schnitten der Haut ermittelt. Bei den Untersuchungen mit Bisphenol A und Nonylphenol wurde durch die Verwendung stabiler Isotope eine sehr sichere und empfindliche Nachweismethode eingesetzt, die den erstmaligen Nachweis der transdermalen Aufnahme dieser Stoffe erlaubte. Am isoliert perfundierten Rindereuter wurde in der Vergangenheit neben den genannten Substanzen die transdermale Penetration, Permeation und Resorption einer großen Zahl weiterer Stoffe untersucht (z.B. Isosorbiddinitrat, Glyceroltrinitrat, Benzoylperoxid, Benzoesäure, Testosteron, Hydrocortison u.a.).
Mit dem isoliert perfundierten Rindereuter steht somit ein In-vitro Modell zur Verfügung, welches einen Beitrag zur Beantwortung von Fragen zur dermalen Penetration, Resorption von Stoffen und zur Einsparung von Tierversuchen leistet.

DNS-Reparaturenzyme: Einsatz bei aktinischen Hautschäden und Xeroderma pigmentosum
Institut für
Umweltmedizinische Forschung (IUF) an der Heinrich-Heine-Universität Düsseldorf
gGmbH
Die solare ultraviolette (UV-) Strahlung kann an der menschlichen Haut eine Vielzahl schädigender Wirkungen entfalten, die unter anderem insbesondere auch zum Auftreten von Präkanzerosen wie z.B. aktinischen Keratosen sowie von Plattenepithelkarzinomen und Basalzellkarzinomen (= heller Hautkrebs) führen. Hierfür sind sowohl die kurzwelligere UVB-Strahlung (290-320 nm) als auch die langwelligere UVA- Strahlung (320-400 nm) verantwortlich. Die Entwicklung effektiver photoprotektiver Ansätze zur Prophylaxe und Verminderung der Hautkrebsentstehung der menschlichen Haut setzt präzise Kenntnisse über die photobiologischen und molekularen Mechanismen voraus, durch die UVB- und UVA-Strahlung karzinogen wirken. In diesem Zusammenhang ist interessant, dass von uns und anderen in den letzten Jahren gezeigt werden konnte, dass UVB-induzierte biologische Wirkungen an der menschlichen Haut nahezu ausschließlich auf der Generation spezifischer DNS-Schäden, insbesondere von Cyclobutanpyrimidindimeren, beruhen. Diese Läsionen stellen somit ein wesentliches Ziel für die Verhinderung der UVB-induzierten Lichtalterung dar. In der Tat konnten wir zeigen, dass es grundsätzlich möglich ist, durch die topische Applikation von in Liposomen verpackten DNS-Reparaturenzymen auf die zuvor UVB-bestrahlte menschliche Haut UVB-induzierte DNS-Schäden teilweise zu reparieren. Diese Reparatur ist funktionell relevant, denn hierdurch können z.B. UVB-induzierte immunsuppressive Effekte verhindert werden. Neueste klinische Untersuchungen wiesen zudem darauf hin, dass durch die regelmäßige Anwendung topisch applizierter DNS-Reparaturenzyme das Neuauftreten von aktinischen Keratosen und Basalzellkarzinomen bei Patienten mit erhöhtem Hautkrebsrisiko wie z.B. Xeroderma pigmentosum signifikant vermindert werden kann. Diese Untersuchungen zeigen, dass die topische Applikation von DNS-Reparaturenzymen einen neuartigen und außerordentlich wirksamen Ansatz zur Vermeidung der UVB-bedingten Hautkrebsentstehung darstellen könnte.

Fumarsäureester: Welche Komponente wirkt, und wie wirkt sie?
Universitäts-Hautklinik, Kiel
Das definierte Gemisch verschiedener Fumarsäureester (Fumaderm®) ist das in Deutschland am häufigsten verschriebene Präparat zur systemischen Therapie der Psoriasis. Wissenschaftliche Untersuchungen aus den letzen Jahren haben für das in Fumaderm® als Hauptkomponente enthaltene Dimethylfumarat (DMF) und seinen Metaboliten Methylhydrogenfumarat (MHF) eine Reihe wichtiger Wirkmechanismen aufgezeigt. So führt MHF zu einer Veränderung des Sekretionsmusters stimulierter Lymphozyten mit Bevorzugung von Th2-Zytokinen wie Interleukin 4 und 5. DMF hemmt die Produktion von Chemokinen wie Interleukin 8 aus Monozyten und führt zu einer verminderten Expression von Adhäsionsmolekülen (z. B. ICAM-1) auf Endothelzellen. Die vor kurzem beschriebene Hemmung der Translokation des nuklearen Transkriptionsfaktors NF-?B durch DMF könnte die zuvor beobachteten Wirkungen erklären. Zudem ist DMF ein potenter Induktor des programmierten Zelltodes bei unreifen dendritischen Zellen und aktivierten T-Zellen, was zumindest teilweise auf dem Einfluss der Substanz auf den NF-?B Signalweg beruhen könnte.
Somit konnten für
die seit 1959 für Psoriasis-Therapie verwendeten Fumarsäureester immunologisch
bedeutsame Wirkmechnismen nachgewiesen werden.

Dr.
Bernd Fröhlingsdorf
Grundlagen
und andere Ausgangsstoffe für die dermatologische Magistralrezeptur
Caesar & Loretz GmbH, Hilden
Die Bedeutung
der dermatologischen Magistralrezeptur hat in den letzten Jahren stetig zugenommen.
Die Vorteile liegen insbesondere in der Möglichkeit, individuelle (auf die
Bedürfnisse des Patienten zugeschnittene) Arzneimittel herzustellen. Eine
Rolle spielen hierbei individuelle Dosierungen von Wirkstoffen, fixe Kombinationen
und/oder der Verzicht auf Konservierungsmittel etc.
Per Rezeptur sind
auch begrenzt haltbare Arzneimittel herstellbar, die – als Fertigarzneimittel
– sonst nicht verfügbar wären. Auch ist die Steigerung der Compliance
von großer Bedeutung für den Patienten, der sich durch sein individuell
für ihn rezeptiertes Arzneimittel optimal behandelt sieht.
Für die Magistralrezeptur stehen sehr moderne Regelwerke (z.B. NRF) zur Verfügung, die zahlreiche Standardvorschriften – auch als Basis für Individualrezepturen – anbieten.
Unsere modernen Arzneibücher enthalten ein großes Spektrum qualifizierter Wirk- und Hilfsstoffe höchster Qualitätsstufe. Auch wichtige Salbengrundlagen sind in den modernen Pharmakopöen beschrieben, wobei – aufgrund entsprechender Herstelltechnologie und Know-how – auch bei schwierigen Salbengrundlagen (z.B. wasserhaltige) häufig auf Konservierungsstoffe etc. verzichtet werden kann (z.B. Basiscreme DAC).
Voraussetzungen für die
pharmazeutische Qualität der Rezepturarzneimittel sind
– die an der
guten pharmazeutischen Praxis orientierte Zubereitung in der Apotheke sowie
– der Verlass auf Ausgangsstoffe der erforderlichen Qualität.
Diese werden
von leistungsfähigen Anbietern hergestellt, analysiert und abgefüllt
und sind in bedarfsgerechten Mengen einschließlich der notwendigen chargenbezogenen
Qualitätsdokumentation in jeder Apotheke verfügbar.

Klinische Bewertung von Dermatika im nationalen und europäischen Zulassungsverfahren
Bundesinstitut für
Arzneimittel und Medizinprodukte (BfArM), Bonn
In den letzten
Jahren wurde basierend auf der vor fast 40 Jahren erarbeiteten EWG-Direktive 65/65
ein umfangreiches Netzwerk von Regularien zur Bewertung von Arzneimitteln im europäischen
Zulassungsverfahren entwickelt. Nationale Zulassungen nach dem deutschen Arzneimittelgesetz
(AMG), welches die Vorgaben der Direktive 65/65 in nationales Recht umsetzte,
werden mehr und mehr zur Seltenheit.
Zentrales europäisches Zulassungsverfahren
Innovative oder gentechnologisch hergestellte Wirkstoffe in neuen Arzneimitteln werden grundsätzlich nach einem zentral durch die europäische Arzneimittelbehörde (EMEA) begleiteten Zulassungsverfahren in allen EU-Staaten geprüft. Vom EU-Arzneimittelausschuss (CPMP) werden dabei zwei federführende Länder als Rapporteur und Co-Rapporteur bestimmt. Diese legen in Bewertungsberichten ein Urteil über die vorgelegte Dokumentation vor.
Nationale Zulassungsverfahren
Die große Masse von Arzneimitteln, die nicht als innovativ angesehen werden, werden nach dem jeweiligen nationalen Recht – welches jedoch in jedem EU-Land auf der o.g. Direktive basiert – beurteilt, zugelassen oder abgelehnt. Die notwendigen Kriterien für Deutschland sind im AMG – quasi im Umkehrschluss – im § 25 als Ablehnungsgrund definiert. Hauptprüfkriterium ist hierbei letztlich eine nachgewiesene positive Nutzen-Risiko-Relation als wichtigster Punkt im vorbeugenden Gesundheitsschutz. Jedes andere Kriterium ist nachrangig.
Europäisches Verfahren der gegenseitigen Anerkennung
Solche nationale Zulassungen – auch sämtliche bereits früher erfolgten – sind nun die Basis möglicher weiterer Zulassungen in sämtlichen EU-Ländern. In diesem Verfahren der gegenseitigen Anerkennung (MRP) dient eine nationale Zulassung als Ausgangsprodukt für dieses Verfahren. Dieses Land fungiert dabei als Reference-Member-State (RMS). Der RMS-Staat hat einen Bewertungsbericht ähnlich dem Bericht des Rapporteurs beim zentralen Verfahren entsprechend der (einst oder gerade erst) erfolgten nationalen Zulassung zu erstellen. Das Verfahren folgt formal gewissen Modulen (CTD) in einem engen Zeitfenster. Die beteiligten Länder (Concerned Member States: CMS) können (aber müssen nicht) den Anforderungen des Bewertungsberichtes folgen. Den Abschluss bildet dann eine jeweilige „nationale Zulassung“ dieses Produktes oder eine Versagung in einigen oder allen EU-Ländern. Bei allen europäischen Verfahren ist neben dem vorbeugenden Gesundheitsschutz („kein Risiko für die Volksgesundheit“) der Abbau von Handelsbeschränkungen innerhalb der EU ein weiteres Hauptkriterium.
Die klinische Bewertung von dermatologischen Topika
Hautkrankheiten sind von Arzt und Patienten gut sicht- und kontrollierbar. Effekte positiver und negativer Art sind vom Vehikel und vom Wirkstoff bei Externaanwendung zu erwarten und sind oft nicht voneinander zu trennen. Dosierung und Dauer der Anwendung unterliegen häufig mehr den Lebensgewohnheiten des Patienten als einer streng vorgegebenen Anwendungsweise wie z. B. bei einer Tabletteneinnahme. Die therapeutische Alternative einer hier zu bevorzugenden systemischen Therapie sind aus Compliance-Gründen jedoch oft enge Grenzen gesetzt.
Zur Wirksamkeit von Topika
Somit
ist für eine rationale Dermatotherapie nicht allein die Nutzen-Risiko-Bewertung
von Interesse, sondern auch Fragen nach der Wirksamkeit einer topischen Zubereitung
mit Wirkstoffen, die zwar ein ausgeprägtes Wirkungsprofil haben, aber trotzdem
möglicherweise keine Wirkung entfalten.
Eher selten ist die Wirkung eindeutig
bestimmbar und „nur“ von Konzentration, Vehikel und Hauterkrankung abhängig,
wie bei den Glucokortikoiden. Die hier notwendigen und sinnvollen Prüfrichtlinien
für eine klinische Prüfung dieser großen topischen Arzneimittelgruppe
regeln innerhalb der EU seit Jahrzehnten die Studiengrundlagen einer klinischen
Prüfung.
Zur Wechselwirkung von Wirkstoff, Vehikel und erkrankter Haut
Die ausgeprägten Spezifika von Topika bedingen häufig in vielen Bereichen einer klinischen Arzneimittelbeurteilung andere oder den Spezifika angepasste Vorgehensweisen. So muss die Beeinflussung der Hornschicht durch die Hilfsstoffe der jeweiligen Vehikel ebenso in die Beurteilung eingehen wie mögliche Stellgrößen der perkutanen Resorption der Wirkstoffe. Diese kann in Abhängigkeit vom Vehikel, vom Hautoberflächenzustand oder der Größe der Hautoberfläche höchst unterschiedlich sein.
Daten zur klinischen Prüfung
Bei den klinischen Prüfungen können
dann davon abhängig neue Fragen zu den zu wählenden Kontrollgruppen
entstehen. Dies gilt verstärkt bei fixen Kombinationen sowie bei Prüfungen
zum Äquivalenznachweis. Die Anforderungen für eine Zulassung von Arzneimitteln
mit bekannten Wirkstoffen sind zwar relativ niedrig, doch gilt dies in der Regel
nicht für lokal anzuwendende und lokal wirkende Dermatika. Hier wurden die
o.g. Überlegungen zur Andersartigkeit solcher Produkte in einer entsprechenden
europäischen Richtlinie zusammengefasst.
Solchen Regelungswerken ist
auch zu entnehmen, dass üblicherweise ein Äquivalenznachweis zwischen
Innovatorprodukt und Generikum nur über eine vergleichende klinische Prüfung
entsprechend der hier diskutierten Kriterien gelingen wird.


Prof. Dr. Hans-Dieter
Höltje
Molecular
Modelling bei topischen Glukokortikoiden:
Korrelation der Ligand-Rezeptor-Interaktion
mit der In-vitro-Aktivität
Institut für
Pharmazeutische Chemie, Heinrich-Heine-Universität, Düsseldorf
Zum Verständnis der bekannten Unterschiede im Benefit-Risk-Quotienten
von topisch verwendeten Glukocorticoiden könnte ein molekulares Modell der
Wechselwirkung der Wirkstoffe mit der Glukocorticoidrezeptor-Bindungsstelle beitragen.
Voraussetzung für eine entsprechende Untersuchung ist ein detailliertes
3-dimensionales Modell des Glukocorticoid-Rezeptors. Wegen der hohen Homologie
der Aminosäuresequenzen konnte ein solches Modell auf der Grundlage einer
Kristallstruktur des Progesteronrezeptors entwickelt werden. Mithilfe von molekular-dynamischen
Simulationen wurden dann insgesamt 11 Corticoide optimal in die Rezeptorbindungstasche
eingepasst und die dabei erhaltenen pharmacophoren Überlagerungen für
die anschließenden QSAR-Untersuchungen verwendet. Die Größe und
Form der Bindungstasche zeigt eine gute Übereinstimmung insbesondere mit
den 17-Monoestern, wodurch deren hohe Rezeptoraffinität zwanglos erklärt
werden kann. In der Nähe der Position 21 des Steroidgerüstes zeigt die
Bindungstasche eine räumliche Begrenzung, so dass 21-Ester mit größeren
Resten als Propyl nur noch nach sterischer Anpassung des Rezeptorproteins gebunden
werden können, was zu einem Verlust an Affinität führt. Alle elf
untersuchten Liganden wurden auch für die Entwicklung eines 3D-QSAR-Modells
verwendet. Die Korrelation mit den experimentell bestimmten Bindungsaffinitäten
ergab einen Korrelationskoeffizienten r2 von 0,98 mit einem prediktiven mithilfe
der leave-on-out (LOO) Methode validierten q2 Wert von 0.79. Die Standardabweichung
der Voraussage liegt bei SDEP = 0.36. Die Qualität des QSAR-Modells wurde
dadurch bewiesen, dass für insgesamt sechs Verbindungen die Bindungsaffinität
korrekt vorausgesagt werden konnte. Die Bedeutung von zwei an der Bindung beteiligten
Aminosäuren Met 639 (dispersive Wechselwirkungen mit den Esterresten) und
Asn 564 (Wasserstoffbrücke mit 11-OH) sowohl für die Affinität
als auch die Transaktivierung und Repression des Transkriptionsfaktors konnte
inzwischen durch Mutationsexperimente bewiesen werden.
Rehydrierung des Stratum corneum: Möglichkeiten der Stimulation der keratinozytären Harnstoffsynthese
Universitätsklinik und Poliklinik für Dermatologie und Venerologie der
Martin-Luther-Universität, Halle (Saale)
L-Arginin wird in der Epidermis durch die keratinozytäre Arginase (Typ II) in Harnstoff und Ornithin metabolisiert. Als essentieller Co-Faktor dieser Reaktion und Regulator der enzymatischen Aktivität fungiert Mn2+. Zudem wird Harnstoff durch die Agmatinase aus Agmatin einem Decarboxylierungsprodukt von Arginin synthetisiert.
Die Produktion von endogenem Harnstoff durch Keratinozyten ist bei einer Reihe von Dermatosen, wie z.B. bei der atopischen Dermatitis oder der Psoriasis vulgaris, vermindert. Eine exogene Harnstoffsubstitution erhöht bekanntlich deutlich die Wasserbindungskapazität und die Hydratation des Stratum corneum. Dieser Effekt hält aber nur eine relativ kurze Zeit vor, so dass eine Anwendung mehrmals am Tag erfolgen muss. Durch eine Verstärkung des keratinozytären Harnstoffzyklus kann der Anteil an intrakorneozytärem endogenem Harnstoff erhöht und damit eine Retardierung der Harnstoffeffekte erzielt werden.
Nach qualitativem und quantitativem Nachweis der keratinozytären Arginase mit immunhisto- und immunzytochemischen sowie proteinchemischen Methoden wurde an HaCaT- und nativen Keratinozytenkulturen der Einfluss von L-Arginin und Agmatin auf das Proliferations- und Apoptoseverhalten untersucht und die Beeinflussung der Arginase-Aktivität sowie die Änderung der intra- und extrazellulären Harnstoffkonzentration bestimmt.
L-Arginin und Agmatin bewirken eine Steigerung
der keratinozytären Harnstoffsynthese. Erste klinische Studien belegen die
Wirksamkeit nach topischer Applikation.

Prof.
Dr. Victoria Kolb-Bachofen
unter Mitarbeit von C.V. Suschek, O. Schnorr,
A. Kuhn, D. Bruch-Gerharz,
und T. Ruzicka
Stickoxid
als neues therapeutisches Prinzip
Institut für Immunbiologie, Heinrich-Heine-Universität, Düsseldorf
Relativ hohe Konzentrationen von Stickstoff-Monoxid (NO) können
auch in der Haut lokal gebildet werden als Folge von entzündlichen Situationen
(1, 2), bei denen durch Zytokine die de novo Expression der induzierbaren NO-Synthese
(iNOS) ausgelöst wird. Diese hohe NO-Synthese benötigt die Aminosäure
L-Arginin und wurde als Verstärker der Gewebezerstörung angesehen, aber
neuere Untersuchungen zeigen, dass diese Sicht zu einfach war. Tatsächlich
gehen von diesem kleinen radikalischen Molekül wichtige Regulatorfunktionen
aus. Neueste Publikationen belegen, dass dem iNOS-synthetisierten NO eine wichtige
Funktion in der Hautphysiologie zukommt. So hatten wir bereits früher zeigen
können, dass die iNOS-Expression eine normale Antwort auf UV-Bestrahlung
der menschlichen Haut ist (3), und das Fehlen dieser Antwort zur richtigen Zeit
einen Krankheitsmarker bei Patienten mit cutanem Lupus darstellt. Auch fanden
wir, dass Kultur von primären humanen Keratinozyten in Gegenwart eines NO-donors
das Wachstum reguliert. Bei niedrigen Konzentrationen wird das Wachstum beschleunigt
und bei höheren Konzentrationsen die Differenzierung induziert (4). Wir können
auch zeigen, dass die endogene iNOS-Aktivität in diesen Zellen ebenfalls
eine Differenzierung auslöst, eine Antwort, die aber essentiell von der vorhandenen
Arginase-1-Aktivität abhängt. Untersuchungen an Hautbiopsien von Psoriasis-Patienten
bestätigen, dass in vivo in den Läsionen die iNOS nicht ausreichend
aktiv ist, in Korrelation zur gefundenen Arginase Überexpression (5). Des
Weiteren konnten wir auch demonstrieren, dass eine iNOS-vermittelte NO-Synthese,
aber auch exogen zugeführtes NO, zu einem vollständigen Schutz vor apoptotischem
Zelltod durch UVA-Bestrahlung führt. Dieser potente Schutz läuft über
zwei unterschiedliche Wege. NO verhindert die UVA-induzierte Lipid-Peroxidation
und trägt so zur Aufrechterhaltung der Membranintegrität bei (6). Zusätzlich
finden wir auch eine enge Korrelation mit einer NO-vermittelten Verstärkung
des anti-apoptotisch wirkenden Proteins Bcl-2 (7). Dieser NO-vermittelte Schutz
vor UV-induziertem Zelltod ist abhängig von der Verfügbarkeit der Aminosäure
L-Arginin, die das Enzymsubstrat für die NO-Synthese darstellt (8). Eine
kleine Versuchserie an 6 gesunden Probanden hat gezeigt, dass eine topisch applizierte
NO enthaltende Creme während der UV-Bestrahlung das Erythem reduziert und
gleichzeitig die Hautpigmentierung etwas verstärkt.
(1) Bruch-Gerharz
D., Fehsel K., Suschek C., Michel G., Ruzicka T. und Kolb-Bachofen V.: J. Exp.
Med. 184, 2007-2012,1996
(2) Bruch-Gerharz D., Ruzicka T. und Kolb-Bachofen
V.: J Invest. Dermatol. 110, 1-7, 1998
(3) Kuhn A., Fehsel K., Lehmann P.,
Krutmann J., Ruzicka T. und Kolb-Bachofen V.: J. Invest. Dermatol. 111, 101-105,
1998
(4) Krischel, V., Bruch-Gerharz, D., Suschek, C., Kröncke, K.-D.,
Ruzicka, T. und Kolb-Bachofen, V.: J. Invest. Dermatol. 111, 286-291, 1998
(5) Schnorr O., Bruch-Gerharz D., Suschek C., Beck K.-F., Pfeilschifter J., Ruzicka
T. und Kolb-Bachofen V.: Am. J. Pathol. 162, 203-211, 2003
(6) Suschek, C.
V., Bribiva, K., Bruch-Gerharz, D., Sies, H., Kröncke, K.-D. und Kolb-Bachofen,
V.: Cell Death Diff. 8, 515-527, 2001
(7) Suscheck, C.V., Schuy, V., Bruch-Gerharz,
D., Berenji, D., Krutmann, J., Kröncke, K.-D. und Kolb-Bachofen, V. : J.
Biol. Chem. 274, 6130-6137, 1999
(8) Suschek C., Schnorr O., Hemmrich K.,
Aust O., Klotz L.-O., Sies H. und Kolb-Bachofen V. : Circulation, 2003 in press
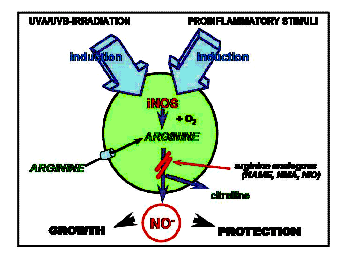
Graphik zur iNOS-Induktion und –Enzymaktivität

Prof. Dr. med. Thomas Luger
Systemische Immunsuppressiva in der Dermatologie
Klinik und Poliklinik für Hautkrankheiten der Westfälischen Wilhelms-Universität, Münster
Neue Erkenntnisse zur Pathogenese von immunvermittelten dermatologischen Krankheiten haben beträchtliche Fortschritte in der Entwicklung therapeutischer Strategien ermöglicht. Demzufolge stehen uns heute bereits mehrere neuartige systemische sowie lokale immunmodulatorische Therapien zur Verfügung bzw. sind in der klinischen Erprobung. Zu den systemischen Medikamenten, die für den dermatologischen Gebrauch entwickelt wurden, gehören z. B. die Fumarsäure, Mycophenolat Mofetil, Leflunomide, Sirolimus, Pimecrolimus u. a. Die Ergebnisse erster klinischer Studien mit Pimecrolimus für die Behandlung der Psoriasis und atopischen Dermatitis waren beachtlich und brachten bislang keine Erkenntnisse über ernsthafte Nebenwirkungen, wie z. B. Nephrotoxizität oder Hepatoxizität, die oftmals den Einsatz von Immunsuppressiva einschränken. Spezielle systemische immunmodulatorische Strategien setzen Zytokine (IL-4, IL-10, IL-11, …), humanisierte Antikörper (Dacalizumab, Infliximab, Adalimumab, Efalizumab …), Fusionsproteine (Enebrel, Alefacept, Denileukin, …) oder die erst kürzlich entwickelten „Zytokinfallen“ (cytokine traps) ein. Diese Ansätze bezwecken im wesentlichen die Funktion der Antigen-präsentierenden Zellen, die T-Zellen-Aktivierung, die Leukozytenadhäsion oder die Zytokin- und die Chemokin-Produktion zu beeinträchtigen. Einige dieser Moleküle haben sich bereits als sehr effektiv bei der Behandlung von entzündlichen Hauterkrankungen (Psoriasis) oder Tumoren (kutanes T-Zellen-Lymphom) erwiesen. Gemäß erster klinischer Studien können Impfstrategien auf der Basis von mit Tumorantigenen gepulsten autologen dendritischen Zellen eine wirkungsvolle Methode darstellen, Melanome zu behandeln. Der Wert verschiedener DNA-basierter Vakzinen wird derzeit in klinischen Studien untersucht. Diese ersten Erfahrungen mit Hilfe von biologischen Substanzen, modifizierten Zellen und DNA-Vakzinen werden entscheidend dazu beitragen, die Mechanismen zu definieren, denen eine Schlüsselrolle in der Pathogenese entzündlicher und neoplastischer Erkrankungen zukommt. Dadurch wird in Zukunft die Entwicklung neuer und verbesserter anti-entzündlicher und immuntherapeutischer Optionen ermöglicht.

Topische Immunstimulatoren in der Dermatologie: Neue Therapieoptionen durch TLR-Agonisten
Klinik für Dermatologie Universitätsklinikum Charité, Berlin
Toll-Like-Rezeptoren sind phylogenetisch hoch konservierte Rezeptoren für mikrobielle Strukturen, die auf der Zelloberfläche exprimiert werden. Unter den identifizierten mikrobiellen Bestandteilen sind Lipide, Kohlenhydrate, Proteine, aber auch DNA. Besonders bemerkenswert ist, dass Toll-Like-Rezeptoren nicht nur wie Antikörper ganz spezifische Strukturen erkennen, sondern eher Muster von Molekülen. Derzeit sind neun verschiedene Toll-Like-Rezeptoren beim Menschen bekannt.
Durch Aktivierung eines Toll-Like-Rezeptors kommt es zu einer Zytokinproduktion und somit zur Aktivierung des angeborenen und später auch des erworbenen Immunsystems im entsprechenden Areal. Nach initialer Zytokinfreisetzung, besonders Interleukin I und TNF-Alpha, werden Makrophagen aktiviert, Lymphozyten und Granolozyten angelockt und über die Lymphozyteneinwanderung später auch die Möglichkeit für die Mitbeteiligung des erworbenen Immunsystems geschaffen. Besonders bemerkenswert ist, dass derartige TLR-Agonisten topisch, aber auch intrafokal appliziert werden können.
Imiquimod ist ein Agonist des Tolla-Like-Rezeptors 7. Nachdem Imiquimod bereits zur Behandlung von virusinduzierten Papillomen im Genitalbereich zugelassen ist, haben nun zahlreiche Studien gezeigt, dass auch In-situ-Karzinome und oberflächliche Basaliome sehr gut auf eine topische Therapie mit Imiquimod ansprechen.
Ein anderes Therapieverfahren, welches in der Entwicklung noch nicht ganz soweit fortgeschritten ist, ist die Anwendung von CpG-reichen Oligonukleotiden, die eine bakterielle DNA simulieren. Derartige CpG-Oligonukleotide werden experimentell intrafokal in Hauttumoren injiziert und induzieren dort ebenfalls eine Regression.
Der Einsatz von Toll-Like-Rezeptoragonisten
kann kaum überschätzt werden und stellt eine große therapeutische
Möglichkeit nicht nur für die Dermatologie, sondern auch für zahlreiche
andere Fachdisziplinen dar.

Prof. Dr. med. Horst Spielmann
Validierung von In-vitro-Methoden in der Verträglichkeitstestung
Bundesinstitut für Risikobewertung, Berlin
Verträglichkeitsprüfungen sind behördlich vorgeschrieben, um Arbeiter während der Herstellung neuer Stoffe zu schützen, um die Sicherheit von Nahrungsmitteln und Getränken abzusichern, um Patienten vor Nebenwirkungen von Arzneimitteln und Medizinprodukten zu schützen und um Mensch und Umwelt vor Gefährdung durch chemische Stoffe und ihre Rückstände zu schützen, wie z.B. in Kosmetika. Die Standardmethode bei der Verträglichkeitsprüfung ist aus historischen Gründen der toxikologische Tierversuch. Um das Leiden von Versuchstieren bei toxikologischen Verträglichkeitsprüfungen zu vermindern, werden diese Tierversuche nach dem „3-R Konzept“ (refinement, reduction and replacement) von Russel and Burch (1959) erfolgreich durch weniger belastende Versuche ersetzt. In einem ersten Schritt führte die Harmonisierung der internationalen Vorschriften für die Verträglichkeitsprüfung zu einer deutlichen Verminderung der Versuchstierzahlen. Es ist jedoch sehr viel schwieriger, einen weltweit für die Verträglichkeitsprüfung akzeptierten Tierversuch durch eine tierversuchsfreie Alternativmethode zu ersetzen.
Inzwischen gibt
es Beispiele dafür, dass sicherheitstoxikologische Tierversuche durch tierversuchsfreie
Methoden ersetzen werden können, wenn diese ausreichend experimentell validiert
wurden, um ihre Reproduzierbarkeit und ihre Zuverlässigkeit für einen
bestimmten Zweck nachzuweisen. Das EU-Zentrum für die Validierung von Alternativmethoden
ECVAM in Ispra/Italien hat ein Konzept für die experimentelle Validierung
von Alternativmethoden entwickelt, in dem die Prävalidierung und die
Anwendung biostatistischer Prädiktionsmodelle eine entscheidende Rolle spielen.
Das ECVAM-Validierungskonzept wurde 1996 von der EU, von den USA und auch von
der OECD akzeptiert. Im Jahr 2000 war der 3T3 NRU PT In-vitro-Phototoxizitätstest
der erste experimentell validierte In-vitro-Toxizitätstest, der von der EU
Kommission offiziell als Verträglichkeitsprüfung akzeptiert wurde. In
demselben Jahr wurden außerdem nach erfolgreicher Validierung durch ECVAM
zwei In-vitro-Tests zur Prüfung auf Äztwirkung an der Haut in die Prüfrichtlinien
der EU für Chemikalien aufgenommen. Inzwischen hat auch die OECD die drei
genannten In-vitro-Toxizitätstests für die Verträglichkeitsprüfung
weltweit anerkannt. Weiterhin hat die OECD im Jahr 2002 einen In-vitro-Test für
die Prüfung auf Hautpenetration mit menschlicher Haut (Operationsmaterial)
akzeptiert und für die Prüfung auf sensibilisierende Eigenschaften eine
neue, weniger belastende Prüfmethode, den LLNA (local lymp node assay). Schließlich
wurde im Jahr 2002 eine ECVAM-Validierungsstudie von drei In-vitro- Embryotoxizitätstests
erfolgreich abgeschlossen, so dass jetzt drei validierte In-vitro- Embryotoxizitätstests
eingesetzt werden können: ein Test, bei dem ganze Rattenembryonen, und ein
Test, bei dem Extremitätenknospen von Rattenembryonen eingesetzt werden,
sowie der Embryonale Stammzell-Test (EST), bei dem im Gegensatz zu den beiden
anderen Embryotoxizitätstests keine schwangeren Tiere verwendet werden, sondern
eine embryonale Stammzelllinie der Maus.

Acne vulgaris : Entstehung, Folgen und Verbreitung
Klinik und Poliklinik für Dermatologie der Rheinischen
Friedrich-Wilhelms-Universität,
Bonn
Akne ist eine der
häufigsten Hauterkrankungen. Etwa jeder dritte Mensch zwischen 15 und 44
Jahren ist betroffen. Nach heutiger Auffassung wirken bei der Entstehung der Akne
mehrere pathogenetische Faktoren zusammen.
• Follikuläre Hyperkeratose (Komedonen)
• Seborrhoe
• Mikrobielle Besiedlung
• Entzündung
Diese pathogenetischen Faktoren wirken nicht unabhängig voneinander, sondern beeinflussen sich gegenseitig: Follikuläre Hyperkeratose einerseits und Seborrhoe andererseits schaffen offenbar im Haarfollikel ein Milieu, das den zur Standortflora zählenden Propionibakterien ein exzessives Wachstum erlaubt. Bakterielle Stoffwechselprodukte wirken chemotaktisch auf Leukozyten und initiieren so die follikulären und perifollikulären Entzündungen, die bis zur Abszedierung und Fistelgangbildung führen können. In den Akneläsionen gebildete Entzündungsmediatoren fördern wiederum die follikuläre Hyperkeratose.
Eine Conditio sine qua non für die Akne ist die Seborrhoe. Androgene, Talgbildung und Akne sind eng miteinander verbunden. Dass Seborrhoe und Akne bei normalen Androgen-Serumspiegeln auftreten, wird auf eine erhöhte Androgensensitivität der talgproduzierenden Sebozyten zurückgeführt (individuelle Aktivität des Enzyms 5alpha-Reduktase). In anderen Fällen liegt Seborrhoe und Akne eine Überproduktion von Androgenen zugrunde.
Therapeutische Interventionen
bestehen in der topischen und systemischen Antibiose, der topischen Anwendung
von Antiseptika sowie „Vitamin-A-Derivaten“ und der systemischen Therapie
mittels Kontrazeptiva bei Frauen und der systemischen Gabe von Isotretinoin für
beide Geschlechter. Kombinationen dieser Behandlungsstrategien sind je nach Schweregrad
des klinischen Bildes synergistisch wirksam.
„Präventive“
Interventionen sind in einem geringeren Maße der geeigneten Ernährung
zuzuschreiben und der frühen Erkennung und Behandlung der Akne mittels topisch
wirksamer Externa bzw. Pflegeprodukte.
Unbehandelte Formen der Akne, insbesondere
der entzündliche papulopustulöse Typ oder die Akne conglobata, führen
je nach Schweregrad zwangsläufig zu Narbenbildungen von atrophem oder hypertrophem
Charakter bis hin zur Keloidentwicklung. Diese kosmetischen Folgen sind später
nur mit kostenintensiven und aufwendigen operativen und/oder laserchirurgischen
Verfahren anzugehen.

Aknegefährdete
Haut: Pflegekonzepte aus der Apotheke
Margarethen-Apotheke,
Baldham
Die seborrhoische,
zu Unreinheiten neigende Haut ist eine Problemhaut. Um eine Verschlechterung ihres
Zustandes zu verhindern, muss sie richtig gepflegt werden. Neben der psychologischen
Betreuung der Betroffenen, die meist jugendlichen Betroffenen stehen oft unter
großem Leidensdruck, besteht die Aufgabe des Apothekers in der Bereitstellung
von adäquaten Pflegekonzepten und der Therapiebegleitung bei ärztlicher
Behandlung. Zur Reinigung, Pflege und dem Schutz der Haut sollen Produkte ausgewählt
werden, die dem aktuellen Hautzustand entsprechen. Stark lipidhaltige Formulierungen
sind zu meiden, ebenso Grundlagen und Wirkstoffe mit komedogener Wirkung. Bei
der Auswahl der Wirkstoffe sind evtl. ärztliche Verordnungen zu berücksichtigen.
Wichtig ist ein ausreichender Sonnenschutz der oft durch systemische und lokale
Behandlung gereizten und empfindlichen Haut. Erweiterte Pflegemaßnahmen
wie z.B. Packungen können, richtig ausgewählt, das Hautbild verbessern

Dr. med. vet. Wolfgang Pittermann
Kosmetische Öle: Ist die Talgdrüse das Ziel?
Henkel KGaA, Düsseldorf
Kosmetische
Öle sind Bestandteile in Cremes und Lotions, die im ´Sensory Assessment´
positiv wirksam sind und wesentlich zur Akzeptanz der Emulsionen beitragen. Die
Eigenschaften der Öle auf der Hautoberfläche gehören zu den aktuellen
Zielen dermatologischer Forschung.
Da tierexperimentelle Tests für kosmetische Inhaltsstoffe verboten sind, ist die Auswahl geeigneter Hautmodelle sehr eingeschränkt. Denn für diese Studien sind eine natürliche Hautbarriere ebenso erforderlich wie funktionsfähiger Stoffwechsel und aktive Talgdrüsen. Das 1993 in die Pharmaforschung eingeführte In-vitro-Modell des isoliert perfundierten Rindereuters (BUS-Modell) bietet diese Voraussetzungen. Die nachfolgend beschriebene Studie verfolgte den Zweck, nach verschiedenen Expositionszeiten Penetrationswege unterschiedlicher Öle in Hornschicht und Haut aufzuklären.
Es wurden fünf kosmetische Öle (INCI: Dibutyl Adipate, Dicaprylyl Carbonate, Ethylhexyl Stearate, Hexyldecanol, Octyldodecanol) für die Penetrationsstudien eingesetzt und mit der natürlichen Verteilung von Tocopherol und Triglyceriden in der Haut verglichen. Für die Hornschichtpenetration wird die Methode der Klebestreifenabrisse verwendet. Die Permeation in die Haut wird durch die Analyse von vier physiologisch unterschiedlichen Schichten (epidermo-dermal [0-150 µm], Talgdrüsen [400-600 µm], Haarpapillen [800-1000 µm] und Hypodermis [1200-1400 µm]) geprüft.
Hinsichtlich der Penetration der Öle zeigte sich, dass bereits nach 10 Minuten die Hornschicht vollständig penetriert und auch nach längeren Expositionszeiten keine Mengenzunahme erreicht wurde. Die unterschiedliche Penetrationskinetik der Öle wurde sichtbar.
Die Aufnahme in die Haut war nach einer Expositionszeit von 1,0 h und 5,0 h von einer großen Variationsbreite gekennzeichnet. Verglichen mit Dibutyl Adipate wurde Octyldodecanol mit dem Faktor 20 vermehrt aufgenommen. Auch war die Verteilung nach 1,0 h und 5,0 h innerhalb der Haut sehr unterschiedlich. Bei vier der Öle blieb der Talgdrüsenanteil nach 1,0 h und 5,0 h an der Gesamthautmenge (vier Schichten) unter 10 %. Im Vergleich dazu reicherte sich Dicaprylyl Carbonate mit 16 % bis zu 27 % nach einer Expositionszeit von 1,0 h bzw. 5,0 h in der Talgdrüsenschicht (Layer II) an.
Die Ergebnisse zeigten, dass Untersuchungen an geeigneten In-vitro-Modellen mit natürlicher Hautbarriere und integrierten Anhangsgebilden wie Talgdrüsen in der Lage sind, spezifische Eigenschaften von kosmetischen Ölen dermatologisch zu charakterisieren.

Medizinische
Hautpflege mit pH-Wert 5,5 für Haut mit Akneneigung
Sebapharma GmbH & Co. KG, Boppard
Medizinische
Hautpflege oder, moderner, Dermokosmetik bietet über die Reinigung und Pflege
der Haut hinaus einen Zusatznutzen besonders für Anwender mit Hautproblemen.
80 % aller Jugendlichen, aber auch viele Erwachsene stehen vor dem Problem, ihre
zu Akne neigende Haut adäquat zu pflegen. Bei der Hautreinigung hat sich
ein Verzicht auf alkalische Seife in wissenschaftlichen Untersuchungen als sinnvoll
erwiesen. Statt dessen haben sich Syndetpräparate mit einem pH-Wert von 5,5
bewährt. Die ausbleibende Quellung beim Waschen ermöglicht eine intensive
Reinigung. Gleichzeitig wird die Zahl der Aknebakterien (Propionibacterium acnes)
auf der Haut vermindert. Eine Reduktion der Anzahl von entzündlichen und
nicht entzündlichen Akneläsionen konnte sowohl für ein festes Syndetpräparat
mit pH-Wert 5,5 als auch für ebenfalls leicht sauren einen Reinigungsschaum
nachgewiesen werden. Um den pH-Wert-Effekt der Reinigung nicht durch anschließend
aufgetragene Pflegepräparate zunichte zu machen und die barrierefördernden
Effekte des pH-Wertes 5,5 zu nutzen, ist die Einstellung des pH-Wertes 5,5 auch
für Pflegeprodukte sinnvoll. Fett- und emulgatorfreie Pflege und antibakterielle
Wirkstoffe in der Kombination mit hydratisierenden, hautberuhigenden und regenerationsfördernden
Wirkstoffen in schwach sauren Formulierungen haben sich bei der Pflege der zur
Akne neigenden Haut bestens bewährt. Nach den vorgenannten Prinzipien wurde
die Pflegeserie sebamed clear face entwickelt.

Optionen
in der Pflege der zur Akne neigenden Haut
Boots Healthcare
Deutschland, Hamburg
Zu
Akne neigende Haut ist ein Problem, das nicht nur Jugendliche, sondern auch immer
mehr Menschen über 20 Jahre betrifft. Die Ursachen hierfür können
vielfältig sein: Neben der „klassischen“ hormonellen Umstellung
während der Pubertät kann bei Frauen über 20 Jahren sowohl ein
Testosteronüberschuss als auch eine erhöhte Empfindlichkeit der Testosteronrezeptoren
an den Talgdrüsen eine Rolle spielen. Das klassische Symptom der prämenstruellen
Akne findet sich hier wieder. Männer haben meist eine höhere Talgdrüsenaktivität
und neigen daher eher zu „fettigerer“ Haut, welches sich auch in der
Porengröße und Komedonendichte widerspiegelt.
Um den verschiedenen Gegebenheiten und Patientengruppen gerecht zu werden, sollte eine Pflegeserie die verschiedenen Anforderungen aus Verwendersicht erfüllen. Dazu gehört aus medizinischer Sicht klinisch belegte Wirksamkeit mit innovativen Inhaltsstoffen mit:
1. Antibakterieller Wirkung
2. Keratolytischer
Wirkung
3. Hautberuhigung
4. Guter Kombinierbarkeit mit Aknetherapeutika
angepasst an verschiedene Stadien der Acne vulgaris.
Und aus kosmetischer Sicht:
1.
Anwenderfreundlichkeit
2. angenehme Produkteigenschaften (z. B. parfümiert,
nicht austrocknend)
3. abdeckende Produkte
Eine kosmetische Pflege macht nur dann Sinn, wenn diese konsequent durchgeführt wird. Also müssen gerade Pflegeprodukte bei unreiner Haut hohen Ansprüchen gerecht werden, die sowohl bei Reinigung, aktiver Pflege und zur Hautberuhigung eingesetzt werden können.
Die Balneum Lutsine Pflegeserie entspricht diesen Anforderungen mit dem Reinigungsprodukt Bactopur mit Wachholderöl, Zink und Undecylensäure. Ein Peeling kann nach Bedarf mit der Balneum Lutsine Peelingcreme durchgeführt werden. Je nach Aknegrad kann eine aktive Pflege der Effloreszenzen mit Kerafnia R (Retinorm®-Komplex) oder Factor 4 (4-fach-Wirkung) erfolgen. Zur Feuchtigkeitspflege und Hautberuhigung steht Hydrafnia (Biolysat Hafnia) zur Verfügung. Eine langanhaltende, kosmetisch hochwertige Abdeckung, die über 8 Stunden sebumabsorbierend wirkt, bieten die Teint Sticks.
Balneum Lutsine bietet je nach Hauttyp und
-zustand geeignete Produkte zur Pflege der unreinen, zu Akne neigenden Haut. So
wird die Patientencompliance gefördert, die wichtig für den Therapie-
bzw. Pflegeerfolg ist.

Therapiebegleitende
Pflege der zur Akne neigenden Haut
Beiersdorf AG, Hamburg
Acne vulgaris ist eine
der häufigsten Dermatosen in den westlichen Industrienationen. Pathophysiologische
Faktoren sind eine erhöhte Sebumproduktion, eine Verhornungsstörung
in den Ausführungsgängen der Talgdrüsen sowie durch Propionibacterium
acnes ausgelöste Entzündungsreaktionen. Insbesondere bei milden Akneformen
(Acne comedonica) spielt die Hyperkeratose eine entscheidende Rolle, häufig
auch auf dem Boden einer gesteigerten follikulären Reaktionsbereitschaft
gegenüber komedogenen Stoffen. Die Behandlung mit keratolytisch wirksamen
Substanzen kann jedoch vor allem bei empfindlicher Haut Irritationen und Hauttrockenheit
verursachen. Daher ist eine komedolytische, auch therapiebegleitende Pflegebehandlung
der Haut unter Verwendung mild wirksamer, nicht-komedogener Produkte mit guter
Hautverträglichkeit sinnvoll.
Ziel der vorliegenden Studie war die Untersuchung der Wirksamkeit und Hautverträglichkeit einer medizinischen Gesichtspflegeserie für unreine, zu Akne neigender Haut (Eucerin® Unreine Haut), auch hinsichtlich ihrer Kompatibilität mit pharmakologischer Akne-Medikation.
1033 Patienten (78 % weibl., 22 % männl., mittleres Alter 23,3 Jahre) mit leichter Acne vulgaris wurden in die offene, kontrollierte Multicenterstudie aufgenommen, die in Deutschland, Österreich, Belgien und Thailand durchgeführt wurde. Aus dieser Pflegeserie erhielten die Patienten für die Hautreinigung das Reinigungsgel und Gesichts-Tonic und zur speziellen Hautpflege das Creme-Gel (getönt und ungetönt) sowie die Abdeckcreme. Die Produkte wurden gemäß ärztlicher Anweisung verwendet. Bei 610 Patienten erfolgte zusätzlich eine arzneiliche Behandlung der Akne. Bewertungen des Hautzustandes im Vergleich zum Ausgangsbefund sowie der Kompatibilität der Pflegeprodukte mit den eingesetzten Arzneimitteln wurden nach 2- und 6-wöchiger Behandlung erhoben. Zusätzlich bewerteten die Patienten bei Studienende die Hautverträglichkeit und Anwendungseigenschaften.
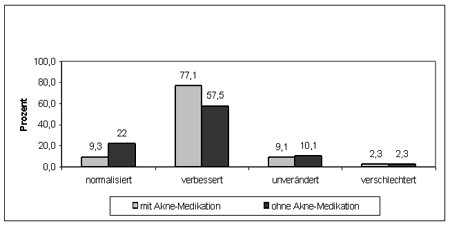
Die ärztliche Beurteilung ergab bei der Abschlussuntersuchung für 80 % der Patienten eine Verbesserung oder Normalisierung des Hautzustandes (Abb. 1). Sowohl bei der Patientengruppe mit als auch ohne arzneilicher Zusatzbehandlung nahm der Symptomscore im Vergleich zum Ausgangsbefund hochsignifikant ab. Die Hautverträglichkeit der Produkte wurde überwiegend mit „gut“ oder „sehr gut“ bewertet, unabhängig, ob eine arzneiliche Behandlung erfolgt war oder nicht. Geruch, Farbe, Konsistenz und Verteilbarkeit aller Produkte wurden zumeist mit „gut“ oder besser beurteilt. Die Patientenzufriedenheit mit den Produkten war extrem hoch und die Weiterverwendung wurde bei der großen Mehrheit der Patienten ärztlich empfohlen.
Damit stellen sich die Produkte der Serie
Eucerin® Unreine Haut als wirksam und gut hautverträglich in der alleinigen
wie auch therapiebegleitenden Hautpflege von Patienten mit leichter Acne vulgaris
dar.
Abbildung 1: Entwicklung des Hautzustandes der Patienten nach
6-wöchiger Pflegebehandlung mit den E
ucerin® Unreine Haut Produkten
mit und ohne medikamentöser Aknetherapie.

Wirksamkeitsnachweise
für Dermokosmetika für die zur Akne neigenden Haut
BioSkin GmbH, Hamburg
Die
Akne ist eine genuine Erkrankung der Haut, die in erster Linie Jugendliche und
junge Erwachsene betrifft. In 90 % aller Fälle findet sich eine natürliche
Regression der Akne im Übergang zum 3. Lebensjahrzehnt. Pathogenetisch relevant
sind im Wesentlichen vier Faktoren:
1. Primäre Faktoren:
follikuläre Hyperplasie, Talgdrüsenhyperplasie
2. Sekundäre
Faktoren: Mikrobielle Hyperkolonisation, Inflammation,
Immunreaktion
3. Genetische Faktoren
4. Exogene Einflüsse: komedogene Externa, Medikamente,
Psyche
Dieser polyfaktorischen Ätiologie muss auch die Entwicklung neuer Aknetherapeutika gerecht werden, und diese bedürfen objetivierbaren und reproduzierbaren Methoden in klinischen Studien zur Darstellung des Wirksamkeitsnachweises.
Zur Beurteilung der Wirksamkeit in der Entwicklung befindlicher Substanzen zur Verbesserung der kutanen Manifestationen der Akne stehen verschiedene Methoden zur Verfügung. Dabei stellt die dematologisch-klinische Beurteilung naturgemäß ein wichtiges Standbein dar. Die Evaluierung der zur Akne gehörenden Hautläsionen sollte stets durch fachdermatologische Bewertung mittels vor Studienbeginn definierter Bewertungsskalen vorgenommen werden. Bewährt hat sich in praxi dazu die folgende nach Allen und Smith modifizierte Bewertungsskala, die neben der relativen Betroffenheit der Gesichtsfläche auch die Unterscheidung inflammatorischer (Pusteln, Papeln) und nicht-inflammatorischer (offene und geschlossene Komedonen) Hautveränderungen heranzieht.
Akneschweregradeinteilung modifiziert nach Allen u. Smith
| Grad | Klinik |
| 0 | Gesicht fast frei, einige wenige Komedonen oder Papeln können verstreut vorhanden sein, aber sind nur bei näherer Inspektion erkennbar. |
| 2 | Etwa ¼ des Gesichts ist befallen mit kleinen Papeln und großen oder kleinen Komedonen. Einige wenige Pusteln oder größere Papeln vorhanden. |
| 4 | Etwa die Hälfte des Gesichts ist befallen mit kleinen Papeln und großen oder kleinen Komedonen. Gewöhnlich sind einige Pusteln oder deutlich prominente Papeln vorhanden (wenn die Effloreszenzen besonders groß sind, wird der Patient Grad 4 zugeordnet, auch wenn nicht über die Hälfte des Gesichts betroffen ist). |
| 6 | Über 3/5 des Gesichts mit Papeln und/oder großen offenen Komedonen befallen (befallene Fläche kann geringer sein, falls entzündliche Effloreszenzen besonders groß). Zahlreiche Pusteln sind gewöhnlich vorhanden, einige davon besonders groß. |
| 8 | Praktisch das gesamte Gesicht mit großen auffälligen Pusteln befallen; häufig stark entzündlich. Weitere Aknecharakteristika (Fistelgänge, Zysten, Abszesse) vorhanden. |
Der Score sollte zusätzlich mit klinischen Beispielphotographien unterlegt sein, insbesondere wenn mehrere Dermatologen an der Prüfung beteiligt sind. Neben der klinischen Einschätzung kommen technische Methoden zur Erfolgskontrolle in Betracht. Hinsichtlich der Sebumsekretion finden die Sebumetrie und die Sebu-Tape®-Evaluierung Anwendung. Bei beiden Methoden ist es von großer Bedeutung, die circadianen Schwankungen in der Talgsekretion zu berücksichtigen und alle Messungen im Studienverlauf zur gleichen Tageszeit durchzuführen. Ferner muss der Einfluss klimatischer Faktoren auf die Talgproduktion durch standardisiert klimatisierte Räumlichkeiten bei der Messung korrigiert werden. Die Nichtbeachtung der genannten Faktoren liefert keine verwertbaren Ergebnisse.
Zur vergleichenden Beurteilung verschiedener Studien zur Wirksamkeit von Dermokosmetika sollten die Beurteilungskriterien und –methoden vereinheitlicht werden.

Dr. Betsy Hughes-Formella
Bedeutung
von Probandendaten bei der Zulassung von Dermatika
BioSkin GmbH, Hamburg
Die frühen klinischen Phasen haben im allgemeinen zum Ziel, die
Verträglichkeit und das Verhalten des Wirkstoffes im Körper zu beurteilen.
Für äußerlich anzuwendende Arzneimittel sind Daten gesunder Probanden
aus Phase-I-Studien zur Hautverträglichkeit, Phototoxizität, zum allergenen/photoallergenen
Potential sowie zur systemischen Toxizität erforderlich.
Normalerweise
wird die Wirksamkeit zunächst in Phase-II-III-Studien mit Patienten, bei
denen ein therapeutischer Nutzen erwartet werden kann, untersucht. Die Haut bietet
jedoch die einzigartige Möglichkeit, die Wirksamkeit in experimentellen Modellen
mit gleichzeitigen (intraindividuellen) Vergleichen gesunder oder symptomatischer
Probanden zu untersuchen. Die dadurch erhaltenen Daten können für eine
Zulassung von einigen „Over-the-Counter“-Arzneimitteln oder Generika
ausreichend sein. Für andere Arzneimittel können „Proof of Concept“-Untersuchungen
in den frühen Phasen dazu dienen, die Wirksamkeit zu belegen, bevor kostspieligere
Entwicklungsphasen eingeleitet werden.
Beispiele zu gesunden Probanden
sind:
Die Förderung der Wundheilung in der frühen Phase der Reepithelialisierung
kann mit Hilfe der Saugblasenmethode in 20 – 40 Probanden bewertet werden. Durch
diese Methode wird ein epidermaler Defekt definierter Größe, der an
die Basalmembran grenzt, durch die Erzeugung von Blasen und die Entfernung der
Blasendecke erreicht. Der transepidermale Wasserverlust von Wunden ist eine geeignete
Variable, die mit dem Grad der Reepithelialisierung korreliert. Die kritische
Phase der Epithelial-Regeneration erfolgt bereits in den ersten Tagen nach der
experimentellen Wunderzeugung.
Topische Kortikosteroide können mit
Hilfe des Vasokonstriktionstests geprüft werden. Dieser pharmakodynamische
Test basiert auf der Eigenschaft von Kortikosteroiden, ein Blanching oder eine
Vasokonstriktion in der Mikrovaskularisation der Haut zu erzeugen. Die FDA erkennt
diese Methode seit vielen Jahren an, um generische topische Kortikosteroide zuzulassen.
Standardisierte Vergleiche entzündungshemmender Mittel können mit
21 – 42 Probanden mittels eines UV-Erythem-Testmodells vorgenommen werden. Die
Entzündung wird durch UV-Bestrahlung erzeugt, und die Erythem-Suppression
in dem behandelten Testfeld wird durch chromametrische Messungen und klinische
Beurteilung bewertet.
Privatdozent
Dr. med. Sigbert Jahn
Biologicals:
Neue Substanzklasse in der Dermatotherapie
BIOGEN
GmbH, Ismaning
Der immunpathogenetische Hintergrund vieler
chronisch rezidivierender Dermatosen wird zunehmend klarer. Aus diesem Verständnis
erwächst eine Reihe neuer Therapieansätze.
Die Psoriasis stellt
sich heute als ein (zumeist unvollständig verstandenes) pathogenetisches
Puzzle dar. Die Keratinozyten-Fehlregulation ist dokumentiert in Hyper- und Parakeratose.
Im dermalen Entzündungsinfiltrat produzieren neutrophile Granulozyten große
Mengen IL-8, die Angiogenese ist deutlich vermehrt. Zunehmend verstehen wir den
Beitrag des Immunsystems zur Pathogenese der Psoriasis. Langerhans-Zellen transportieren
Antigen-Material in den Lymphknoten und präsentieren es dort an T-Lymphozyten.
Antigen-geprägte T-Lymphozyten erreichen über die Blutbahn mit Hilfe
ihrer haut-spezifischen Adhäsions-(Homing-)Rezeptoren die Dermis und werden
von Langerhans-Zellen erneut mit Antigen konfrontiert. Hier kommt es offenbar
durch eine immunologische Kreuzreaktion zur Auslösung einer dysregulierten
Immunantwort. Basierend auf diesem Wissen enstand die inzwischen gut belegte Hypothese
von der Psoriasis als einer anti-bakteriellen, kreuzreaktiven, sterilen, T-Zell-vermittelten
Autoimmunerkrankung.
Das Verständnis der Immunpathogenese der Psoriasis
und anderer Dermatosen hat zur Entwicklung einer Reihe neuer immunolgisch aktiver
Substanzen (Biologicals) geführt, die in den kommenden Jahren den Markt erreichen
werden. Als Biologicals werden rekombinante Proteine verstanden, die in immunregulatorische
und Entzündungs-Mechanismen eingreifen. Zu unterscheiden sind Interleukine/Interferone,
monoklonale Antikörper (Endung -mab) und Fusionsproteine (Endung -cept).
Die therapeutische Beeinflussung der Psoriasis erfolgt durch: (a) Verhinderung
der T-Lymphozytenaktivierung, (b) Blockierung pro-inflammatorischer Zytokine,
(c) Korrektur des gestörten Th1/Th2-Zytokinprofils, (d) Verhinderung der
Extravasation von aktivierten T-Lymphozyten in die Haut und (e) die selektive
Immunmodulation unter Berücksichtigung spezifischer Marker der pathogenetisch
relevanten T-Lymphozyten. Ähnliche Ansätze werden bei weiteren, T-Lymphozyten-vermittelten
dermatologischen Erkrankungen klinisch erprobt.
Prof.
Dr. Gregor Cevc
Einsatz
selbstregulierender Träger in der Dermatologie
IDEA
AG, München
Die Hauptbarriere der Haut, das Stratum
corneum, ist durch weitgehend kristalline Lipidlamellen, die an die Plasmamembranen
gekoppelt sind, versiegelt. Die gesunde
Haut durchdringen folglich vorwiegend
kleine und hydrophobe Substanzen (Molmasse
< 300 Da), die durch Defekte
in der interzellulären Lipidmatrix diffundieren können;
die 0.4
nm engen hydrophilen Passagen durch das Stratum corneum spielen praktisch
keine Rolle (1), außer bei der transepidermalen Verdunstung von Wasser (Molmasse
18 Da; Durchmesser 0.3 nm).
Gängige dermatologische Formulierungen
optimieren folglich den Arzneimitteltransport in die Haut auf dem Wege der Maximierung
der Diffusion durch das Stratum corneum (1): am besten erhöht man die Wirkstoffkonzentration
auf der Haut und/oder fördert die Löslichkeit und Diffusion des Wirkstoffs
in der Lipidmatrix in der Hornschicht der Haut. Diverse Löslichkeits- und
Permeationsverstärker sowie eine (Semi-)Okklusion der Haut werden dafür
verwendet. Eine interessante Ausnahme bilden die oberflächlich hydrophilen
ultradeformierbaren Wirkstoffträger. Diese überwinden die Hautbarriere
durch reversible Erweiterung der interzellulären Kontakte in der Haut (2),
begleitet durch die Verformung der sehr elastischen Träger selbst (3,4).
Die resultierenden, transient geöffneten, hydrophilen interzellulären
Passagen sind im Durchschnitt schätzungsweise etwa 30 nm breit und können
auch sehr großen, ausreichend deformierten Wirkstoffträgern (Durchmesser
>100 nm) den Durchgang durch das Stratum corneum gewähren. Das lässt
sich in Modellsystemen überzeugend testen und belegen (4).
Eine
früher übersehene Antriebskraft für den Transport von großen
hydrophilen Gebilden durch die Haut ist das Wasserkonzentrationsgefälle über
das Stratum corneum (5), das effiziente Wirkstoffverabreichung in die Haut auch
ohne Okklusion erlaubt Die Verteilung geeigneter, stark hydrophiler und verformbarer
Wirkstoffträger in der lebenden Haut ist folglich durch die lokal aufgetragene
Trägermenge und nicht durch die Träger- oder Wirkstoff-Konzentration
geregelt (1,5). Das erlaubt kontrollierte, z.T. selbstregulierende Verabreichung
kleiner (1) (chemischer) und großer (3) (makromolekularer) Wirkstoffe mittels
ultradeformierbarer Träger in und durch die Haut.
Der Einsatz von
hochdeformierbaren, selbstregulierenden Wirkstoffträgern (Transfersom®;
eine Schutzmarke von IDEA AG) zur gezielten Behandlung der Haut und der subkutanen
Gewebe wird für mehrere etablierte Arzneimittel beispielhaft dargestellt
(6,7,8).
Literatur:
(1) Cevc, G., Exp. Opinion Invest.
Drugs 6 , 1887-1937, 1997
(2) Schätzlein, A., Cevc, G., Br. J. Dermatol.
138, 583-592, 1998
(3) Cevc, G. et al. Biochim. Biophys. Acta 1368, 201-215,
1998
(4) Cevc, G. et al. Biochim. Biophys. Acta 1564, 21-30, 2002
(5)
Cevc, G., Gebauer, D., Biophys. J. 84, 1010-1024, 2003
(6) Fesq, H. et al.
Arch. Dermatol. Res. 291,130, 1999
(7) Cevc, G., Blume, G., Biochim. Biophys.
Acta 1514, 191-205, 2001
(8) Fesq, H. et al. Br. J. Dermatol. im Druck, 2003

Dr.
Andreas Goppelt
Gentherapie
und Wundheilung
Switch
Biotech AG, Neuried
Die Sequenzierung des humanen Genoms
und die schnellen Fortschritte in der Entwicklung von Genexpressionstechniken
hat die Forscher erstmals in die Lage versetzt, die Pathomechanismen von Krankheiten
auf molekularer Ebene zu analysieren. Gentherapie ist der direkt daraus abgeleitete
Ansatz, dieses Wissen in Therapien umzusetzen. Obwohl die regulatorischen Hürden
hoch sind, gehen verschiedene Vorhersagen von einem Multimilliarden-Dollar-Markt
aus. Noch werden durch Gentherapie aber keine Umsätze erzielt.
Die
Methoden des Gentransfers beinhalten zellbasierende Technologien, virale Vektoren
und Liposomen, die von Forschern nicht nur für Ex-vivo-Experimente, sondern
auch bereits in vivo für klinische Versuche eingesetzt werden. Haut ist ein
besonders attraktives Zielorgan für Gentherapie, da sie leicht zugänglich
ist.
Wir haben einen „functional genomics“-Ansatz gewählt,
um neue Targets zur Behandlung kutaner Ulzera zu identifizieren. Die Screens basierten
auf der vergleichenden Analyse der Genexpression in Wundbiopsien gesunder Spender
und Patienten, die an chronischen Wunden leiden. Nach Analyse der zeitlichen und
räumlichen Expression der Genprodukte wurden die Zielgene im Tiermodell funktionell
validiert. Mittels biolistischem Gentransfer wurde eine transiente Überexpression
ausgewählter Zielgene in experimentell gesetzten Wunden erreicht, was die
Reepithelialisierungrate und die Bildung von Granulationsgewebe in der Wunde signifikant
erhöhte.
Diese Ergebnisse zeigen, dass mit unserem Ansatz valide
Targets für eine Wirkstoffentwicklung gefunden wurden, die direkt für
die Behandlung schwer zu heilender Wunden eingesetzt werden können.

Dr.
Albrecht-Georg Schmidt
Globale
Prüfstrategien bei neuartigen Ekzemmitteln
Novartis
Pharma AG, Clinical Development, Basel, Schweiz
Üblicherweise
werden neue Medikamente zunächst bei Erwachsenen und erst später bei
Kindern entwickelt. Die atopische Dermatitis manifestiert sich jedoch bereits
im Kindesalter. Dies stellt eine besondere Herausforderung für die klinische
Entwicklung neuartiger Ekzemmittel dar. Am Beispiel des klinischen Entwicklungsprogrammes
für Elidel 1 % Creme (Pimecolimus) soll dargestellt werden, wie diese Herausforderung
in Zusammenarbeit mit Patienten, Ärzten und regulatorischen Behörden
erfolgreich adressiert wurde.
Die klinischen Phase-3-Studien für
Elidel wurden nach weltweit einheitlichen Protokollen durchgeführt. Die Schwerpunkte
des Studienprogrammes lagen zum einen auf der Behandlung von Kindern und Kleinkindern
(mehr als 1000 wurden in Phase 3 mit Elidel behandelt, davon n = 678 für
6 Monate oder länger), zum anderen auf der Untersuchung der Wirksamkeit und
Sicherheit einer Langzeit-Behandlungsstrategie, innerhalb derer Elidel frühzeitig
(bei ersten Krankheitssymptomen) zur Verhinderung von Krankheitsschüben eingesetzt
wird. Diese Elidel-Behandlungsstrategie unterscheidet sich damit von der bisher
üblichen reaktiven, kurzzeitigen Intervention mit topischen Kortikosteroiden.
Topische Steroide wurden nur verabreicht, wenn es unter der Studienbehandlung
zu Krankheitsschüben kam. In den doppel-blinden Studien war bei mehr als
60 % der mit Elidel behandelten Patienten über den Zeitraum eines Jahres
keine Behandlung mit Kortikosteroiden notwendig. Dabei zeigte Elidel ein sehr
gutes Tolerabilitäts- und Sicherheitsprofil.
Die angewandte Prüfstrategie
erlaubte damit nicht nur die Untersuchung einer neuen Substanz, sondern zugleich
einer neuen Behandlungsstrategie, die über die bisher übliche kurzzeitige,
reaktive Intervention mit topischen Steroiden hinausweist. Das vollständige
Potential dieser frühzeitig einsetzenden, intermittierenden Langzeitherapie
mit Elidel wird derzeit in weiteren internationalen Studien untersucht.

Dr.
Marcel Langenauer
Konstanz
und Wandel bei Vehikeln dermatischer Wirkstoffe
Spirig
Pharma AG, Egerkingen, Schweiz
Bei näherer Betrachtung
dieses Themas ist es lohnenswert, eine Unterteilung in Dermatika, sprich Arzneimittel
zur Behandlung von Hautkrankheiten, und Dermokosmetika vorzunehmen. Sind doch
die Unterschiede punkto Wandel oder Konstanz zwischen diesen beiden Produkteklassen
am größten.
Dermatika: Grundsätzlich kann man
sagen, dass sich die Vehikel bei den Dermatika in den letzten paar Jahren kaum
verändert haben. Man setzt nach wie vor auf altbewährte einfache Trägersysteme
mit wenigen Einzelkomponenten, die problemlos und einfach herzustellen und bei
höheren Temperaturen stabil sind. Auch sind die Lebenszyklen solcher Produkte
meist sehr lange (> 10 Jahre). Die entsprechenden Rohstoffe müssen daher
über längere Zeiträume in derselben pharmazeutischen Qualität
weltweit problemlos verfügbar sein. Ein weiterer Grund, auf bekannte Rohstoffe
zu setzen. Wegen der hohen regulatorischen Anforderungen ist man auch weniger
gewillt, Veränderungen an Produkten vorzunehmen.
Liposomale
Trägersysteme kommen speziell in letzter Zeit immer mehr auch bei Dermatika
zum Einsatz. Dabei versucht man meist hydrophile oder höher molekulare Wirkstoffe,
die nur schwer in die Haut penetrieren, besser penetrierbar zu machen. Die meisten
dieser neueren Systeme befinden sich jedoch noch im Versuchsstadium. Ist doch
die Stabilität dieser Systeme nicht unkritisch. Auch ist zu beweisen, dass
die Wirkstoffe wirklich verpackt sind und es auch bleiben.
Generell steht
bei Dermatika die Wirksamkeit der Wirkstoffe im Vordergrund. Erst wenn man diese
Wirksamkeit nicht mit einfachen und bekannten Vehikelsystemen erreicht, werden
komplexere Systeme wie z.B. liposomale Verpackungssysteme für die Wirkstoffe
eingesetzt. Hier steckt die Forschung noch in den Kinderschuhen. Eine andere Variante
wäre, spezifische lipophile Wirkstoffe für die Haut zu entwickeln, die
leichter penetrieren. Ein Beispiel dazu sind sogenannte Prodrugs. Dabei handelt
es sich meist um lipophile Derivate bekannter Wirkstoffe, die, wenn sie einmal
in der Haut sind, chemisch durch Abspaltung wieder in den Wirkstoff umgesetzt
werden. Die nächsten paar Jahre werden zeigen, wohin die Forschung gehen
wird.
Dermokosmetika: Etwas anders sieht es bei den Dermokosmetika
aus. Hier steht ganz klar die kosmetische Akzeptanz des Produktes im Vordergrund
und weniger die Wirksamkeit der eingesetzten kosmetischen Wirkstoffe. Das setzt
hohe galenische Anforderungen an die Vehikelwahl. Hier sind in den letzten paar
Jahren einige neue Rohstoffe dazugekommen. Ein Grund ist sicherlich der Umstand,
dass die Hürden für eine kosmetische Zulassung eines Rohstoffes tiefer
sind als für Pharma. Neben den klassischen nach wie vor aktuellen Systemen
kommen seit Jahren auch liposomale Systeme zum Einsatz. Im Trend sind auch Sprays
und Schäumer.
Auch sind die Lebenszyklen der Dermokosmetika meist
sehr kurz. Hier ist man eben eher gewillt, das Vehikel zu ändern oder gar
neue Produkte zu bringen, die die alten ablösen. Da die regulatorischen Hürden
tief sind im Vergleich zu Dermatika, sind solche Wechsel auch recht günstig
und schnell durchzuführen.
Generell kann man aber auch bei Dermokosmetika
sagen, dass die meisten Formulierungen nach wie vor klassische Emulsionen oder
Gele sind. Nur ist hier die Palette der einzusetzenden Hilfsstoffe um einiges
umfangreicher als bei den Dermatika. Dadurch ist es möglich, die Bedürfnisse
der Kunden noch besser zu treffen (Hautstraffung, shining effect, smooth effect
etc) und ein „customized“ Produkt zu schaffen. Kauft doch der Kunde
das Produkt vor allem deswegen, weil es ihm gefällt und weil es gut riecht
und nicht weil es wirklich wirkt!

Dr.
Julia E. Diederichs
Liposomale
und nanopartikuläre Wirkstoffträger für topische Dermatika
MCS Micro
Carrier Systems GmbH, Neuss
Nanopartikuläre Systeme
sind vielfältig beschrieben als therapeutische Arzneistoffträger zur
topischen Behandlung von Hauterkrankungen. Systeme basierend auf Phospholipiden
sind besonders attraktiv wegen ihrer vernachlässigbaren Toxizität und
dem geringen allergenen Potential aufgrund der strukturellen Ähnlichkeit
mit Zellmembranen. Phospholipide dienen als Lösungsvermittler und Penetrationsverbesserer
durch die Verkapselung von Arzneistoffen als Liposome oder durch die Bildung von
niedrigmolekularen Komplexen. Auf diese Weise können Arzneistoffe angereichert
und Depot-Effekte beobachtet werden. In einer Reihe von klinischen Studien konnte
die Überlegenheit von liposomalen Arzneistoffformulierungen gegenüber
konventionellen Applikationssystemen gezeigt werden. Es scheint jedoch so zu sein,
dass nur eine ge-schädigte epidermale Barriere es den Liposomen ermöglicht,
intakt in die Haut einzu-dringen.Gewöhnlich werden Liposome direkt in ihrer
wässrigen, dispersen Form ver-wendet oder in eine gelbildende Matrix eingearbeitet.
Dennoch sind auch mehrere Ar-ten von Phospholipid-Gelen und ihnen entsprechender
Herstellungsprozesse beschrieben. Diese Gele benötigen entweder eine relativ
große Menge Alkohol, was nur für wenige Hauterkrankungen günstig
ist, oder große Mengen Phospholipid, um eine Gelbildung sicherzustellen.
Im Gegensatz zu den oben genannten Systemen haben wir zwei verschiedene Phospholipidgel-Formulierungen
entwickelt, die über einen breiten Konzentrationsbereich der Phospholipide
die Möglichkeit bieten, die physiko-chemischen Eigenschaften des Gels maßzuschneidern,
ohne die Notwendigkeit Alkohol zuzugeben. Wenn erwünscht, können jedoch
Alkohol und andere Lösungsvermittler zugegeben werden, um die Löslichkeit
des eingearbeiteten Wirkstoffes zu erhöhen. Die Vorteile dieser Gele sind
geringes
Allergierisiko, da sie aus natürlichen Phospholipiden bestehen und emulgatorfrei
sind,
feuchtigkeitsspendend
und nicht austrocknend, da sie frei von organischen Lösungsmitteln sind
nicht fettend
gut haftend auf
Haut und Schleimhaut
Die Gele sind für die Einarbeitung von lipophilen,
hydrophilen und amphiphilen Arznei-stoffen geeignet. Bis jetzt haben wir schwer
lösliche NSAR’s und Substanzen vom Ubi-quinone-Typ wie z.B Coenzyme Q10 eingearbeitet
mit einer Stabilität von wenigstens 6 Monaten.

Dr.
Maurice Zultak
Retinoide
für Ekzeme
Basilea
Pharmaceutica AG, Basel, Schweiz
Orale und topische Retinoide
sind wirksam in der Behandlung bei einer Reihe von Dermatosen, unter anderen Akne,
Psoriasis, Erkrankungen bei Keratinisation und Lichtschaden der Haut. Mukokutane
Nebenwirkungen, insbesondere Hauttrockenheit, Erythema, Desquamation und Pruritus,
sind allgemeine Nebenwirkungen, die bei beiden Verabreichungen auftreten und als
retinoide Dermatitis beschrieben werden. Da Retinoide dazu neigen, Dermatitis
zu verschlechtern, sind sie generell nicht zu empfehlen, oder sind sogar kontraindiziert
bei Patienten mit den meisten Ekzemarten, einschließlich der atopischen
Dermatitis.
Chronische Handdermatitis ist eine häufige Hauterkrankung
mit verschiedenartigen Ätiologien, unter anderem irritative oder allergische
Kontaktdermatitis, und einem atopischen Hintergrund. Keine klare Korrelation zwischen
Ätiologien und den verschiedenen klinischen Aspekten von chronischer Handdermatitis
konnte erwiesen werden. Für Patienten, die nicht auf topische Steroide ansprechen,
stehen nur beschränkte therapeutische Behandlungsmöglichkeiten zur Verfügung.
Kürzlich wurde berichtet, dass gewisse orale Retinoide bei verschiedenen
Arten von chronischer Handdermatitis ansprechen. In einer offenen klinischen Studie
mit 38 Patienten wurde das orale Alitretinoin erfolgreich angewendet in der Behandlung
von verschiedenen Arten chronischer Handdermatitis, die auf topische Therapie
refraktär sind (Bollag et all 1999). In einer einfach-blinden Placebo-kontrollierten
Studie mit 29 Patienten konnte gezeigt werden, dass das orale Acitretinoin bei
Patienten mit hyperkeratotischen Ekzemen der Handflächen wirksam ist (Thestrup-Pedersen
et al. 2001).
Der Wirkmechanismus von Alitretinoin bei chronischer Handdermatitis
ist unbekannt. Alitretinoin ist ein Ligand sowohl für RXRs und RARs, und
RXR bildet Heterodimere mit anderen nuklearen Hormonrezeptoren. RXR-Agonisten
steigern die Th2-Funktion in vitro, und die Immunomodulation kann ebenso eine
wichtige Rolle bei dem Aktivitätsspektrum von Alitretinoin spielen (Stephensen
et al. 2002).

Dr. med. Dr. Wolfgang
Greb
Wirksamkeitsprüfungen
von Dermatika für die nationale und internationale Zulassung
FOCUS Clinical Drug Development
GmbH, Neuss
Wie in den anderen Indikationen steht auch die
Entwicklung neuer Dermatika stark unter dem Druck von Kosten- und Zeitersparnis.
Man setzt daher auf eine frühe und effiziente Erreichung von „Clinical
Proof of Concept“. Dazu gehören frühe Studien an Patienten unter
Verwendung von adaptiven Studiendesigns mit flexibler Patentenzahl und Endpunkten
sowie der Einsatz von Early Effect Markern zum Nachweis und Monitoring biologischer
Effekte, entweder als Konsequenz der Arzneimittelapplikation oder des Krankheitsverlaufs.
Um diese Prinzipien erfüllen zu können, müssen die entsprechenden
präklinischen und pharmazeutischen Arbeiten sorgfältig abgestimmt werden.
Nur bei frühzeitiger und umfassender Projektplanung ist eine optimale Abfolge
gewährleistet. Voraussetzung ist ferner eine möglichst frühe Produktdefinition
und die Festlegung von Erfolgskriterien.
Gleiches gilt auch für
die späte Phase der klinischen Entwicklung. Anhand von Beispielen werden
verschiedene Strategien demonstriert.

Einführung
zum Workshop*
Topische Immunmodulatoren (TIMs): Etablierte und zukünftige
Indikationen
Klinik und Poliklinik für Hautkrankheiten der Westfälischen
Wilhelms-Universität, Münster
*Veranstalter:
Fujisawa Deutschland GmbH, München
Wie in der gesamten Medizin, hat es in den letzten
Jahren auch in der Dermatologie Aufsehen erregende Entwicklungen in der Therapie
gegeben. Den wesentlichen Fortschritt im therapeutischen Arsenal bei der Behandlung
der Atopischen Dermatitis stellen die topischen Immunmodulatoren dar (TIM), die
spezifisch über den Mechanismus der Calcineurininhibition auf die Entzündung
bei der Neurodermitis wirken.
Seit Einführung der topischen Kortikosteroide
vor mehr als 50 Jahren stellt dies die erste wirkliche Innovation in der topischen
Therapie dar und füllt damit eine große therapeutische Lücke:
TIM sind wirksam, gut verträglich und auch bei langfristiger Anwendung sicher.
Es gibt inzwischen zwei Vertreter dieser neuen Therapeutika: Tacrolimus-Salbe ist bereits seit etwa einem Jahr erhältlich, und seit Ende des letzten Jahres steht mit der Pimecrolimus-Creme bereits der zweite Vertreter zur Verfügung.
Aufgrund ihrer molekularen Eigenschaften (Molekülgröße und Lipophilie) sind diese bei topischer Anwendung wirksam, und eine systemische Exposition ist minimal.
Beide sind für die Atopische Dermatitis zugelassen, aber auch für weitere Dermatosen, bei denen die T-Zellen eine pathogenetische Rolle spielen, ist ein Einsatz denkbar.
| |

Etablierte
Indikationen von TIMs
Klinik für Haut- und Allergieerkrankungen
der Universität Helsinki, Helsinki, Finnland
Die
einzige zugelassene Indikation für die topischen Immunmodulatoren ist die
Atopische Dermatitis (AD) oder Neurodermitis, für Tacrolimus-Salbe die mittelschwere
und schwere Form der AD und Pimecrolimus für leichte und mittelschwere Fälle.
Mit Tacrolimus-Salbe wurden vergleichbare Studien mit Kindern (ab 2 Jahren)
und mit Erwachsenen (ab 16 Jahren) durchgeführt, wobei in allen Studien Tacrolimus-Salbe
als Monotherapie angewendet wurde. Zusammenfassend kann gesagt werden, dass Tacrolimus-Salbe
in allen getesteten Konzentrationen (0,03 %, 0,1 %, 0,3 %) dem Placebo stets deutlich
signifikant überlegen war (1-4). Diese Studien hatten eine Dauer zwischen
3 und 12 Wochen. Die in den USA durchgeführten Studien konnten im Gegensatz
zu den europäischen Studien keinen signifikanten Unterschied zwischen der
0,03%igen und der 0,1%igen Formulierung nachweisen. In europäischen Studien
war die Tacrolimus-Salbe 0,1 % der 0,03%igen Formulierung deutlich überlegen.
Daher wurde von der Zulassungsbehörde FDA in den USA für Kinder nur
die schwächere Tacrolimus-Salbe 0,03 % zugelassen. Die europäische Zulassungsbehörde
EMEA ist diesem Entwurf leider gefolgt.
Tacrolimus-Salbe 0,03 % ist für mittelschwere Formen der Erkrankung
hinreichend. Bessere Behandlungserfolge in den schweren Formen wurden mit der
0,1%igen Formulierung erzielt. Dementsprechend zeigte eine einmal tägliche
Behandlung von Kindern vergleichbare Ergebnisse bei mittelschweren Formen. Bei
den eher schweren Formen der AD war die einmal tägliche Anwendung weniger
wirksam.
Im Vergleich zu einer topischen Standardtherapie mit Kortikosteroiden zeigte die Tacrolimus-Salbe 0,1 % in Kurzzeitstudien über drei Wochen ein vergleichbares Potential zu Hydrocortisonbutyrat 0,1 %, einem mittelstark wirksamen Kortikosteroid (5). Tacrolimus-Salbe 0,03 % war dem Hydrocortisonacetat 1 %, einem schwach wirksamen Kortikosteroid überlegen (6). In einer Studie über sechs Monate, bei der die Studienmedikation intermittierend bei Bedarf angewendet wurde, zeigte sich Tacrolimus-Salbe 0,1 % der Therapie mit Kortikosteroiden signifikant überlegen (Hydrocortisonacetat 1 % für Gesicht und Hals, Hydrocrotisonbutyrat 0,1 % für den restlichen Körper).
Bei allen Studien war die systemische Exposition gering, und es konnten keine klinischen Zeichen einer systemischen Immunsuppression nachgewiesen werden (7). Eine häufige unerwünschte Arzneiwirkung besteht in einem initialen Brennen an der Applikationsstelle, das bei etwa 50 % der erwachsenen Patienten beobachtet werden kann. Bei Kindern ist dieser Anteil geringer. Gelegentlich kommt es auch zu einer Verstärkung des Juckreizes. Diese Nebenwirkungen sind nur in den ersten Behandlungstagen zu beobachten. Im Vergleich mit der Placebogruppe konnte keine erhöhte Rate an Infektionen verzeichnet werden (8). Bei vergleichenden Studien gab es einen leichten Anstieg bei Infektionen mit Herpes simplex während der ersten Behandlungswoche. Bei längeren Behandlungsperioden war dieser Unterschied zwischen den Behandlungsgruppen nicht mehr nachweisbar. Im Gegensatz zu Kortikosteroiden konnte eine Atrophie der Haut nicht nachgewiesen werden. Bei vorgeschädigter Haut, bei der es durch Anwendung von Kortikosteroiden zu einer Verdünnung gekommen war, wurde eine allmähliche Normalisierung der Hautdicke unter Behandlung mit Tacrolimus-Salbe nachgewiesen.
Für die Pimecrolimus-Creme konnte in einer europäischen Dosisfindungsstudie (Maximaldosis 1,0 %) für die 0,6%ige und 1,0%ige Formulierung eine Wirksamkeit nachgewiesen werden. Niedrigere Formulierungen waren weniger wirksam. In dieser Studie waren alle getesteten Konzentrationen der Pimecrolimus-Creme weniger wirksam als das Betamethason-17-valerat 0,1 % (9).
Für die weitere Entwicklung wurde Pimecrolimus-Creme 1 % ausgewählt. In einer 12-monatigen Vergleichsstudie war Pimecrolimus-Creme weniger wirksam verglichen mit Triamcinolon Acetonid 0,1 %, einem mittelstarken Kortikosteroid (10). Etwa 60 % der Patienten aus der Pimecrolimusgruppe brachen die Studie vorzeitig ab, vor allem aufgrund mangelnder Wirksamkeit. Studienabbrecher waren daher hauptsächlich Patienten mit mittelschwerer und schwerer Form der AD. In nachfolgenden Studien wurde Pimecrolimus-Creme mit einer so genannten Standardtherapie verglichen, die aus einer Basispflege und Kortikosteroiden für einen Schub der Erkrankung bestand. In diesen Studien war Pimecrolimus wirksamer als eine Behandlung mit dem Vehikel allein (11-13). Eingeschlossene Patienten hatten milde bis mittelschwere Form der AD, bei etwa 25 % der Patienten war eine Behandlung ausschließlich mit dem Vehikel hinreichend. Kinder- und Erwachsenenstudien zeigten vergleichbare Ergebnisse: Pimecrolimus kann als Kortikosteroid einsparende Behandlung bei leichter bis mittelschwerer AD eingesetzt werden. Pimecrolimus-Creme ist daher in den USA und in Europa nur für die leichte bis mittelschwere AD zugelassen worden.
Das Profil der unerwünschten Arzneimittelwirkungen der Pimecrolimus-Creme ist vergleichbar der Tacrolimus-Salbe. Das initiale Brennen scheint bei der Pimecrolimus-Creme weniger häufig zu sein. Eine systemische Exposition war in den Studien mit Pimecrolimus-Creme durchgängig niedrig.
Auch wenn ein direkter Vergleich zwischen Tacrolimus-Salbe und Pimecrolimus-Creme noch nicht vorliegt, so ist eine höhere Wirksamkeit der Tacrolimus-Salbe unbestritten. Dies zeigt sich in den Ergebnissen der oben erwähnten Studien. Tacrolimus-Salbe kann als Monotherapie auch bei schwereren Formen der AD erfolgreich eingesetzt werden. Pimecrolimus-Creme dagegen ist nur bei leichten Formen der AD als Monotherapie einsetzbar. Grundsätzlich sollte die Monotherapie einer Kombinationstherapie von TIM und Kortikosteroiden vorgezogen werden, da langfristige Ergebnisse mit einer Monotherapie überlegen sind. Zusammenfassend können TIM topische Kortikosteroide als Behandlung der ersten Wahl herausfordern.
Literaturnachweis:
(1) Ruzicka
T. et al.
A short-term trial of tacrolimus ointment for atopic dermatitis.
N Engl J Med 337, 816-21,1997
(2) Boguniewicz M. et al.
A randomized,
vehicle-controlled trial of tacrolimus ointmenty for the treatment of atopic dermatitis
in children.
J Allergy Clin Immunol 102, 637-44, 1998
(3) Hanifin J.M.
et al.
Tacrolimus ointment in the treatment of atopic dermatitis in adult
patients: part I, efficacy.
J Am Acad Dermatol 44, 28-38, 2001
(4) Paller
A. et al.
A 12-week study of tacrolimus ointment for the treatment of atopic
dermatituis in pediatric patients.
J Am Acad Dermatol 44, 47-57, 2001
(5) Reitamo S. et al.
Efficacy and safety of tacrolimus ointment compared
with that of hydrocortisone butyrate ointment in adult patients with atopic dermatitis.
J Allergy Clin Immunol 109, 547-55, 2002
(6) Reitamo S. et al.
Efficacy
and safety of tacrolimus ointment compared with that of hydrocortisone acetate
ointment in children with atopic dermatitis.
J Allergy Clin Immunol 109,
539-46, 2002
(7) Reitamo S. et al.
Safety and efficacy of 1 year of tacrolimus
ointment monotherapy in adults with atopic dermatitis.
Arch Dermatol 136,
999-1006, 2000
| |



Mögliche
zukünftige Indikationen von topischen Immunmodulatoren (TIM)
Hautklinik der Heinrich-Heine-Universität, Düsseldorf
Für die neuen topischen Immunmodulatoren (TIM) Tacrolimus-Salbe
(Protopic 0,03 % und 0,1 %) und Pimecrolimus-Creme (Elidel 1 %) besteht derzeit
eine Zulassung für die Therapie der mittelschweren bis schweren beziehungsweise
der leichten bis mittelschweren Form der Atopischen Dermatitis bei Erwachsenen
und Kindern. In mehreren multizentrischen Studien konnten die Effektivität
und die Sicherheit dieser Medikamente für Kurzzeit- und intermittierende
Langzeitbehandlung demonstriert werden. Über Bindung der TIM an zytosolische
Rezeptoren kommt es zu einer Blockade Ca2+ abhängiger Phosphatasen, was zu
einer Inhibition der Genexpression zahlreicher proinflammatorischer Zytokine (unter
anderem IL -2, IL-3, IL-4, IL-5, IFN- , GM-CSF, TNF- ) führt.
Aus diesem Grund scheinen die TIM auch bei einer Reihe anderer Lymphozyten vermittelter Dermatosen eine therapeutische Alternative darzustellen, wie neuere klinische Untersuchungen zeigen konnten.
In Pilotstudien und
kleineren klinischen Untersuchungen konnte anhand von kleineren Patientenzahlen
die Wirksamkeit von Tacrolimus-Salbe auch bei der Behandlung anderer inflammatorischer
Hauterkrankungen demonstriert werden:
Psoriasis vulgaris (insbesondere inverser
Formen), erosiver Lichen ruber mucosae, seborrhoische Dermatitis, Lichen sclerosus
et atrophicus der Vulva, chronisch-aktinische Dermatitis, Periorale Dermatitis
/ Steroid induzierte Rosazea, Vitiligo, chronisch-diskoider Lupus erythematodes,
Pyoderma gangraenosum, Ulcus cruris bei rheumatoider Arthritis, Acrodermatitis
continua suppurativa, chronische GvHD.
Für die neuere Pimecrolimus-Creme konnten erste klinische Untersuchungen positive Effekte unter anderem bei der Behandlung der Psoriasis unter okklusiven Bedingungen, der seborrhoischen Dermatitis und der Kontaktdermatitis zeigen.
Im Allgemeinen gelten T-Zell vermittelte Dermatosen, welche unter anderem auch auf systemische Gabe von Cyclosporin ansprechen, als mögliche Zielerkrankungen. In der Zukunft werden systematische und kontrollierte Studien erforderlich sein, die die Effektivität und Sicherheit von Tacrolimus-Salbe beziehungsweise Pimecrolimus-Creme bei anderen inflammatorischen Dermatosen untersuchen. Vielversprechende Beobachtungen bei verschiedenen entzündlichen Dermatosen gibt es derzeit vor allem für die Tacrolimus-Salbe.
| |

Schlusswort
zum Workshop*
Topische Immunmodulatoren (TIMs): Etablierte und zukünftige
Indikationen
Hautklinik der Heinrich-Heine-Universität,
Düsseldorf
*Veranstalter: Fujisawa Deutschland
GmbH, München
Mit der Einführung der TIM wurde eine neue Ära in der Therapie der AD eingeleitet. Bislang gibt es zwei Vertreter, die mit identischem Wirkmechanismus ihre Wirksamkeit und Sicherheit in ausführlichen Studien unter Beweis gestellt haben.
Tacrolimus-Salbe hat in zahlreichen Studien mit insgesamt über 16.000 Patienten seine Wirksamkeit als Monotherapie auch für schwere Fälle der Neurodermitis eindrücklich unter Beweis gestellt.
Pimecrolimus-Creme ist ein ebenfalls sehr sicheres Präparat, und seine Wirksamkeit bei leichten und mittelschweren Neurodermitisformen auch in Kombination mit Kortikosteroiden in Studien gut untersucht.
Beide Präparate sind ab dem zweiten Lebensjahr für die Therapie der Neurodermitis zugelassen. Aufgrund des hervorragenden Sicherheitsprofils gibt es keine Einschränkungen in der Behandlungsdauer oder der maximal behandelten Fläche.
Somit ist es erstmals möglich, eine wirksame, sichere und langfristig anwendbare topische Therapie durchzuführen.
Eine Hoffnung für die Zukunft ist eine langfristige Modulation des Krankheitsverlaufes der AD durch TIM.
| |

Wirkmechanismen der Topischen Immunmodulatoren (TIM)
Klinik
und Poliklinik für Dermatologie der Rheinischen Friedrich-Wilhelms-Universität,
Bonn
Ähnlich wie Cyclosporin, binden die
TIM (Pimecrolimus und Tacrolimus) an intrazelluläre Rezeptorstrukturen, die
so genannten Makrophiline oder FKBP (für FK-binding proteins), und unterscheiden
sich hiermit pharmakologisch grundsätzlich von Glukokortikosteroiden. Diese
Makrophiline, deren natürliche Liganden noch nicht identifiziert wurden,
sind ubiquitär exprimiert. Unter den bislang acht bekannten FKBPs binden
die TIM das so genannte FKBP12 und das FKBP12.6 mit der höchsten Affinität.
FKBP12-TIM-Komplexe hemmen die Aktivität von Calcineurin und damit die Aktivierung
(Dephosphorylierung) und nukleäre Translokation des Transkriptionsfaktors
für Zytokingene NFAT. Als Folge wird unter anderem eine Inhibition der IL-2-Synthese
durch T-Zellen, aber auch der Produktion anderer proinflammatorischer Zytokine
bewirkt. Es wurde darüber berichtet, dass zumindest Tacrolimus auch an den
TGF-ß- Rezeptor Typ 1 bindet beziehungsweise seine Aktivierung hemmt. Ob
Pimecrolimus ähnliche Aktivitäten aufweist, bleibt zunächst unklar.
Aufgrund der ubiquitären Expression von FKBP12 sollten die TIM
– zumindest theoretisch – alle Zellen pharmakologisch beeinflussen können,
vor allem auch die Zellen, die in der Haut an der Entzündungsreaktion beteiligt
sind. In der Tat konnte gezeigt werden, dass Tacrolimus neben T-Zellen auch auf
Keratinozyten, Mastzellen, Endothelzellen sowie Antigen präsentierende Zellen
wirkt. Somit können sowohl residente Zellen der Haut als auch eingewanderte
Entzündungszellen von TIM in ihrer Funktion beeinflusst werden. Unklar bleibt
hier noch eine rationale Erklärung, warum Pimecrolimus nur auf T-Zellen und
nicht auf Langerhans-Zellen (LZ) in der Haut wirken soll. Neben der um einen Log
niedrigeren Affinität von Pimecrolimus für FKBP12 könnte unter
anderem auch eine Variation der Expression der FKBPs in Abhängigkeit des
Zelltyps hierfür eine Erklärung sein. Dies ist für kutane Antigen
präsentierende Zellen wie die LZ und die inflammatorischen dendritischen
epidermalen Zellen (IDEC) von Bedeutung, da diese Zellen maßgeblich für
die Auslösung und den Erhalt der atopischen Entzündungsreaktion verantwortlich
gemacht wurden. Laufende Untersuchungen mittels Genchip-Technologie sollen in
näherer Zukunft wichtige ergänzende Informationen über die Wirkungsmechanismen
der TIM auf LZ und IDEC liefern. Während in der läsionalen Haut der
AD beim Menschen LZ nur wenig durch Tacrolimus beeinflusst werden, scheinen die
IDECs ein wichtiges Ziel dieses Moleküls zu sein. Ob Pimecrolimus ein ähnliches
Wirkungsprofil zeigt, muss noch untersucht werden. Bislang liegen im Wesentlichen
nur Ergebnisse aus Tiermodellen vor, in denen dendritische Zellen nicht beeinträchtigt
sein sollen.
Zahlreiche klinische Studien mit den TIM haben gezeigt, dass, wie bei anderen
Medikationen auch, hier einige Individuen auf diese Therapie nicht gut ansprechen.
Die immunpharmakologischen Hintergründe dieser so genannten „non-responder“
sind noch unklar. Zukünftige Untersuchungen über mögliche Variationen
(so genannte single nucleotide polymorphisms; SNPs) der Gene, die für Makrophiline
und/oder Calmodulin und Calneurin kodieren, könnten hier in Verbindung mit
pharmakogenomischen Ansätzen wichtige Erklärungen anbieten.
| |



