Abstracts 2001
Peter Elsner
Aktuelle Aspekte
der Europäischen Kosmetik-Gesetzgebung
Klinik für Dermatologie und Allergologie, Friedrich-Schiller-Universität Jena
Da der Handel von Kosmetika zwischen den Mitgliedsstaaten der
Europäischen Union dem Gemeinschaftsrecht unterliegt, wird die Kosmetikgesetzgebung
wesentlich von der EU bestimmt. Das 6. Amendment (Council Directive 93/35 EEC)
der europäischen Kosmetikdirektive 76/768 EEC ist die derzeit gültige
Basis der Kosmetikgesetzgebung in Europa. Die Mitgliedsstaaten haben das europäische
Recht in ihr nationales Recht umzusetzen.
Diese Ergänzung brachte
einige wesentliche Fortschritte im Sinne des Verbraucherschutzes und der für
ihre Verbraucher und Patienten engagierten Dermatologen. So wurde eine Kennzeichnungspflicht
für die Bestandteile von Kosmetika eingeführt, eine obligatorische Sicherheitsbewertung
gesetzlich verankert und erstmals der Begriff der „Wirksamkeit“ von
Kosmetika verwendet. Nach dem gültigen Recht müssen Unternehmen, die
Kosmetika auf den Markt bringen, ein Produktdossier vorhalten, das die Sicherheitsbewertung
und die Daten enthält, die behauptete Wirkungen belegen. Damit ist der Wirksamkeitsnachweis
zur gesetzlichen Pflicht geworden.
Ein wesentlicher Schwerpunkt des
Amendments war die Verpflichtung zum Ersatz von Tierversuchen in der Sicherheitsbewertung,
soweit validierte Alternativen vorliegen. Dies ist bisher allerdings nur in beschränktem
Umfang der Fall (Phototoxizität und Korrosion). Während die Direktive
nicht explizit zur Kosmetiktestung am Menschen Stellung nimmt, hat das Scientific
Committee for Cosmetics and Non-Food Products (SCCNFP), das die Kommission berät,
in einer Reihe von Opinions Stellungnahmen zu Sicherheitstestungen am Menschen
abgegeben; danach werden hohe Maßstäbe bezüglich der Qualifikation
der Untersucher, der Qualität der Studien (Good Clinical Practice) und der
ethischen Überprüfung gesetzt.
Literatur:
1.
Elsner P, Merk H, Maibach Hi (eds.) (1999) Cosmetics: Controlled efficacy studies
and regulation. Springer, Heidelberg, Berlin, New York
2. Elsner P, Maibach
Hi (eds.) (2000) Cosmeceuticals. Marcel Dekker, New York




Anton Stütz
Ascomycine:
Eine neue antiinflammatorische Substanzklasse
Novartis Forschungsinstitut Wien
Ascomycin ist ein immunmodulierender macrocyclischer Naturstoff, der erstmals
aus Streptomyces hygroscopicus var. ascomyceticus isoliert wurde. Ascomycin
bindet an Macrophilin-12, inhibiert Calcineurin und hemmt die Aktivierung von
T-Zellen sowie die Synthese und Freisetzung von inflammatorischen Cytokinen.
Am Novartis Forschungsinstitut Wien wurde erstmals die topische antiinflammatorische
Wirksamkeit dieser und anderer Macrophilin-Liganden in Modellen der allergischen
Kontaktdermatitis gefunden. Mehr als 400 Derivate der strukturell hochkomplexen
Ascomycin-Macrolactame wurden synthetisiert, biologisch charakterisiert und
Struktur-Wirkungs-Beziehungen unterzogen. SDZ-ASM-981 wurde als Entwicklungssubstanz
ausgewählt, weil sie hautspezifisches pharmakologisches Wirkungsprofil
aufweist: Sie ist in vivo sowohl nach topischer als auch nach oraler Gabe in
Hautentzündungsmodellen hochwirksam, zeigt aber im Gegensatz zu Cyclosporin
A oder FK 506 nur ein geringes Potential in Modellen der systemischen Immunsuppression.
In Multizenterstudien an Patienten mit atopischer Dermatitis wurde bewiesen,
dass SDZ-ASM-981-Creme hochwirksam und außerordentlich gut verträglich
ist, ohne die Nebenwirkungen der Kortikosteroide wie z.B. Hautatrophie. Selbst
bei einer Behandlung von bis zu 90% der Körperoberfläche der Patienten
oder von Kleinkindern ab drei Monaten konnten keine oder nur sehr niedrige Blutspiegel
gemessen werden. Die Ergebnisse der Studien an mehr als 2000 Patienten bestätigen,
daß SDZ-ASM-981-Creme zur Langzeitbehandlung bei Kindern und Erwachsenen
geeignet ist und therapeutische Vorteile gegenüber Standardbehandlungen
besitzt. Die klinische Wirksamkeit wurde auch an Patienten mit allergischer
Kontaktdermatitis und chronischer Handdermatitis nachgewiesen.
SDZ-ASM-981 wurde oral erstmals an Patienten mit mittelschwerer bis schwerer
chronischer Plaque-Psoriasis getestet. Dabei wurde im Verlauf der vierwöchigen
Studie bei einer Dosierung von 40 und 60 mg/Tag eine beeindruckende klinische
Verbesserung [PASI-Reduktion 60% (40 mg) und 75% (60 mg)] erzielt, ohne dass
Nebenwirkungen beobachtet wurden. Diese Resultate legen nahe, dass das in Tiermodellen
etablierte hautspezifische pharmakologische Profil auf den Menschen übertragbar
ist und dass SDZ ASM 981 ein vielversprechendes antiinflammatorisches Potential
auch zur oralen Behandlung entzündlicher Hauterkrankungen wie Psoriasis
und atopischer Dermatitis besitzt. Zur Zeit wird orales SDZ ASM 981 in Phase
II in Multizenterstudien geprüft.
Literatur
1. Meingassner JG, Stuetz A, J. Invest. Dermatol. 98, 851-855 (1992)
2. Meingassner JG, Grassberger M, Fahrngruber H et al., Brit. J. Dermatol. 137,
568-576 (1997)
3. Van Leent EJM, Graeber M, Thurston M et al., Arch. Dermatol. 134, 805-9 (1998)
4. Grassberger M, Baumruker T, Enz A et al., Brit. J. Dermatol. 141, 264-73
(1999)
5. Neckermann G, Bavandi A, Meingassner J, Brit. J. Dermatol.142, 669-79 (2000)
6. Paul C, Graeber M, Stuetz A, Exp. Opin. Invest. Drugs 9, 69-77 (2000)
7. Rappersberger K, Komar M, Ebelin ME et al., J. Invest. Dermatol., 114, 776
(2000)


Frank Rippke
Beschleunigung
der epidermalen Regeneration: Dexpanthenol-Effekte in einem reproduzierbaren In-vivo-Modell
Beierdorf
AG, Hamburg
Sowohl zur Behandlung oberflächlicher Hautläsionen
als auch zur Regeneration der epidermalen Barriere bei empfindlicher Haut werden
vielfach Externa mit 5% Dexpanthenol eingesetzt. Den guten klinischen Erfahrungen
steht eine begrenzte Zahl kontrollierter klinischer Studien an menschlicher Haut
gegenüber. In früheren Untersuchungen wurde bereits eine Reihe von Hautpflegepräparaten,
die 3% Dexpanthenol als Wirkstoff enthalten, im humanen epidermalen Saugblasen-Modell
untersucht. Bei dieser Methodik werden durch Unterdruck (0,4 bar) standardisierte,
streng intra-epidermale Hautdefekte (Ø 6 mm) induziert und anschließend
über einen Zeitraum von fünf Tagen die Prüfprodukte oder physiologische
Kochsalzlösung als Kontrolle okklusiv mit Duhringkammern appliziert. Alle
24 Stunden erfolgt eine Bestimmung des transepidermalen Wasserverlustes (TEWL)
als Maß der Barrierefunktion.
In der vorliegenden Studie wurde
eine kosmetische W/O-Emulsion mit 5% Dexpanthenol (pH5 Eucerin® Hand Intensiv
Pflege) an 20 Probanden in doppelblinder, randomisierter und Vehikel-kontrollierter
Versuchsanordnung geprüft. Es zeigte sich sowohl gegenüber der Kontrolllösung
als auch der Grundlage ein signifikanter epithelisierungsfördernder Effekt
der wirkstoffhaltigen Formulierung. Insbesondere in der frühen Phase kam
es im Vergleich zur Grundlage jeweils zu einer deutlichen Beschleunigung der epidermalen
Regeneration.
Mit den dargestellten Untersuchungen konnten sowohl die
Wirksamkeit von Dexpanthenol in entsprechender galenischer Formulierung als auch
die Eignung und Validität der eingesetzten Methodik belegt werden.




Theo Rufli
Biochirurgie
chronischer Wundenl
Dermatologische Universitätsklinik,
Kantonspital Basel
Chronische Wunden sind in der Dermatologie
als Ulcera cruris bei vaskulär bedingten Durchblutungsstörungen und
zahlreichen anderen, selteneren Ursachen zu beobachten. Chronische Wunden zeigen
praktisch keine Heilungstendenz mehr, der Wundgrund ist nekrotisch belegt, Granulationsgewebebildung
fehlt, die Wundränder sind verdickt und aufgeworfen, epitheliale Proliferation
wird vermisst. Am Beginn der lokalen Behandlung steht das Débridement,
die Entfernung nekrotischer und infizierter Gewebeteile. Das Débridement
hat selektiv zu erfolgen. Zur Verfügung stehen die chirurgische Abtragung
in Anaesthesie, z.B. unter Emla® mit der Curette. Enzymatisch wirksame Präparationen
haben nur geringfügige Wirkung.
Dokumente aus Zeiten der napoleonischen
Feldzüge und des ersten Weltkrieges berichten, dass mit Fliegenlarven befallene,
auch grossflächige Wunden keine Infektionen aufwiesen und wider Erwarten
rasch und komplikationslos heilten. Dies veranlasste den amerikanischen Orthopaeden
Baer nach 1920 zur wissenschaftlichen Entwicklung der Biochirurgie (Larventherapie),
einer kontrollierten Nachahmung der Wundmyiasis. Die Larven bestimmter Fliegenarten,
meist Lucilia sericata (Gattung Goldfliegen der Familie Calliphoridae, Schmeissfliegen)
werden im Laboratorium unter sterilen Bedingungen gezüchtet und im Alter
von 2 bis 3 Tagen nach bestandener Sterilitätskontrolle auf die zu reinigenden
Wunden gebracht. Sie werden dort während 3 bis 4 Tagen belassen. Eine Wiederholung
der Prozedur ist jederzeit möglich. Das nekrotische Material wird durch die
Speichelenzyme, Proteasen mit starker Kollagenase-Aktivität, präoral
vorverdaut und dann aufgenommen. Die bakterielle Besiedelung wird sowohl durch
die Ausscheidung von bakteriziden Peptiden wie auch durch Degradation im Darmlumen
reduziert. Die Ausscheidung von Zytokinen mag einen Teil der messbaren Durchblutungssteigerung
und Ödemreduktion unter Biochirurgie erklären.
Die Methode
ist sicher und sehr effektiv. Nachteile ergeben sich aus der aufwendigen Logistik,
der nicht immer einfach zu erreichenden Sterilität der Fliegenlarven und
der Schmerzhaftigkeit. Die Akzeptanz bei den Patienten ist dennoch erstaunlich
hoch.




Bernard Gabard
unter Mitarbeit von E. Chatelain, E. Bieli und S. Haas
Corneosurfametrie:
Eine einfache Methode für die Erfassung der Irritation von Handreinigungsmitteln
Abteilung Biopharmazie, Spirig Pharma AG, Egerkingen/Schweiz
Eine durch Reinigungs-
oder Spülmittel, Detergenzien, Seifen usw. hervorgerufene Hautirritation
ist eine häufige Problemquelle in der klinischen Dermatologie und in der
Berufsdermatologie. Solche Produkte können zur Austrocknung der Hornschicht
und bei wiederholter Anwendung zur Schädigung und Entzündung der Haut
führen, bekannt als irritative Kontaktdermatitis. Behauptungen wie „mild“
oder „hautschonend“ sind an erster Stelle bei der Produktbeschreibung
zu finden, der primäre Zweck der Anwendung, nämlich die Reinigung, tritt
erst an zweiter Stelle auf. Die Prüfung der Hautverträglichkeit ist
eine Hauptaufgabe der Hersteller von Reingungsprodukten geworden. Eine große
Anzahl von Veröffentlichungen beschäftigt sich mit der klinischen Prüfung
der Verträglichkeit, wobei Fragen wie Verbesserung und Standardisierung der
Methode, Verminderung der Prüfungskosten und Erleichterung der Produktauswahl
behandelt werden. Der Einsatz von Bioengineering-Messmethoden im Vergleich zur
klinischen Auswertung wird ebenfalls evaluiert. Im Allgemeinen ist eine Differenzierung
zwischen den Produkten mit den bisher etablierten Prüfmethoden schwierig,
wenn nicht unmöglich, da wirklich stark irritative Produkte nicht verkauft
werden.
19 verschiedene Syndets und Shampoos, die alle als „mild“,
„hautschonend“ bzw. „für Babies geeignet“ deklariert
wurden, sind geprüft worden. Einerseits kamen etablierte In-vivo-Prüfmethoden
wie der Ellenbeugen-Waschtest und der Seifenkammertest zur Anwendung, andererseits
wurde auch eine neue In-vitro-Methode verwendet, die Corneosurfametrie. Für
die genaue Evaluierung der Hautverträglichkeit wurde ein Irritationsindex
(IOI) vorgeschlagen. Als Standard und Positivkontrolle kam Natriumlaurylsulfat
in Frage. Die Ergebnisse der In-vivo-Prüfungen wurden mit Bioengineering-Messmethoden
wie dem transepidermalen Wasserverlust und der Hautfarbe gewonnen.
Die
Ergebnisse der Corneosurfametrie führten zu einer Klassifizierung der Produkte
in drei Kategorien mit steigender Schädigung der Hornschicht, dem IOI entsprechend.
Keine der In-vivo-Prüfungen war in der Lage, zwischen den Produkten zu unterscheiden.
Die aus den Bioengineering-Messmethoden erhaltene Reihenfolge der Produkte zeigte
eine gute Korrelation mit den entsprechenden IOIs, besonders im Falle des transepidermalen
Wasserverlustes (Barriereschädigung), aber nicht für das irritationsbedingte
Erythem.
Die Corneosurfametrie kann als eine schnelle, einfache und kostensparende
Methode bezeichnet werden, die zu einer relevanten Klassifizierung von Reinigungsprodukten
bezüglich ihrer Hautverträglichkeit verwendet werden kann. Allerdings
haben auch die Ergebnisse der Bioengineering-Messmethoden gezeigt, dass gewisse
Produkte zu Hautreaktionen (z.B. einem Erythem) führen können, die nicht
durch eine In-vitro-Prüfung wie die Corneosurfametrie erfasst werden.
PD Dr. Christian Surber, links, im Gespräch mit Dr. Bernard Gabard
Prof. Dr. Rolf Daniels, links, und Dr. Bernard Gabard
Bernard
Gabard
in cooperation with E. Chatelain, E. Bieli und S. Haas
Corneosurfametry:
a simple method to investigate the mildness
of cleansing products
Department of Biopharmacy, Spirig Pharma Ltd., CH-4622 Egerkingen, Switzerland
Irritant reactions to surfactants, cleansing products, soaps or detergents are common in clinical and occupational dermatology. The repeated use of such products may damage the skin, drying out the Stratum corneum and may cause irritant contact dermatitis. Mildness benefit has become a major claim, even overriding the primary purpose of the products, i.e. the cleansing benefit. Testing for mildness now ranks among the First concerns of the manufacturing industry. A wealth of publications deals with the clinical testing of cutaneous tolerance, trying to improve the methodology, to reduce the costs of testing and to facilitate decision-making. Differences can be assessed by clinical and/or instrumental assessment. However, this may be difficult as commercially available products are generally safe to use and none are harsh in the absolute sense. Fine ranking is difficult, if not impossible.
The mildness of 19 different syndets and shampoos, all claimed to be „mild“
or „suitable for Babies“, was evaluated with two methods in vivo (flex
wash test, soap chamber test) and with a new one in vitro, corneosurfametry. For
this purpose, the calculation of an index of irritation (IOI) was proposed. Na-laurylsulfate
was used as a standard and as a model surfactant in each test. Bioengineering
methods (skin colour, transepidermal water loss TEWL) were used throughout.
The results of the corneosurfametry allowed us to classify the products in
three categories with increasing aggressiveness toward the horny layer according
to their IOIs. None of the in vivo test was able to discriminate between the different
products. However, TEWL-ranking, but not skin colour ranking from the in vivo
tests showed a good correlation with I0I from the corneosurfametry.
Corneosurfametry emerged as simple, low-cost and fast new technique for ranking different materials according to their mildness. However, the skin bioengineering techniques showed that some products could lead to measurable skin reactions such as erythema. Thus, corneosurfametry should not be used alone, but should be combined with a suitable in vivo test.
PD Dr. Christian Surber, left,
in conversation with Dr. Bernard Gabard
Prof. Dr. Rolf Daniels,
left, and Dr. Bernard Gabard
Â





Wolfgang Gehring
Das Prinzip
der Rückfettung bei Hautreinigungsmitteln
Hautklinik am Klinikum der Stadt Karlsruhe
Hautreinigungsmitteln
werden rückfettende Inhaltsstoffe beigegeben, um die Hautfreundlichkeit zu
verbessern. Am Beispiel verschiedener Waschlösungen, Badeölen, Duschölen
und Duschcremes haben wir vergleichende Untersuchungen durchgeführt und den
Einfluss der unterschiedlichen Hautreinigungsmittel auf die Hornschichtfeuchtigkeit
und den transepidermalen Wasserverlust sowie den rückfettenden Einfluss auf
die Hautoberfläche dokumentiert.
Eine im leicht sauren pH-Bereich
von pH 5,5 eingestellte Waschlösung wurde mit 5 % Cetiol HE und Isopropylpalmitat
(IPP) als rückfettende Substanzen untersucht. Wählt man die gebrauchsfertige
Verdünnung der Waschlösungen so, dass gleiche Reinigungskraft gegeben
ist, zeigt sich, dass der austrocknende und irritierende Effekt des Waschvorganges
durch keine der beiden rückfettenden Substanzen vermindert wurde. Durch den
Zusatz von Cetiol HE war eher noch ein gesteigertes irritatives Potential erkennbar.
Eine rückfettende Nutzwirkung war nicht feststellbar.
Bei emulgierenden
Badeölen fanden wir vergleichbare Ergebnisse und konnten belegen, dass der
Waschvorgang zu einem Verlust an Hornschichtfeuchtigkeit und einem Anstieg des
transepidermalen Wasserverlustes führt. Anders verhielt sich nur ein spreitendes
Ölbad auf Mandelölbasis.
Duschöle sind in ihrem Verhalten
ähnlich wie emulgierende Badeöle. Auch hier konnten wir einen austrocknenden
Einfluss und einen Anstieg des transepidermalen Wasserverlustes dokumentieren,
der allerdings durch die Formulierung beeinflusst und minimiert werden kann. Eine
wirkliche Rückfettung ließ sich jedoch nicht belegen.
Duschcremes
können dem gewöhnlichen galenischen Aufbau entsprechen und nur einen
geringen Ölanteil und konditionierende Zusätze enthalten, die auf der
Haut ein cremiges Gefühl vermitteln. Wir haben uns mit Duschcremes beschäftigt,
die einen Ölanteil von bis zu 50 % vorwiesen und durch geeignete Tensidkörper
homogenisiert waren, so dass die optischen Eigenschaften einer Creme mit den Anforderungen
an ein Reinigungsmittel und an eine pflegende Emulsion kombiniert sein sollten.
Ein Prüfpräparat mit einem Erdnussölanteil von 50 % und einem Tensidgehalt
von 15 % Cocoamphodiacetat hat sich als besonders vorteilhaft dargestellt. Der
Waschvorgang hat nur zu einem minimalen Verlust an Hornschichtfeuchtigkeit und
nur zu einem geringen Anstieg des TEWL geführt. Der entfettende Einfluss
durch den Waschvorgang konnte vollständig verhindert werden.
Das
Prinzip der Rückfettung durch Hautreinigungsmittel ist schwierig. Postuliert
man eine ausreichende Wasch- und Reinigungswirkung durch das Hautreinigungsmittel,
ist ein Tensidüberschuss erforderlich, der zum Verlust an Hornschichtfeuchtigkeit
und Anstieg des TEWL führt. Allerdings kann dieser Effekt durch die Formulierung
des Produktes gesteuert werden. Eine deutliche Abgrenzung fanden wir nur bei einer
Duschcreme mit einem Ölanteil von 50 % und einem Tensidgehalt von 15 %. Der
Verlust an Hornschichtfeuchtigkeit und der irritierende Einfluss waren minimiert.
Die Entfettung der Hautoberfläche konnte vollständig verhindert werden.
Prof.
Dr. med. Wolfgang Gehring




Thomas Ruzicka
in cooperation
with H.F. Abts and G. Michel
Genomic
analysis of drug effects
Hautklinik der Heinrich-Heine-Universität,
Düsseldorf
While the completion of the human genome sequence in reliable quality is in sight, the ordering of the scattered sequences and moreover, identification of the genes within will still take some time. But even then the important question will be which of the genes from the whole transcriptome are involved in particular pathophysiological and pharmacological events. To identify candidates for these relevant genes academic biomedical research as well as biotechnology and pharmaceutical industries are forced to integrate differential gene expression profiling into their basic research, drug discovery and development strategies.
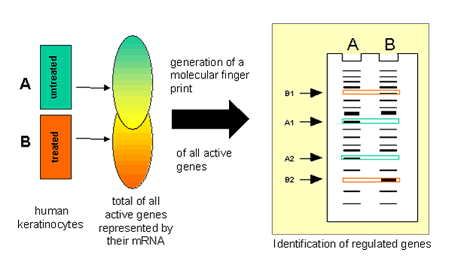
Expression profiling using mRNA differential-display (DD) offers the opportunity to identify differentially expressed genes genome-wide with high sensitivity. Since the identification is based solely on differences in mRNA abundance between the compared cell populations no sequence information of the target genes is necessary. Therefore this allows also the analysis of so far unidentified genes.
The usefulness of the approach has been demonstrated during the analysis of UV-regulated genes in human epidermal keratinocytes. Since induced and repressed genes can be detected simultaneously we were able to identify a formerly unrecognized large set of UV-repressed genes. One of these unknown sequences has been completely cloned and identified as new serine proteinase inhibitor (serpin). Serpins have not yet been connected to the UV-response. This finding emphasizes that genome-wide expression profiling by differential display does not restrict the analysis to a particular set of genes, selected based on the actual knowledge in a particular field. This advantage might also be essential when the pharmacological modes of action should be dissected. The genes which are regulated in a cell by a pharmacological substance form the molecular basis of the desired curative effect as well as the unwanted site effects. The knowledge of these genes will allow to elucidate the mechanisms underlying both actions.
By a restricted differential display PCR analysis several genes which are regulated in human keratinocytes by antihistaminic substances have been identified. The majority of the isolated sequences have been so far only described as ESTs or anonymous sequence information from the human genome project. Although this documents the enormous increase in sequence data in the databases due to the human genome project, there were still completely new sequences identified. Among the known sequences the cytoplasmic protein a-catenin was identified. This protein plays a crucial role in E-cadherin mediated cell-cell adhesion by binding E-cadherin to the cytoskeleton via beta-catenin or gamma-catenin and actin. These results implicate that antihistaminica may influence epithelial integrity by modulating the expression of relevant genes like the catenins.
In
summary expression profiling will identify not only new targets for future drug
development but also allow the identification of the molecular basis of drug action
and unwanted side effects. This information will help to optimize current drugs
and to individualize therapy based on pharmacogenomic analysis.




Karl-Heinz Nietsch
Hauttoxikologische
Bewertung unterschiedlicher mittelstarker topischer Glukokortikoide mittels hochfrequentem
Ultraschall
Aventis
Pharma Deutschland GmbH, Bad Soden
Zu den in der Dermatologie
am häufigsten eingesetzten Therapeutika gehören topisch angewandte Glukokortikosteroide.
Im Fall einer längerfristigen Behandlung, wie sie bei chronisch-entzündlichen
Dermatosen unvermeidbar ist, muss das unterschiedliche atrophogene Potential verschiedener
Kortikosteroide berücksichtigt werden. Erfahrungen mit konventionellen halogenierten
Kortikosteroiden zeigen, dass eine starke antientzündliche Wirkung mit einer
starken antiproliferativen Potenz gekoppelt ist. Der Wunsch, erwünschte und
unerwünschte Steroidwirkungen zu trennen, führte zur Entwicklung neuer,
halogenfreier Kortikosteroide, dessen erster Vertreter das doppelt-veresterte
Prednicarbat ist.
Um das Risiko der atrophogenen Potenz eines Kortikosteroids
für die klinische Praxis abschätzen zu können, bietet sich als
brauchbarer Parameter die direkte Messung der Hautdicke an. Objektivierbare Ergebnisse
liefert die Hautdickenmessung mittels Ultraschall. In verschiedenen Studien wurde
für Prednicarbat nach offener Anwendung über 6 Wochen ein geringeres
atrophogenes Potenzial als für halogenierte Steroide vergleichbarer Wirkstärke
nachgewiesen (Dykes et al. 1987, Korting et al. 1992, Schäfer-Korting et
al. 1993). Für das zuletzt auf dem Markt erschienene halogenierte Mometason
lagen bisher noch keine vergleichenden Daten vor. Eine Einordnung dieser Substanz
sollte deshalb in einer vergleichenden Studie vorgenommen werden.
In
einer doppelblinden, randomisierten, intraindividuellen Studie wurden 24 Probanden
unter standardisierten Bedingungen mit Prednicarbat 0,25% Salbe, Betamethason-17-valerat
0,1 % Salbe und Mometasonfuroat 0,1% Salbe über eine Zeitraum von 6 Wochen
2 x täglich in vormarkierten Feldern der Armbeuge behandelt. Die Veränderung
der Hautdicke wurde mittels eines Hautsonographen (DUB 20S/DUB 50S) ermittelt.
Kontrolluntersuchungen wurden in wöchentlichem Abstand durchgeführt.
Parallel hierzu erfolgte eine visuelle Beurteilung hinsichtlich des Auftretens
von Atrophiezeichen nach einem 5-Punkte-Score. Ergebnisse: Die Sonographie zeigte
bei der als Kontrolle mitlaufenden Salbengrundlage von Prednicarbat praktisch
keine Veränderung der Hautdicke (1%). Die prozentuale Abnahme der Hautdicke
war in den mit Prednicarbat 0,25% Salbe behandelten Testfeldern geringer als in
den mit den Vergleichssubstanzen behandelten Feldern. Die maximale Abnahme der
Hautdicke wurde am Tag 36 für alle drei Testsubstanzen erreicht (Prednicarbat
13%, Mometason 17%, Betamethason 24%). Der Vergleich zwischen Prednicarbat und
den anderen Kortikosteroiden zeigte einen hochsignifikanten Unterschied mit dünnerer
Haut in den mit Mometason ( p= 0,0061) sowie Betamethason (p< 0,0001) behandelten
Feldern (Abbildung). Keine Zeichen von Atrophien oder Teleangiektasien wurden
in den mit Prednicarbat oder dem Vehikel behandelten Feldern beobachtet. Anzeichen
von Atrophie (Score 1) wurden bei zwei Probanden in den mit Mometason und Betamethason
behandelten Feldern gesehen. Für Mometason wurden Teleangieektasien (Score
1) bei zwei Probanden an Tag 22 und an Tag 29 festgestellt. Ebenso konnten bei
Betamethason Anzeichen von Teleangieektasien bei zwei Probanden an den Prüftagen
29 und 36 beobachtet werden.
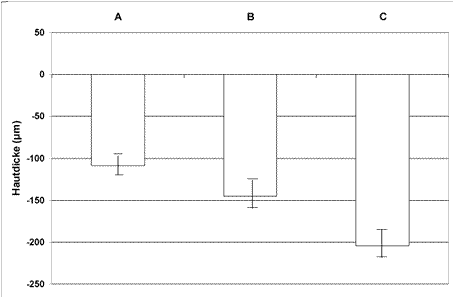
Abbildung
Abnahme der Hautdicke (Mittelwert ±
Standardabweichung) nach 6wöchiger, offener Anwendung von (A) Prednicarbat
0,25% Salbe, (B) Mometasonfuroat 0,1% Salbe und Betametason-17-valerat 0,1 % Salbe
Literatur
1.
Dykes, P. J., Hill, S., and Marks, R. (1988): Assessment of the atrophogenicity
potential of corticosteroids by ultrasound and by epidermal biopsy under occlusive
and nonocclusive conditrions; in Topical corticosteroid therapy: a novel approach
to safer drugs, edited by E. Christophers et. Al., Raven Press, Ltd. New York
2. Korting, H.C. et al. (1992): 0.025% prednicarbate cream and the corresponding
vehicle induce less skin atrophy than 0.1% betamethasone-17-valerate cream and
0.05% clobetasol-17-propionate cream; Eur. J. Clin. Pharmacol. 42, 159 – 161
3. Schaefer-Korting, M., Korting, H.C., Kerscher, M. J., and Lenhard, S. (1993):
Prednicarbate activity and benefit/risk ratio to other topical glucocorticoids.;
Clin. Pharmacol. Ther. 54, 448 – 456


Isaak Effendy
Irritation als Wirkprinzip der Behandlung der Altershaut?
Hautklinik der Philipps-Universität Marburg
In letzter Zeit werden immer mehr Externa
zur Hautglättung, Hautverschönerung bzw. Hautverjüngung der Altershaut
angeboten. Es handelt sich dabei vor allem um Präparate mit Vitamin A-Säure
oder Fruchtsäuren, deren irritative Wirkung auf die Haut wohl bekannt ist.
Die Vermutung liegt nahe, dass Irritanzien durchaus eine oberflächliche
„Hautablation“ induzieren können. Dies könnte möglicherweise
für die Bildung der „neuen“ Haut (Hautverjüngung) verantwortlich
sein. Daher ist es interessant zu untersuchen, ob andere Substanzen mit bekanntem
Irritationspotential auch ähnliche Hautveränderungen zustande bringen
können.
Eigene Untersuchungen weisen in der Tat darauf hin, dass
Natriumlaurylsulfat (Detergens) und Calcipotriol (Vitamin D-Analogon) durchaus
vergleichbare biophysikalische Hautveränderungen verursachen können:
Erhöhung des TEWL, Reduzierung der Hauthydratation sowie vor allem eine Zunahme
der Proliferationsrate der Epidermiszellen. Man darf darauf gespannt sein, ob
die Anwendung dieser und ähnlicher Stoffe auch eine klinische Besserung der
Altershaut herbeiführen kann.
Isaak Effendy
Are
Irritants Cosmetically Usefull ?
Department of Dermatology, Philipps-University Marburg, Germany
Recently, a number of topical agents (perhaps better: cosmeceuticals) are available for treating of photoaged skin or for skin rejuvination. The active agents provide particularly vitamin A and fruit acids with their known irritant potential.
lt is therefore intriguing to determine whether or not other irritant substances may induce comparable skin changes compared to the established cosmeceuticals. Experimental studies an volunteers revealed that detergens sodiuml aurylsulfat (SLS) and vitamin D analogue (calcipotriole) as well are able to induce similar changes of epidermal functions as retinoic acid and glycolic acid did. Although it is known that the effects of all?trans?retinoic acid an the skin are mediated by their nuclear receptors (RAR and RXR families), the irritant potential of the other substances may explain the positive effects an the skin. Further studies are requested to determine whether SLS, vitamin D analogues, Tazaratone etc. will also produce a good clinical effect an photoaged skin.





Matthias Augustin
Keratinozyten-Transplantation:
Pharmakoökonomische
Aspekte des Tissue Engineering bei Ulcus cruris
Universitäts-Hautklinik Freiburg/Breisgau
Hintergrund: Chronische Ulcera
sind aus sozioökonomischer Sicht von großer Bedeutung. Insbesondere
Ulcera crurum und Decubital-Ulcera führen in Deutschland zu direkten und
indirekten Kosten von jährlich mehreren Milliarden Mark. Von ebenso großer
Bedeutung sind die negativen Auswirkungen dieser Ulcus-Erkrankungen auf die Lebensqualität
der betroffenen Patienten. Viele der herkömmlichen Behandlungsstrategien
chronischer Ulcera führen nur zu unbefriedigenden Behandlungsverläufen
und schnellen Rezidiven. Aus dermatologischer Sicht von großem Interesse
ist daher die Entwicklung neuer biotechnologischer Behandlungsansätze wie
die In-vitro-Kultivierung und Transplantation von Keratinozyten-Suspensionen autologer
oder allogener Herkunft. Diese Therapieverfahren stellen auch aus pharmakoökonomischer
Sicht interessante Innovationen dar, bei denen allerdings höhere initiale
Kosten mit sekundären zusätzlichen Benefits abgewogen werden müssen.
Fragestellung: Wie ist der wissenschaftliche Kenntnisstand über
Nutzen und Effektivität moderner Tissue Engineering-Verfahren in der Therapie
chronischer Wunden aus pharmakoökonomischer Sicht?
Methoden:
Wissenschaftliche Metaanalyse (Literature Review) unter Berücksichtigung
eigener Studiendaten, darauf basierend pharmakoökonomische Modellbildung
für ausgewählte Therapieverfahren des Ulcus cruris venosum.
Ergebnisse: Nur in wenigen Therapiestudien zu chronischen Wunden wurden
qualifizierte pharmakoökonomische Analysen durchgeführt. Das jährliche
Kostenaufkommen für das Ulcus cruris venosum liegt pro Patient bei konservativer
Therapie zwischen 15.000 bis 30.000 Mark Wichtigste Prädiktoren für
eine kostenintensive Behandlung sind die stationären Krankenhaustage sowie
die Personalkosten für die pflegerische Versorgung des Ulcus. Diese variieren
in Abhängigkeit von der Wahl des Ulcus-Dressings.
Je nach Wirksamkeit
und Rezidivfreiheit liegen die mittleren jährlichen direkten Kosten für
die verschiedenen Verfahren des modernen Bioengineerings zwischen 8.000 und 20.000
Mark Unter verschiedenen Wirksamkeitsmodellen ist die Transplantation kultivierter
autologer Keratinozyten gegenüber konservativen Verfahren dann kosteneffektiver,
wenn die Behandlung ambulant durchgeführt werden kann und die Rezidivfreiheit
diejenige der konservativen Behandlung signifikant übersteigt. Nach eigenen,
präliminären Daten an 42 Patienten ist dies der Fall. Die Literaturdaten
hierzu sind uneinheitlich.
Schlußfolgerung: Aufgrund der
noch zu geringen Datenlage aus kontrollierten Studien kann bislang kein „systematic
review“ zu den pharmakoökonomischen Effekten des Tissue Engineering
bei Ulcus cruris durchgeführt werden. Unter Zusammentragung von eigenen Studiendaten
und ersten Publikationen kann konstatiert werden, dass die Behandlung des Ulcus
cruris mit Keratinozyten-Transplantaten aus pharmakoökonomischer Sicht unter
den derzeitigen Bedingungen des deutschen Vergütungssystems eine interessante
Alternative zur konventionellen Therapie darstellt.



Christian Surber
Neue
Theorie der Vehikels
Institut für Spital-Pharmazie,
Universitätskliniken, Kantonsspital Basel
Konsumenten,
Patienten, Ärzte (Dermatologen), Apotheker und Wissenschaftler (Galeniker)
sprechen dem topischen dermatologischen Vehikel besondere Eigenschaften zu. Abhängig
vom Standpunkt sind die Sichtweisen und die Erwartungen an ein Vehikel sehr unterschiedlich.
Biopharmazeutische, pharma-zeutisch-technologische, pharmakologische, physikalische
und kosmetische Eigenschaften werden von Konsumenten, Patienten, Dermatologen,
Apothekern und Galenikern verschieden bewertet und verstanden. Es muss deshalb
analysiert werden, welche Eigenschaften der Vehikel für welche Effekte verantwortlich
sind. Dabei ist darzulegen, welche Vehikeltaxonomien heute vorliegen, wie diese
interpretiert werden, welche Effekte gemessen und wie diese Effekte gezielt verändert
werden können. Im Vordergrund der Diskussion steht die Frage, inwieweit die
Struktur eines Vehikel oder die Summe der Hilfsstoffe für bestimmte Effekte
verantwortlich sind (s. Abbildung).
Christian Surber
Holistic
Examination of Topical Dermatological Vehicles
Institut of Hospital-Pharmacy, University Clinics, Kantonssptial, Basel, Switzerland
Consumers,
patients, doctors (dermatologists), pharmacists and researchers believe that topical
dermatological vehicles comprise distinctive features. Depending an the point
of view the expectations in a vehicle effect may be very different. Biopharmaceutical,
pharmaceutical?technological, pharmacological physical and cosmetic features are
appraised by consumers, patients, dermatologists, pharmacists and researchers
differently. It is analysed which features of a vehicle are responsible for distinctive
effects. Furthermore known and novel vehicle taxonomies are presented. It is discussed
which vehicle effects can be measured and how these effects can be influenced.
The discussion is focused an the question whether the structural matrix or the
sum of the ingredients (s. figure) are responsible for a distinctive effect.
Â




Gerd Folkers
Paradigmenwechsel
in der Arzneimittelentwicklung
Präsident des Beirats des Collegiums Helveticum der ETH Zürich
„Fast
alle wirksamen Arzneimittel stammen aus der belebten Natur oder sind aus ihren
chemischen Strukturen abgeleitet“.
Diese Behauptung stimmt tatsächlich
und wird auch noch einige Zeit gelten. Dann aber werden die Arzneimittel auf dem
Markt sein, die sich momentan in der Entwicklung befinden und bei welchen die
Entwicklungslinie sozusagen auf den Kopf gestellt wurde.
Als Mitte der
Neunziger ein Psychopharmakon als potentieller Inhibitor der HIV-Protease und
damit als mögliches AIDS-Therapeutikum identifiziert wurde, zeigte sich darin
ein in der forschenden pharmzeutischen Industrie bereits weitgehend vollzogener
Wandel im Denkprozess der Arzneimittelentwicklung. Dabei steht als Arzneimittelwirkung
die optimale Erkennung einer auf molekularer Ebene definierten Zielstruktur im
Organismus, in der Regel ein Eiweiss, im Vordergrund. Das Eiweiss selbst ist das
Produkt eines Genfragments, welches mit einem Krankheitsgeschehen korreliert wurde.
Diese „molekulare Vorgehensweise“ hat Implikationen und Konsequenzen
für Therapien, Patienten und Märkte.
Zweifellos sind die
„Lebenswissenschaften“ (Life Sciences) unabdingbar für das Verständnis
von Gesundheit. Letztendlich beeinflusst jede Form therapeutischer Intervention
die Biochemie unseres Organismus. Mit der Ausschüttung kurzer Eiweissfragmente
im Gehirn, die Schmerz stillen, reagiert der Körper ebenso auf den äusseren
Reiz einer Akupunkturnadel, wie er die Einnahme eines ß-Rezeptorenblockers
mit der Absenkung des Blutdrucks beantwortet. Ein Gesprächspartner, der die
richtigen Worte findet, wird ebenso die Gleichgewichtslage unserer Biochemie im
Gehirn beeinflussen, wie ein „life style“ Medikament unsere Gefühlslage
„korrigiert“.
Es ist dabei offenkundig, dass das Individuum
selbst Einfluss auf die Therapie nimmt. In welchem Ausmass, hängt ab von
der genetischen Disposition, vom sozialen Kontext, von persönlichen Ängsten
und Erwartungen. Diese Faktoren und ihre Wirkungsweisen zu untersuchen, hat sich
ein Forschungszweig zur Aufgabe gemacht, der in der Pharmabranche „Functional
Genomics“ genannt wird. Die ihm eigenen Technologien werden in allen Unternehmen
der forschenden pharmazeutischen Grossindustrie eingesetzt. Sie dient der Erkennung
von Mustern auf der Ebene der Erbsubstanz und deren Produkte, der Eiweisse (Proteine)
und biologisch wirksamen kurzkettigen Eiweissfragmente (Peptide). Ihr Ziel ist
es, Möglichkeiten zu finden, diese Muster über gezielt entworfene Therapeutika
zu beeinflussen. Die Technologie und die riesigen Datenmengen, die „Functional
Genomics“ erst ermöglichen, werden von einem weltweiten Netz von großen
Unternehmen, Forschungsinstituten und kleinen hochspezialisierten Start-up-Companies
erzeugt. Erst die Kombination von Robotisierung, Informationstechnologie und Biotechnologie
hat Functional Genomics realisierbar gemacht. Die technologische Fähigkeit,
individuelle molekulare Muster aufzuzeichnen und auszuwerten hat die Arzneimittelforschung
und -entwicklung grundlegend geändert.




Claudia S. Leopold
Penetrationsorientierte
Vehikeloptimierung — Pharmakokinetische und pharmakodynamische Aspekte
Institut für Pharmazie, Universität Leipzig
Mit der
Applikation von Wirkstoffen auf die Haut lassen sich verschiedene Ziele verfolgen.
Einerseits kann es erwünscht sein, dass der Wirkstoff auf der Hautoberfläche
verbleibt; andererseits kann die Wirkstoffpenetration in tiefere Hautschichten
bis hin zur Resorption das Ziel sein. Die Wirkstoffpenetration ist durch die Wahl
des Vehikels beeinflussbar. Neben thermodynamischen Effekten, bedingt durch die
unterschiedliche Affinität des Wirkstoffes zu verschiedenen Vehikeln, spielen
hier penetrationsbeschleunigende, d.h. barrieremodifizierende Effekte eine große
Rolle. Solche Effekte können entweder direkt durch Messung des Wirkstofffluxes
in die Haut oder durch Wirkungsmessungen mit Arzneistoffen, die eine quantifizierbare
pharmakodynamische Reaktion hervorrufen, erfasst werden. Bei der Durchführung
der Wirkungsmessungen und der Auswahl der Wirkungsparameter müssen pharmakokinetische
Gesetzmäßigkeiten berücksichtigt werden, um möglichst genaue
Aussagen zur relativen Bioverfügbarkeit der Zubereitungen treffen zu können
und um zwischen thermodynamischen und penetrationsbeschleunigenden Vehikeleffekten
differenzieren zu können. Verschiedene intensitäts- und zeitbezogene
Wirkungsparameter und die aus simulierten Dosis-Wirkungs-Kurven ermittelten Bioverfügbarkeitsdaten
werden unter Berücksichtigung pharmakokinetischer Gesichtspunkte hinsichtlich
ihrer Aussagekraft beurteilt. Diese Wirkungsparameter sind die reziproke Latenzzeit
LT bis zum Auftreten eines pharmakodynamischen Effektes, die Wirkungsdauer D und
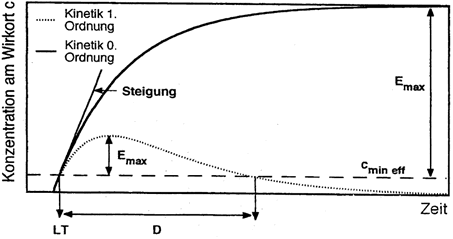
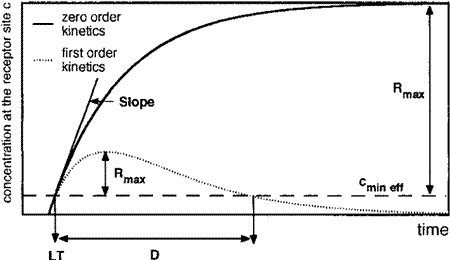
die maximale Wirkung Emax (Abb. 1).
Abb. 1: Simulierte Wirkstoffspiegel
am Wirkort für Penetrationskinetik erster (····)
und nullter (-) Ordnung bei Annahme eines offenen Einkompartimentmodells (Abkürzungen
siehe Text)
Werden Bioverfügbarkeits- und Beschleunigungsfaktoren
f und BF aus Dosis-Wirkungs-Kurven bestimmt, so können zu ihrer Bestimmung
die horizontalen Abstände zwischen parallel verlaufenden Kurven eines Standard-
und einer Testzubereitung sowie die Vertikalquotienten im Bereich der oberen Wirkplateaus
zwischen Test und Standard herangezogen werden (Abb. 2). Während die Horizontalabstände
thermodynamische wie auch penetrationsbeschleunigende Vehikeleffekte beinhalten,
können unterschiedliche Wirkplateaus nur durch barrieremodifizierende Vehikeleffekte
bedingt sein. Aus den Horizontalabständen zwischen parallelen Dosis-Wirkungs-Kurven
lässt sich also der Bioverfügbarkeitsfaktor bestimmen, während
die Vertikalquotienten den Beschleunigungsfaktor darstellen (Abb. 2). Bei penetrationsbeschleunigenden
Vehikeleffekten ist in der Regel durch die unterschiedlichen Wirkplateaus, die
von Standard und Test erreicht werden, mit einem nicht parallelen Kurvenverlauf
zu rechnen. Setzt man die Wirkstoffkonzentration in den Zubereitungen zur jeweiligen
Wirkstofflöslichkeit in den Vehikeln in Beziehung, was der Umrechnung der
Wirkstoffkonzentration in die Wirkstoffaktivität entspricht, so eliminiert
man die thermodynamischen Vehikeleffekte und kann dann aus den Horizontalabständen
der erhaltenen Aktivitäts-Wirkungskurven direkt den Beschleunigungsfaktor
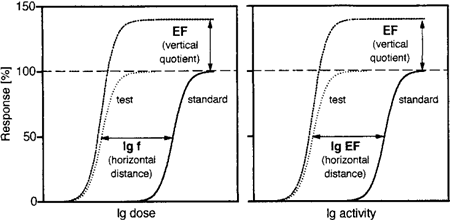
BF bestimmen (Abb. 2).
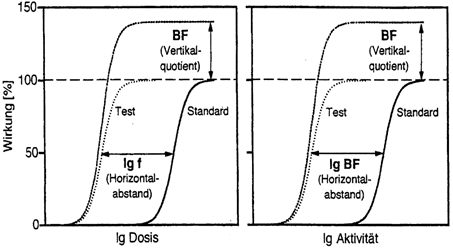
Abb. 2: Bestimmung von
Bioverfügbarkeits- und Beschleunigungsfaktoren aus Dosis- bzw. Aktivitäts-Wirkungskurven
Praktische Relevanz haben diese Ergebnisse, wenn es um die Planung und Durch-
führung von Wirkungsmessungen zur Quantifizierung von Vehikeleffekten oder
zur Beurteilung der Penetrationseigenschaften unterschiedlicher Wirkstoffe geht.
Die Wirkung sollte möglichst schnell, auf einfache Weise (z.B. visuell) und
ohne großen Versuchs- und Zeitaufwand erfaßbar sein. Diese Forderung
wäre bei den Wirkungsparametern maximale Wirkung und reziproke Latenzzeit
gegeben.
Grundsätzlich ist zu beachten, dass stationäre
Bedingungen garantiert werden sollten, um eine Wirkstoffentleerung, die zu verminderter
Wirkung führt, zu verhindern. Diese Forderung ist mit dem Wirkungsparameter
Wirkungsdauer nicht zu erfüllen. Stationäre Bedingungen können
durch Applikation großer Salbenvolumina über einen gewissen Zeitraum
sowie durch Applikation von Suspensionszubereitungen erreicht werden. Mit Suspensionszubereitungen
lassen sich allerdings keine Dosis-Wirkungs-Kurven aufnehmen. Es handelt sich
hier vielmehr um Einpunktmessungen, durch die nur das obere Wirkplateau einer
Dosis- oder Aktivitäts-Wirkungs-Kurve erfasst werden kann. Aus diesen Plateauwerten
lassen sich dann in Analogie zur Berechnung der Vertikalquotienten aus Dosis-
oder Aktivitäts-Wirkungs-Kurven Beschleunigungsfaktoren bestimmen. Die maximale
Wirkung ist ein geeigneter Parameter für eine solche Bestimmung. Weniger
geeignet für solche Einpunktmessungen ist der Wirkungsparameter reziproke
Latenzzeit, da hier im Beschleunigungsfaktor nur die Beeinflussung des Diffusionskoeffizienten
in der Barriere berücksichtigt wird. Grundsätzlich muss darauf geachtet
werden, dass nach Applikation von Suspensionszubereitungen, die in der Regel zum
maximalen Wirkstoffflux führen, noch nicht die intrinsische Aktivität
des Wirkstoffes (= erreichbarer Maximaleffekt im biologischen System) erreicht
wird, was eine Differenzierung zwischen den Vehikeln unmöglich macht. Eventuell
muss in einem solchen Fall auf einen anderen Modellarzneistoff ausgewichen werden.
Es sollte auch nicht vergessen werden, dass die maximale Wirkung beeinflusst wird
durch die Schwellenkonzentration am Wirkort cmin eff, die überschritten werden
muss, um eine Wirkung messen zu können (Abb. 1).
Prinzipiell sollten
statt Dosis-Wirkungs-Kurven immer Aktivitäts-Wirkungs-Kurven durch Einsatz
unterschiedlicher Wirkstoffaktivitäten in den Vehikeln aufgenommen werden,
um von vornherein thermodynamische Effekte zu eliminieren und somit penetrationsbeschleunigende
Effekte direkt erfassen zu können. Hier ist bei starker Penetrationsbeschleunigung
allerdings mit nicht-parallelen Kurven zu rechnen, da durch Penetrationsbeschleunigung
entsprechend höhere Wirkplateaus erreicht werden. Die Ermittlung von Beschleunigungsfaktoren
über den Horizontalabstand zwischen Aktivitäts-Wirkungs-Kurven setzt
aber eine Parallelität der Kurven voraus, so dass in diesem Fall die Bestimmung
von Vertikalquotienten im Plateaubereich sinnvoller erscheint.
Diese
Betrachtungen haben direkte Bedeutung für die FDA Guidance for Industry „Topical
dermatologic corticosteroids: In vivo bioequivalence“, in der die Durchführung
des Hautabblassungstestes mit Glucocorticoiden über die Messung der maximalen
Wirkung beschrieben wird. In dieser Guidance sollte darauf hingewiesen werden,
dass für eine unverfälschte Quantifizierung von Abblasseffekten stationäre
Bedingungen gewährleistet sein sollten und dass bei der Untersuchung von
Vehikeleffekten die intrinsische Aktivität des Modellwirkstoffes bekannt
sein muss.
Claudia S. Leopold
Penetration-oriented
optimization of ointment bases
University of Leipzig
With the topical application of drugs to the skin different objectives may be pursued. On the one hand, it may be desirable that the drug remains an the skin surface. In other situations, the penetration of the drug into deeper layers of the skin and thus drug absorption is required. Percutaneous drug penetration may be influenced by the proper choice of the vehicle, i.e. the ointment base. Besides any thermodynamic effects caused by different drug solubilities in the vehicles, penetration-enhancing, i.e. barrier-modifying effects may play a major role. Such effects may be quantified either directly by recording the drug flux through the skin or by the measurement of the pharmacodynamic response, if drugs are used that are able to induce a quantifiable pharmacodynamic reaction. The measurement of the pharmacodynamic response and the choice of the response parameter require the consideration of pharmacokinetic principles. This allows it to determine the relative bioavailability accurately and to differentiate between thermodynamic and penetration-enhancing vehicle effects. Various intensity- and time-related response parameters and bioavailability data, determined from simulated dose-response curves, were evaluated with regard to their suitability. These parameters included the reciprocal of the latency time of onset of the response LT, the duration of that response D and the maximum response Rmax (Fig. 1).
Fig.
1: Drug concentration vs. time profiles in the receptor compartment simulated
for first ( ….) and zero (—) order input kinetics. Open one-compartment-model,
(abbreviations see text)
Bioavailability and enhancement factors f and EF may be determined from the horizontal distance between parallel dose-response curves of a standard- and a test formulation or as vertical quotients from the upper plateau region of the curves (Fig. 2). While the horizontal distances between the curves include both thermodynamic and penetration-enhancing vehicle effects, differences in the response plateau values may only be caused by a barrier-modifying action. Consequently, bioavailability factors are determined from the horizontal distances while the vertical quotients of the response plateaus represent enhancement factors (Fig. 2). Penetration-enhancing vehicle effects typically lead to non-parallel dose-response curves because of the different maximum response plateaus that are reached. If the drug concentration in the vehicle is divided by the respective drug solubility, i.e. the drug concentration is converted into the drug activity, the influence of thermodynamic effects is eliminated and enhancement factors can then be determined from the horizontal distance between so-called activity-response curves (Fig. 2).
Fig. 2: Determination of bioavailability and enhancement factors from dose-
and activity-response curves of a test and a standard preparation.
These observations are of practical relevance, if studies are planned to quantify vehicle effects or to evaluate the penetration properties of drugs by pharmacodynamic measurements. The pharmacodynamic response should be measurable in a quick and easy way (e.g. visually) thus avoiding sophisticated experimental setups and time-consuming experiments. These requirements are given with the response parameters maximum response and the reciprocal of the time of onset.
In general, steady-state conditions should be guaranteed to avoid drug depletion in the vehicle, which would lead to a reduced response. However, steady-state conditions, i.e. zero order penetration kinetics, cannot be achieved if the duration of a response is measured. Zero order penetration kinetics can be maintained for a certain time period by application of large amounts of solution-type ointment formulations. With suspension-type ointments a constant drug penetration rate is observed as long as there is an excess amount of undissolved drug present. However, with suspension-type ointments no dose-response curves can be obtained. They only allow onepoint measurements in the upper plateau region of dose- or activity-response curves. From these values enhancement factors may be calculated in analogy to the calculation of vertical quotients from dose- or activity-response curves. The maximum response represents a suitable response parameter for one-point measurements. A less suitable parameter for these one-point-measurements is the reciprocal of the latency time, because enhancement factors determined with this parameter describe only the contribution of an increased diffusion coefficient in the barrier to overall penetration enhancement and disregard the contribution of increased drug solubility in the barrier. In general, it has to be taken care that after application of suspension-type preparations the intrinsic activity of the drug (= maximum effect in the biological system) is not reached because drug suspensions typically lead to the maximum drug flux. This would make a differentiation between different vehicles impossible. In this case, another model drug should be chosen. It should also be mentioned that the maximum response is affected by the threshold concentration at the receptor site Cmin eff, which has to be overcome to induce a measurable response (Fig. 1).
In general, activity-response curves should be recorded instead of dose-response curves to eliminate thermodynamic vehicle effects and to be able to directly quantify penetration-enhancing effects. However, strong penetration enhancement causes non-parallel curves because of the different response plateaus that are reached. The determination of enhancement factors from the horizontal distance between activity-response curves however requires a parallelism of the curves. Therefore, vertical quotients from the upper response plateaus should be calculated in this case.
These theoretical observations have impact an
the experimental methods described in the FDA Guidance for Industry „Topical
dermatologic corticosteroids: In vivo bioequivalence“, which uses the maximum
skin blanching response caused by glucocorticoids as response parameter. In this
Guidance it should be mentioned that for an accurate quantification of the skin
blanching response steady-state conditions have to be maintained and that the
intrinsic activity of the applied corticosteroid should be known.




Andreas J. Bircher
(#)
Wirksamkeit und Verträglichkeit eines Phytokosmetikums
bei atopischer Dermatitis
Allergologische Poliklinik, Kantonsspital Basel
Ein in einem europäischen
Land frei verkäufliches, häufig bei Hautkrankheiten verwendetes Phytokosmetikum
wurde untersucht. Es enthält nach CFTA deklariert circa 34 Inhaltsstoffe,
neben pflanzlichen Substanzen auch bekannte Kontaktallergene. Bisher wurden damit
einige unkontrollierte Studien bei unterschiedlichsten Hautkrankheiten durchgeführt
und mehrheitlich positive Resultate publiziert. Die Creme wurde vermehrt auch
in die Schweiz importiert und zur Selbstmedikation bei Kleinkindern mit atopischer
Dermatitis eingesetzt.
Im Rahmen einer Pilotstudie wurden 21 Patienten
mit atopischer Dermatitis untersucht. Einschlusskriterien waren eine chronische
oder chronisch?rezidivierende Dermatitis in symmetrischer Verteilung. Das Alter
betrug 2 bis 56 (Mittelwert 26) Jahre (inkl. 5 Kinder zwischen 2 und 4 Jahren
), 9 männlichen, 12 weiblichen Geschlechts. Das Ausmaß der Dermatitis
wurde mit der Neunerregel, der Schweregrad mittels des SCORAD-Index erfasst. Eine
bilaterale Lokalisation mit symmetrischem Befall wurde gewählt, die Therapie
mit dem Verum und einem von Konsistenz, Farbe und Geruch vergleichbaren Vergleichspräparat
(„Placebo“) wurde doppelblind randomisiert zugeordnet und während
vier Wochen angewendet. Als Rescue-Medikamente wurden Prednicarbat-Salbe und Cetrizin-Tabletten
abgegeben. Die Patienten wurden an den Tagen 0, 3, 7, 14, 21 und 28 klinisch,
mittels des SCORAD-Index und einer visuellen Analogskala auf Wirkung und Nebenwirkungen
evaluiert. Ein Patient brach die Studie am Tag 3 wegen einer einseitigen Aggravation
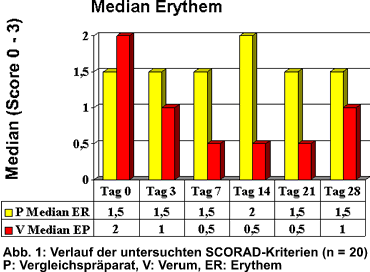
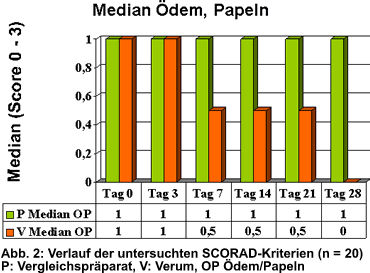
auf der Placeboseite ab, 20 Patienten vollendeten die Studie. Bei 16 kam es frühestens
ab Tag 3 im SCORAD zu einem mäßigen bis ausgeprägten Unterschied
zugunsten der Verumseite (Abb. 1-2), bei vier Patienten wurde kein signifikanter
Unterschied beobachtet. Fünf Patienten benötigten im Verlauf die topische
Reservemedikation (Prednicarbat) wegen Verschlechterung des Hautzustandes, vier
Patienten bei der Vergleichsmedikation, ein Patient beim Verum. Außer einer
leichten Irritation, vor allem bei der Vergleichsmedikation, wurden keine anderen
Nebenwirkungen beobachtet. Frühestens sechs Wochen nach Abschluss wurden
Epikutantests durchgeführt, relevante Kontaktsensibilisierungen wurden nicht
gefunden.
Das Phytokosmetikum schien eine rasch auftretende, entzündungshemmende
und juckreizstillende Wirkung zu haben, wobei das aktive Prinzip aufgrund der
deklarierten Inhaltsstoffe nicht klar war. Die Analyse mittels Flüssigkeits?
und Gaschromatographie des Präparates ergab, sowohl im in der Studie verwendeten
Lot als auch in anderen Chargen, das Vorliegen von Triamcinolonacetonid in Konzentrationen
von 16 bis 40 (Mittel 27) µg/g. Diese Werte liegen tiefer als die typischen
Konzentrationen von 100 bis 1000 µg/g in therapeutischen Präparaten.
Da es sich um ein als Kosmetikum deklariertes Präparat handelt, ist der Gehalt
von Kortikosteroiden illegal, und die Gesundheitsbehörden wurden informiert.
Zwischenzeitlich wurden von der Vertreiberfirma verbesserte Kontrollen der GMP
eingeführt, um die deklarierte Zusammensetzung des Kosmetikums zu gewährleisten.
Die Herkunft des Triamcinolonacetonid blieb unklar, eine Kontamination ist unwahrscheinlich,
da in mehreren Lots wiederholt ähnliche Konzentrationen gefunden wurden.
Eine Zugabe der Substanz zu einem der Ausgangsstoffe oder zum Endprodukt ist möglich.
Unsere Untersuchungen zeigen, dass offenbar auch mit geringeren Konzentrationen
eines Kortikosteroides eine therapeutische Wirkung erzielt werden kann. Frei verkäufliche
Präparate, die eine ungewöhnliche therapeutische Wirkung zeigen, sollten
deshalb auf illegale Wirkstoffe untersucht werden.
(#)
unter Mitarbeit von B. Hrubes (Allergologische Poliklinik und Institut für
Spitalpharmazie, Kantonsspital Basel), U. Hauri (Kantonales Laboratorium Basel-Stadt)
und Ch. Surber (Institut für Spitalpharmazie, Kantonsspital Basel)
Prof.
Dr. med. Andreas Bircher


Andreas Klotz
unter Mitarbeit von A. zur Mühlen und M Veeger
Wirksamkeitsprüfung von Hautschutzmitteln im repetitiven Irritationstest
Stockhausen GmbH & Co. KG, Krefeld
Bei vielen beruflichen
Tätigkeiten wird die Haut durch häufiges Händewaschen, intensive
Feuchtarbeit und wiederholten Kontakt zu gering irritativen Arbeitsstoffen wie
Wasser, Detergenzien oder Kühlschmierstoffe stark belastet. Neben technischen
und organisatorischen Maßnahmen, die eine Reduktion der Hautbelastung zum
Ziel haben, haben sich Hautschutzmittel zum Schutz der Haut vor beruflichen Belastungen
bewährt. Hierbei handelt es sich um spezielle kosmetische Formulierungen,
die vor der Arbeit aufgetragen werden und daher nicht mit Pflegeprodukten, die
nach der Arbeit verwendet werden, zu verwechseln sind.
Die Empfehlung
solcher Produkte richtet sich hierbei häufig nach der Löslichkeit des
Schutzproduktes in dem jeweiligen Arbeitsstoff. Dementsprechend werden für
wässrige Substanzen Wasser-in-Öl-Emulsionen oder Fettsalben empfohlen,
wogegen als Schutz gegenüber öligen Stoffen Öl-in-Wasser-Emulsionen,
Suspensionen oder Gele angeboten werden. In einigen experimentellen In-vivo-Humanstudien
konnten jedoch Ausnahmen zu dieser simplifizierenden Regel festgestellt werden
[1].
In der Diskussion ist, ob spezieller, belastungsadaptierter Hautschutz
zur Verwendung vor der Arbeit und dem Hautzustand angepasste Pflegeprodukte nach
der Arbeit, überhaupt nötig sind. Teilweise wird die Meinung vertreten,
dass die Wirksamkeit dieser Produkte nicht auf einem Schutz, sondern auf einer
Unterstützung der natürlichen Hautregeneration beruht, womit die Anwendung
entsprechender Feuchtigkeits- oder Pflegecremes nach und ggf. zusätzlich
vor der Arbeit völlig ausreichend wäre.
[2, 3]
Für
die Überprüfung von Hautschutzprodukten werden in der Literatur verschiedene
Verfahren vorgeschlagen [1, 4-13]. Anerkennung genießt die von einer Arbeitsgruppe
überarbeitete Methode des erstmals von Frosch und Kurte im Jahr 1993 [7]
beschriebenen Repetitiven Irritationstestes [14]. Bei diesem Modell erfolgt die
Applikation des Modellirritants (0,5 %iges SDS oder unverdünntes Toluol)
in Finnkammern auf mit Hautschutzprodukt eingecremte Hautareale des volaren Unterarmes
zweimal täglich über einen Zeitraum von einer Woche. Bewertet wird hierbei
neben dem visuellen Score auch die Barrierewirkung der Haut in Form des transepidermalen
Wasserverlustes im Vergleich zu einem nicht geschützten Hautareal. Durch
eine Modifikation des Verfahrens, bei dem der Auftrag der Prüfproduke erst
nach der Irritation erfolgt, kann auch der Effekt der Produkte auf die Hautregeneration
beurteilt werden.
In den beschriebenen Untersuchungen wurde ein neuartiges
mehrphasiges Emulsionssystem vom Typ Wasser-in-Öl-in-Wasser (W/O/W), das
bislang nur Einsatz in hochwertiger Gesichtskosmetik findet, im Vergleich zu Vaseline
(VAS), einer Panthenol und Vitamin E enthaltenden Wasser-in-Öl-Emulsion (W/O)
und einem Lipogel (LIP=Mischung aus Vaseline, einem Wachs und einer Silikonverbindung)
hinsichtlich Schutz- und Regenerationswirkung in einem repetitiven, okklusiven
Irritationstest [14, 15] an jeweils 15 hautgesunden Probanden gegenüber Natriumlaurysulfat
untersucht. Dabei zeigte das neuartige Schutzprodukt vom W/O/W-Typ die beste Schutzwirkung
vor SLS-induzierter Hautschädigung und einen signifikant besseren Schutz
als das wasserfreie Lipogel. Die Untersuchung des Einflusses der Produkte auf
die Hautregeneration ergab eine deutlich verschlechterte Barrierewiederherstellung
durch Vaseline im Vergleich zum unbehandelten Kontrollfeld – aber auch die Wasser-in-Öl-Emulsion
(W/O) und das Lipogel (LIP) hatten keinen positiven Effekt auf die Wiederherstellung
der geschädigten Hautbarriere (Tab. 2). Dagegen vermochte die neuartige Hautschutzformulierung
(W/O/W), wenn auch nicht signifikant, so jedoch tendenziell, die Erreichung eines
normalen Hautzustandes nach SLS-Irritation positv zu unterstützen.
Literatur
1. Frosch,
P.J. and A. Kurte, Efficacy of skin barrier creams (IV). The repetitive irritation
test (RIT) with a set of 4 standard irritants. Contact Dermatitis, 1994. 31: p.
161-168.
2. Berndt, U., et al., Efficacy of a barrier cream and its vehicle
as protective measures against occupational irritant contact dermatitis. Contact
Dermatitis, 2000. 42: p. 77-80.
3. Zhai, H. and H.I. Maibach, Moisturizers
in preventing irritant contact dermatitis: an overview. Contact Dermatitis, 1998.
38: p. 241-244.
4. Grunewald, A.M., et al., Lipophilic Irritants – Protective
value of urea- and of glycerol-containing oil-in-water emulsions. Dermatosen,
1996. 44: p. 81-86.
5. Frosch, P.J., A. Kurte, and B. Pilz, Efficacy of skin
barrier creams (III). The repetitive irritation test (RIT) in humans. Contact
Dermatitis, 1993. 29: p. 113-118.
6. Frosch, P.J., et al., Efficacy of skin
barrier creams (II). Ineffectiveness of a popular „skin protector“ against
various irritants in the repetitive irritation test in the guinea pig. Contact
Dermatitis, 1993. 29: p. 74-77.
7. Frosch, P.J., et al., Efficacy of skin
barrier creams. Contact Dermatitis, 1993. 28: p. 94-100.
8. Schlüter-Wigger,
W. and P. Elsner, Efficacy of 4 commercially available protective creams in the
repetitive irritation test (RIT). Contact Dermatitis, 1996. 34: p. 278-283.
9. Zhai, H., P. Willard, and H.I. Maibach, Evaluating skin-protective materials
against contact irritants and allergens. Contact Dermatitis, 1998. 38: p. 155-158.
10. Glang-Vetter, S. and F.A. Bahmer, Testing of Weak Irritants by the IT50-method
In vivo estimation with an objective, reproducible, and subject friendly irritancy
test model. Dermatosen, 1999. 47: p. 157-161.
11. Zhai, H., P. Willard, and
H.I. Maibach, Putative skin-protective formulations in preventing and/or inhibiting
experimentally-produced irritant and allergic contact dermatitis. Contact Dermatitis,
1999. 41: p. 190-192.
12. Gehring, W., M. Gloor, and P. Kleesz, Predictive
washing test for evaluation of individual eczema risk. Contact Dermatitis, 1998.
39: p. 8-13.
13. Zhai, H. and H.I. Maibach, Effect of barrier creams: human
skin in vivo. Contact Dermatitis, 1996. 35: p. 92-96.
14. Schnetz, E., et
al., Multicentre study for the development of an in vivo model to evaluate the
influence of topical formulations on irritation. Contact Dermatitis, 2000. 42:
p. 336-343.
15. Wigger-Alberti, W., A. Krebs, and P. Elsner, Experimental
irritant contact dermatitis due to cumulative epicutaneous exposure to sodium
lauryl sulphate and toluene: single and concurrent application. British Journal
of Dermatology, 2000. 143: p. 551-556.
Tabelle 1: Hautschutzwirkung von Externa im rep. okkl. Irritationstest (n=15)
| Produkt | delta TEWL [mg/hm²] |
| W/O/W – 0,5 % SLS | 8,76 ± 1,18 *** |
| VAS – 0,5 % SLS | 11,78 ± 1,63 *** |
| LIP – 0,5 % SLS | 13,17 ± 2,28 * |
| W/O – 0,5 % SLS | 13,88 ± 1,90 n.s. |
| 0,5 % SLS | 19,56 ± 2,08 |
Tabelle
2: Einfluss von Externa auf die Hautregeneration (n=15)
| Produkt | delta TEWL [mg/hm²] |
| 0,5 % SLS – W/O/W | 8,32 ± 0,83 |
| 0,5 % SLS | 9,06 ± 1,20 |
| 0,5 % SLS – LIP | 9,33 ± 1,26 |
| 0,5 % SLS – W/O | 9,62 ± 1,05 |
| 0,5 % SLS – VAS | 13,11 ± 2,39 |
Abbildung: Einfluss von Externa auf SLS-induzierte Hautirritation (TEWL)
| GD – Online | A. Klotz et al.: Efficacy of Skin Protectants | ||||||||||||||||||||||||||
| Printversion or Abstracts 2001 | |||||||||||||||||||||||||||
|
A. Klotz, A. zur Mühlen, M. Veeger Testing
the Efficacy of Skin Protectants with the Repetitive Irritation Test Background: In many occupational activities, the skin is put under great stress from frequent washing of hands, working for long periods in damp and wet conditions, and repeated contact with slightly irritative workplace substances such as water, detergents and cooling lubricants. In addition to the technical and organisational measures that can be taken to reduce this skin stressing, skin protectants have also proved to be an effective way of protecting the skin against on-the-job stressing. Such protectants are special cosmetic formulations which are applied to the skin before starting any work, and they should therefore not be confused with skin conditioning or care products, which are meant to be used when the work is finished. Making any recommendations as to which products to use is frequently guided by the solubility of the protectant in the particular workplace substance. Water-in-oil emulsions or oily ointments are therefore recommended for water-based substances, whereas oil-in-water emulsions, suspensions or gels are put forward as protection against their oil-based counterparts. However, exceptions to this somewhat oversimplified rule have been found in a number of experimental in-vivo human studies [1]. Central to the discussion is whether special stress-matched skin protection for applying before work, and care products matched to the skin condition and applied after work are actually necessary. The view is held in some circles that the efficacy of these products is not based on protecting the skin but on supporting the skin’s natural regeneration, and that using suitable moisturising or skin care creams after, and if need be also before work, is therefore perfectly adequate [2, 3]. Various methods are put forward for testing skin protectants in the literature available on this subject [1, 4-13]. The method modified by a working group of the German Clinic for Occupational Dermatology, and based on the repetitive irritation test [7] first described by Frosch and Kurte in 1993 [14], enjoys recognition. In this model, the skin protectant is first of all put on areas of skin on the volar forearm and the model irritant (0.5% SDS or undiluted toluene) then applied to these areas in Finn chambers twice a day for a period of one week. In addition to the visual score, evaluation also takes into account the barrier function of the skin in the form of the transepidermal water loss in comparison with an area of skin that has not been protected. By modifying the method and not applying the test product until after the irritation, the effect of the product on skin regeneration can also be assessed. Materials and Methods: In the tests described, a new kind of multiphase emulsion system of the type water-in-oil-in-water (W/O/W), which had mainly been used only in high-quality facial cosmetics before, was tested on 15 candidates with healthy skin and compared with Vaseline (VAS), a water-in-oil emulsion (W/O) containing panthenol and vitamin E, and a lipogel (LIP = mixture of Vaseline, a wax and a silicone compound as to their protective effect in a repetitive, occlusive irritation test [14, 15] and their influence on skin regeneration where skin irritation had been induced by sodium lauryl sulphate. Results:
Table 2: Influence of topical formulations on skin regeneration (n=15)
Diagram 1: Influence of topical formulations on SLS-induced skin irritation (TEWL) In the repetitive, occlusive irritation test (Table 1, Diagram 1), the new protectant of the type water-in-oil-in-water demonstrated the best protective effect against SLS-induced skin damage and significantly superior protection to an anhydrous lipogel. The tests carried out to determine the influence of the products on skin regeneration (Table 2, no diagram) showed a considerable deterioration in barrier recovery in the case of Vaseline compared with the untreated reference area – but nor did the water-in-oil emulsion (W/O) or the lipogel (LIP) have any positive effect on restoring the barrier function of the damaged skin. The new skin protection formulation (W/O/W), however, showed definite signs, even though they were not significant, of being able to support the attainment of normal skin condition following SLS irritation. Summary/Discussion: The prevention of occupational skin diseases can be effectively supported by using suitable, special skin protection products. Using the wrong types of preparations, such as an oil-in-water moisturiser, leaves the skin not only inadequately protected, but it can even impair restoration of a natural skin condition after the skin has been exposed to stressing. The example of Vaseline and the hydrophilic W/O/W emulsion shows only too clearly that a product recommendation cannot be made simply on the basis of knowing the hydrophilic or lipophilic properties of the protectant and the substances concerned. The efficacy of each protective product must be tested using suitable in-vivo methods. The method employed in the repetitive, occlusive irritation test is highly suitable for evaluating skin protectants and it should be adopted as a standard method. Additionally, it is possible to assess the main principle of how topically applied skin protectants work (protectively/regeneratively) using the inverted, repetitive, occlusive irritation test. References: 1.
Frosch, P.J. and A. Kurte, Efficacy of skin barrier creams (IV). The repetitive
irritation test (RIT) with a set of 4 standard irritants. Contact Dermatitis,
1994. 31: p. 161-168. | |||||||||||||||||||||||||||








Reinhard Neubert
Zukunft
der pharmazeutischen Technologie aus der Sicht der Dermopharmazie
Institut für Pharmazeutische
Technologie und Biopharmazie, Fachbereich Pharmazie der Martin-Luther-Universität
Halle-Wittenberg
Neben „klassischen“ dermalen Zubereitungen
gibt es heute auch moderne Vehikelsysteme für die dermale Anwendung. Sie
basieren auf Liposomen, multiplen Emulsionen oder Nanopartikeln und besitzen Vor-
und Nachteile. Bei den Liposomen wird besonders die dermale Anwendung der Transfersomenâ
kontrovers in der Literatur diskutiert. Bei allen Vehikelsystemen muss die Frage
beantwortet werden, ob sie für eine kontrollierte Arzneistoff-Liberation
bzw. für das drug targeting nutzbar sind. Es konnte gezeigt werden, dass
mit Hilfe sowohl der multiplen Emulsionen als auch der Nanopartikel über
den Liberationsprozess die Penetration in die Haut gesteuert sowie Stabilitätsprobleme
gelöst werden können.
Zu den modernen dermalen Zubereitungen gehören auch kolloidale Vehikel
wie Mikroemulsionen (ME). Die Theorien zum Mechanismus der Penetration der Wirkstoffe
aus ME in und durch die Haut sind Gegenstand zahlreicher Untersuchungen gewesen.
Hierbei konnte gezeigt werden, dass die ME-Systeme große Vorteile hinsichtlich
der transdermalen Therapie aufweisen.
Neben den ME gibt es weitere zukunftsträchtige
kolloidale Systeme. Mit einfachen galenischen Maßnahmen lässt sich
der Durchmesser der kolloidalen Phase verändern und damit die Penetration
beinflussen.
Reinhard Neubert
Future
of Pharmaceutics under Dermatopharmaceutical Aspects
Department of Pharmazeutische Technologie und Biopharmazie, Fachbereich Pharmazie der Martin-Luther-Universität Halle-Wittenberg
Starting from the „classical“ dermal
formulations in the lecture modern vehicle systems for dermal administration are
presented. Liposomes, multiple emulsions and nanoparts are shown and dis? and
advantages of these systems are discussed. Regarding the liposomes the dermal
administration of Transfersomes® is demonstrated because it is controversially
discussed in the literature. The presentation of these vehicle systems is focused
an their applicability for controlled drug delivery and for drug targeting, respectively.
Using multiple emulsions and nanoparts it is shown that the penetration of drugs
can be controlled by the liberation process.
In the second part of the
lecture colloidal drug delivery systems are presented. First of all the dermal
administration of microemulsions (ME), the theories regarding the mechanism of
drug penetration from these systems and the advantages of ME for the transdermal
administration are demonstrated.
Finally, the chances of colloidal vehicle
systems are discussed and effective colloidal systems for dermal drug delivery
are presented. Using simple galenic procedures it is shown that the diameter of
the colloidal phase can be changed to influence the drug penetration.

