Teil
1 Tagungshauptprogramm
Teil 2
Workshop Magistralrezepturen
Teil
3 Workshop Sonnenschutz
Teil
4 Poster
3.
Symposium „Gesundheitsökonomie in der Dermatologie“ (PDF-Dokument:
Programm und Abstracts)
Satellitensymposium
des Industrieverbandes Körperpflege- und Waschmittel e.V. (IKW): „Kosmetika
– wirksam und sicher“
Prof. Dr. med. Erwin
Schöpf
Biotechnologie und Tissue Engineering in der
Dermatologie:
Ein
Weg in die Zukunft?
Universitäts-Hautklinik, Freiburg
Bei der Suche nach neuen und besseren Behandlungsmöglichkeiten
von Krankheiten hat sich die Biotechnologie für den Gesundheitsmarkt in den
letzten Jahren zu einer unverzichtbaren Schlüsseltechnologie entwickelt.
Dies ist möglich geworden durch die großartigen Fortschritte, insbesondere
im Bereich der Molekularbiologie. Neben der Wirkstoffentwicklung mit biotechnologischen
Methoden wird zunehmend der Bereich TissueEngineering, d.h. das Züchten eines
lebenden Gewebeersatzes mit der Aussicht, Gewebedefekte durch vollwertige und
lebende Gewebekonstrukte zu rekonstruieren, als ein zukünftig wichtiger Bereich
der Biotechnologie angesehen. TissueEngineering ist damit ein neues interdisziplinäres
biomedizinisches Forschungsgebiet, welches Material- und Biowissenschaften mit
der klinischen Forschung zur Entwicklung lebender Substitute von Gewebedefekten
vereinigt. Dadurch können die bekannten Nachteile des allogenen Gewebeersatzes
durch Verwendung autologer Zellen mit fehlender immunologischer Abwehrreaktion
und Infektübertragung vermieden werden. Darüber hinaus erlaubt diese
Technologie eine Vermehrung der autologen Zellen ex vivo unter Minimierung der
Biopsiemengen.
Schon im Jahre 1979 wurde von Greenetal eine autologe
Keratinozytentransplantation zur Behandlung von Verbrennungswunden eingesetzt.
Inzwischen gibt es international mehrere Firmen, die unter GMP-Bedingungen autologe
Keratinozytenkultivierung anbieten, insbesondere zur Behandlung von chronischen
Wunden. Darüber hinaus bietet eine Firma, die als Start-up Company des Universitätsklinikums
Freiburg vor wenigen Jahren gegründet wurde, auch die Möglichkeit der
Vitiligo-Behandlung mit autologen Melanozytentransplantationen an. Über die
klinische Anwendung in der Dermatologie hinaus, sind dreidimensionale autologe
Knorpel- und Knochenkonstrukte auf der Basis bioresorbierbarer Materialien wie
Polymilchsäurezucker in der Entwicklung. Allerdings sind unter GMP-Bedingungen
gezüchtete autologe Zellpräparationen bei älteren Menschen nur
schwer zu erhalten. Die Kultivierungsdauer ist relativ lang (etwa drei Wochen)
und nicht zuletzt ist die Technologie sehr teuer. TissueEngineering, z.B. bei
chronischen Wunden, ist daher aufgrund pharmakoökonomischer Studien nur bei
bestimmten Indikationen sinnvoll. Von großer Bedeutung werden in der Zukunft
die Ausnutzung der Pluripotenz von Stammzellen oder gewebetypischer Vorläuferzellen
sein. Zusammenfassend ist festzustellen, dass auch in der Dermatologie das TissueEngineering
eine zunehmende Bedeutung erlangen wird, nicht zuletzt auch durch die Möglichkeit,
Gendefekte durch Transfektion gesunder Gene in autologe Zellen der Patienten zu
kompensieren, wie dies am Beispiel der Epidermolysis bullosa hereditaria denkbar
wäre.
| Foto: Gesellschaft für Dermopharmazie
|
| Foto: Gesellschaft für Dermopharmazie
|


Prof. Dr. med. Dr.
rer. nat. Erhardt Proksch*
Dermatopharmakologie von Dexpanthenol
Universitäts-Hautklinik, Kiel
Dexpanthenol-haltige Cremes und Salben werden
seit Jahren für die Behandlung von Läsionen (oberflächliche Wunden)
der Haut und der Schleimhäute benutzt. Die Wirkungsmechanismen dieser Substanz
sind aber nur zum Teil bekannt. Dexpanthenol wird im Gewebe zu Panthothensäure
umgewandelt, die eine Komponente des Coenzyms A darstellt. Coenzym A katalysiert
den ersten Schritt der Synthese von Fettsäuren und Sphingolipiden. Diese
Lipide sind wesentliche Bestandteile der bilamellären Schichten des Stratum
corneums als Permeabilitätsbarriere der Haut und auch in der Zellmembran
aller Säugetierzellen enthalten.
In einer kontrollierten Studie
haben wir den Einfluss einer Dexpanthenol-haltigen Salbe auf die Reparatur der
gestörten Permeabilitätsbarriere, auf die Hydratation des Stratum corneums,
auf die Hautrauhigkeit und auf die Entzündungen der Haut untersucht. Die
Irritation wurde durch Applikation von Natriumlaurylsulfat in einer Patch-Test-Kammer
über 24 Stunden induziert Danach wurde eine Dexpanthenol-haltige Salbe (Bepanthen®
Salbe) auf das Vehikel (Wirkstoffgrundlage) zweimal täglich appliziert und
Barrierereparatur, Hydratation, Rauhigkeit und Entzündung der Haut mit Hilfe
biophysikalischer Messmethoden untersucht.
Die Messungen ergaben eine
signifikant beschleunigte Reparatur der Permeabilitätsbarriere nach Anwendung
der Dexpanthenol-haltigen Salbe im Vergleich zur Vehikel behandelten und zur unbehandelten
Haut. Beide Präparate, Verum und Placebo, führten zu einem Anstieg der
Stratum corneum-Hydratation; die Hydratation war jedoch nach Anwendung der Dexpanthenol-haltigen
Salbe deutlich ausgeprägter. Beide Salben reduzierten auch die Hautrauhigkeit,
aber auch hier war das Verum-Präparat überlegen. Die Dexpanthenol-haltige
Salbe reduzierte signifikant die Rötung der Haut als Zeichen der Entzündung;
das Vehikel beeinflusste die Entzündung nicht.
Zusammenfassend zeigen
unsere Untersuchungen, dass die Behandlung mit einer Dexpanthenol-haltigen Salbe
signifikant zu einer beschleunigten Reparatur der Permeabilitätsbarriere
der Haut, einem Anstieg der Stratum corneum-Hydratation, einer Reduktion der Hautrauhigkeit
und einer Reduktion der Entzündung führt.
*unter Mitarbeit
von H.P. Nissen, Dermaconsult, Bonn-Alfter
Prof. Dr. med. Dr. rer. nat. Erhardt Proksch
| Foto: Gesellschaft für Dermopharmazie |
| Foto: Gesellschaft für Dermopharmazie |


Dipl.-Ing. Martin
Albrecht
Entwicklung
eines neuartigen an der Hautmembranstruktur orientierten Cremepräparates
zur Pflege bei trockener Haut
Kuhs GmbH & Co. KG, Leichlingen
Während der Evolution
fand die Natur einen natürlichen Weg, den Körper vor der Austrocknung
und so zusätzlich vor dem unkontrollierten Eindringen von exogenen Substanzen
zu schützen: die Hautlipid-Barriere. Die äußerste Schicht der
Epidermis, das Stratum Corneum, bildet eine Permeabilitätsbarriere, die vor
der Austrocknung schützt und so das Leben an Land ermöglicht. Die Stärke
und Funktion dieser Barriere werden durch eine spezifische Zusammensetzung lamellar
orientierter Lipide im Intrazellularraum des Stratum Corneums charakterisiert.
Diese Lipide, die in den „Outland Bodies“ des Stratum Granulosum synthetisiert
werden, haben beim Übergang zum Stratum Corneum eine primär enzymatisch
gesteuerte Modifikation erfahren. Es entstehen in erster Linie mittel- bis langkettige,
gesättigte Fettsäuren, frei und gebunden in einer Triglyceridstruktur,
verschiedene Ceramid-Typen und Cholesterol bzw. seine Derivate. Die Struktur dieser
Lipide in lamellaren Schichten ist von außerordentlicher Bedeutung für
die Barriere-Funktion.
Schon geringe Änderungen der Lipidbarrieren-Zusammensetzung,
des pH-Werts oder eine Ladungsveränderung können die Phasenübergangstemperatur
der Barrierelipide und somit deren Struktur beeinflussen. Viele topische Produkte
erzeugen strukturelle Defekte, indem sie die Fluidität der Lipidbarriere
erhöhen. Dieses ist der derzeit bedeutendste Faktor, welcher eine verminderte
Barrierefunktion beschreibt. Unter Verwendung von anionischen, nicht-ionischen
(bevorzugt kurzkettigen) Emulgatoren können die an sich lamellaren Strukturen
der Lipidbarriere verändert werden. Ein Anstieg von sogenannten „hydrophilic
pathways“ ist zu erwarten. Dies ist ein irreversibler Prozess. Bei einer
kontinuierlichen Anwendung ist die Haut nicht in der Lage, ihre Regenerations-
und Schutzfunktion zu halten.
Daher muss die Frage gestellt werden, ob
der Einsatz dieser Ingredentien in topisch applizierbaren Produkten physiologisch
ist. Indem die Lipidbarriere geöffnet und nicht wieder verschlossen wird,
übt man einen repetetiven Stress aus, der einen degenerativen Prozess zur
Folge haben kann. Eine erhöhte Sensibilität gegenüber Fremdstoffen
und damit eine erhöhte Disposition für allergische Reaktionen und Ekzeme
jeglicher Art ist zu erwarten.
DMS®, Derma Membrane Structure®,
ist eine Cremebase, welche spezifisch für die Bedürfnisse trockener
und sensibler Haut entwickelt worden ist. Sie baut sich auf spezifisch zusammengesetzten
Membranlipiden auf, welche in dem Cremekonzentrat lamellare Strukturen aufweisen.
Die Koexistenz von physiologischer Struktur und physiologischer Zusammensetzung
ist eine wichtige Voraussetzung für ein „gesundes“ Hautbild.
Als Konsequenz sollte ein ideales, topisches Produkt primär physiologische
Inhaltsstoffe, wie Triglyceride unterschiedlicher Kettenlänge, hydriertes
Phosphatidylcholin, Mono- oder Diglyceride, Derivate des Cholesterols und NMF’s
enthalten. Bei der Entwicklung von DMS® vermieden wir den Einsatz physiologisch
bedenklicher Emulgatoren und Inhaltsstoffe, welche die Lipidbarriere stören
können (Konservierungsmittel, Duftstoffe, comedogene Lipide, wie Paraffine
und Farbstoffe). Mit Hilfe von Hochdrucktechnologie verwandelten wir ein zunächst
fluides, primär vesikuläres System in ein rigides, primär lamellares
System. Mit Hilfe von Experimenten arbeiteten wir heraus, dass die besten Ergebnisse
unter Einsatz von 25 – 35 % des Cremekonzentrates zu erreichen sind. In Studien
konnte der Unterschied zu herkömmlichen Systemen herausgearbeitet werden.
Während eine DMS®-Basis-Formulierung ohne Zusatz von weiteren Wirkstoffen
die Lipidbarriere stärkte, hatten hochwertige Moisturizing-O/W-Produkte in
Langzeit einen schädigenden Effekt auf die Lipidbarriere. Dies ist vermutlich
primär auf die Revesikulierungs-Kapazität der Emulgatoren zurückzuführen
(Wash-out effect). DMS®-Formulierungen scheinen die Lipidbarriere durch eine
Art Mosaikmodulation zu stärken. Gestörte Barrierestellen werden restrukturiert.
Seit mehreren Jahren befinden sich Produkte im Markt (z.B. Physiogel Creme
der Fa. Stiefel Laboratorium GmbH), welche zeigen, dass Theorie und Praxis übereinstimmen.
Gerade im Bereich der sensitiven, geschädigten Haut sind die größten
Erfolge erkennbar.
| Foto: Gesellschaft für Dermopharmazie |
| Foto: Gesellschaft für Dermopharmazie |


Prof. Dr. Claudia
Valenta
Entwicklung neuer Konservierungsstoffe auf Peptid-
und Polypeptid-Basis
Institut für Pharmazeutische Technologie und Biopharmazie der Universität Wien
Die Konservierung topischer Arzneimittel (Salben, Cremes, Gele)
kann in der Praxis zu Problemen wie z.B. erhöhtes Allergisierungsrisiko oder
zu Unverträglichkeiten führen (1, 2). Um einen mikrobiellen Verderb
zu verhindern, muss eine Zubereitung hygienisch einwandfrei hergestellt und bei
Bedarf antimikrobiell behandelt werden. Der Zusatz eines geeigneten Konservierungsmittels
(KM) soll eine mikrobielle Kontamination während der Verwendung ausschließen.
In früheren Arbeiten wurde bereits darauf hingewiesen, dass durch das zusätzliche
Verdünnen von an sich ausreichend konservierten Salbengrundlagen ihre mikrobielle
Stabilität nicht mehr gewährleistet ist (3, 4) und daher in diesem Fall
der Apotheker verpflichtet ist, das KM zu ergänzen. Ein KM für Dermatika
sollte folgende Forderungen erfüllen (5): Es sollte ein breites Wirkungsspektrum
haben, nicht toxisch, nicht irritierend, nicht allergisierend sein, einen guten
Verteilungskoeffizienten besitzen, so dass eine ausreichend hohe Konzentration
in der Wasserphase vorliegt, über einen breiten pH-Bereich stabil sein, mit
den verschiedenen Komponenten des Präparates verträglich sein und die
physischen Eigenschaften wie Aussehen, Geruch und Farbe nicht verändern.
Kein KM besitzt alle diese Eigenschaften, daher muss für jedes Präparat
ein geeignetes oder eine Kombination aus mehreren gefunden werden.
Da
die Zahl der KM für Dermatika eingeschränkt ist (6) und es ein hohes
Allergisierungsrisiko gibt, erscheint es sinnvoll, nach alternativen Konservantien
zu suchen. Mikroorganismen produzieren eine Vielzahl von Verbindungen, um durch
diese andere Mikroorganismen am Wachstum bzw. an ihrer Vermehrung zu hindern.
Bei solchen Verbindungen handelt es sich nicht nur um niedermolekulare Strukturen
wie Antibiotika, sondern auch um höhermolekulare Peptide und Proteine, die
eine ausgezeichnete antibakterielle und/oder antifungale Wirkung aufweisen. Aus
der Gruppe solcher antimikrobiell wirkender Peptide wurde das Lantibiotikum Nisin
als mögliche Alternative zu bekannten KM auf sein Wirkungsspektrum und seine
Stabilität in Dermatika getestet (7).
Jedoch wirken diese Peptide
vorwiegend gegen grampositive Keime und nur eingeschränkt gegen gramnegative
Bakterien, die aber den Hauptteil der abzutötenden Wasserbakterien darstellen.
Eine Möglichkeit, das Wirkungsspektrum zu erweitern ist die Kombination mit
Chelatbildnern. Es konnte z.B. gezeigt werden, dass das Wirkungsspektrum von Nisin
in einem Chitosan-EDTA-Gel auch auf die weitaus problematischeren gramnegativen
Keime ausgedehnt werden kann (8).
Bei der Auswahl von Peptiden für
die Austestung als mögliche KM in topischen Zubereitungen sollen folgende
Kriterien herangezogen werden: Geringe bis keine Toxizität, Mindestmolekularmasse
von 3000 Da, um eine Hautresorption auszuschließen (9) und die Verfügbarkeit
genügend großer Mengen des Reinpeptides. Aufgrund dieser Überlegungen
wurde Lysozym ausgewählt. Lysozym, ein globuläres Peptid mit einer mittleren
Molekularmasse von 14 400 Da, ist gut gegen grampositive Keime wirksam. Die Wirkung
beruht auf einer Spaltung der ß-1,4-glykosidischen Bindungen zwischen N-Acetylmuraminsäure
und N-Acetyl-D-glucosaminresten in Peptidoglykanen wie z.B. dem Murein. Dadurch
kommt es zur Bakteriolyse durch direkten Angriff auf die Zellwand grampositiver
Bakterien. Lysozym wird bereits oral und i.v. gegen bakterielle Infektionen eingesetzt.
Topisch wird es gegen Herpes simplex und Herpes zoster angewendet (10).
Das gegen grampositive Bakterien wirkende Lysozym wurde nun mit Verbindungen,
wie Zimtaldehyd, Kaffee- oder Zimtsäure, die auch gegen gramnegative Bakterien
wirksam sind, kovalent gekoppelt.
In einer erstern Versuchsanordnung wurde
eine reduktive Kopplung (11) von Zimtaldehyd an die freien Aminogruppen der Lysinreste
des Lysozyms vorgenommen; durch diese Modifikation wurde zwar das Wirkungsspektrum
erweitert, bei der Austestung in dermalen Formulierungen als mögliche neue
Konservantien konnte eine Keimzahlverminderung jedoch nicht im geforderten Ausmaß
der Pharmakopoe erreicht werden (12).
Als zweite Reaktion wurde die kovalente
Kopplung von Kaffeesäure bzw. Zimtsäure an Lysozym durch Ausbildung
von Amidbindungen zwischen der Carboxylgruppe des Liganden und einer primären
Aminogruppe am Lysozym durch eine von Carbodiimid vermittelte Reaktion durchgeführt.
Es entstanden neue kovalent gebundene Kaffee- bzw. Zimtsäure/Lysozymkonjugate
(13).
Die Austestung des antimikrobiellen Spektrums wurde für alle Konjugate
mit Staphylococcus aureus (ATCC 6538) als Modellkeim für grampositiv und
mit Escherichia coli (ATCC 8739) als Modellkeim für gramnegativ durchgeführt.
Während bei den Lysozym/Kaffeesäure Konjugaten zwar die Wirkung auf
gramnegative Keime verstärkt werden konnte, kam es zu einer Wirkverminderung
gegen grampositive Keime. Die Lysozym/Zimtsäurekonjugate zeigten keine signifikante
Erweiterung des antimikrobiellen Spektrums.
Um den Verlust der Wirkung gegen
grampositive Keime der Kaffesäurekonjugate wieder auszugleichen, erschien
es sinnvoll, eine Mischung von Lysozym/Kaffeesäurekonjugat mit Lysozym (1+1)
auf ihre antimikrobielle Wirkung auszutesten. Diese Mischung wurde in 3 verschiedenen
dermal angewendeten Hydrogelen auf ihre ausreichende Konservierung gestestet.
In HPMC und Natrium-Chitosan-EDTA-Gelen war eine ausreichende Konservierung gegeben.
Nur in Carbopol-Gelen war diese aufgrund von adsorptiver Bindung an das Polymersystem
behindert (14).
Abschließend kann festgestellt werden, dass es
sich bei Lysozym-Kaffeesäurekonjugaten um interessante neue Konservantien
handelt, deren Penetration durch die Haut aufgrund ihrer hohen Molekülmasse
nahezu auszuschließen ist. Ihre Wirkung hängt jedoch auch vom Vehikel
ab, in dem sie eingesetzt werden. Die antimikrobielle Wirkung sollte daher immer
überprüft werden, da eine Wirkverminderung aufgrund von adsorptiver
Bindung an Vehikelbestandteile nicht auszuschließen ist. Durch neue biotechnologische
Methoden werden immer mehr antimikrobielle Peptide in ausreichendem Ausmaß
zur Verfügung stehen und daher wird ein Einsatz von KM auf Basis von Peptiden/Polypeptiden
immer interessanter werden.
Literatur:
(1) Van Doorne H.: Preservation
of ointments and creams. Deutsche Apotheker Zeitung 125, 800, 1985
(2) Wallhäußer
K.H.: Praxis der Sterilisation Desinfektion-Konservierung 4.Ed.,p. 319, Thieme
Verlag, Stuttgart 1984
(3) Bernkop-Schnürch A., Valenta C., Urban U.:
Mikrobielle Stabilität von magistral hergestellten Dermatika. Sci.Pharm.
63, 65, 1995
(4) Bernkop-Schnürch A. und Valenta C.: Untersuchungen zur
mikrobiellen Stabilität von magistral hergestellten Cremen und Gelen. ÖAZ
49, 926, 1995
(5) Croshaw B.: Preservatives for cosmetics and toiletries.
J.Soc.Cosmet Chemists 28, 3, 1977
(6) Van Ooteghem M.: Gebrauch von Konservierungsmitteln
in Dermatica. Pharmazie 39, 621, 1984
(7) Valenta C., Bernkop-Schnürch
A. und Teltscher Ch.: Nisin, ein potentielles Konservierungsmittel in topischen
Zubereitungen. Pharmazie 51, 119, 1996
(8) Valenta C.; Christen B., Bernkop-Schnürch
A.: Chitosan-EDTA Conjugate: A Novel Polymer for Topical used Gels. J.Pharm.Pharmacol.
50, 1-8, 1998
(9) Bernkop-Schnürch A., Valenta C., Gatterwe V.: In vitro-skin
permeation of the lantibiotic nisin. Eur.J.Pharm.Biopharm. 42, 336, 1996
(10)
Morant J., Ruppaner H., (Ed): Arzneimittelkompendium Schweiz, Documed Basel 1995
(11) Means, G.E., Feeny, R. E.: Reductive Alkylation of Proteins. Analytical Biochemistry.
224, 1-16, 1995
(12) Valenta C., Bernkop-Schnürch A., Schwartz M.: Modification
of lysozyme with cinnamaldehyde: A strategy for constructing novel preservatives
for dermatics. Int.J.Pharm. 148, 131-137, 1997
(13) Bernkop-Schnürch
A., Krist S., Vehabovic M., Valenta C.: Synthesis and Evaluation of lysozyme derivatives
exhibiting an enhanced antimicrobial action. Eur.J.Pharm.Sci. 6, 301-306, 1998
(14) Valenta C., Schwarz E., Bernkop-Schnürch A.: Lysozyme-Caffeic acid
conjugates: Possible novel preservatives for dermal formulations. Int.J.Pharm.
174, 125-132, 1998
| Foto: Gesellschaft für Dermopharmazie |

Priv.-Doz. Dr. med.
Klaus-P. Wilhelm
Experimentelle Absicherung von Wirkansprüchen
bei Kosmetika
proDERM
Institut für Angewandte Dermatologische Forschung GmbH, Schenefeld
Kosmetika sind zur Reinigung und Pflege der Haut bestimmt. Die häufig
gestellte Frage ‚dürfen Kosmetika wirken?‘ kann eindeutig mit ‚ja‘ beantwortet
werden.
Moderne Kosmetik verfügt über vielfältige Wirkungen.
Sofern diese Wirkungen werblich für das Produkt genutzt werden, müssen
diese durch geeignete Untersuchungen nachgewiesen werden. Wenngleich manche heute
gemachten blumigen Auslobungen jeder wissenschaftlichen Grundlage entbehren, gibt
es für zahlreiche Wirkungen von Kosmetika geeignete Untersuchungsverfahren
zur wissenschaftlichen Absicherung.
Zu diesen nachweisbaren Wirkversprechen
gehören u. a.:
Priv.-Doz. Dr. med. Klaus-P. Wilhelm
| Foto: Gesellschaft für Dermopharmazie |

Dr. med. Frank Rippke
Freie Radikale und Hautalterung:
Relevanz
des täglichen antioxidativen Lichtschutzes
Beiersdorf AG, Hamburg
UV-Exposition kann an der menschlichen
Haut zu einer Reihe akuter und chronischer Schäden wie Sonnenbrand, Photodermatosen
und vorzeitiger Hautalterung führen, bei denen die Bildung freier Radikale
eine wichtige Rolle spielt. Diese hochreaktiven Sauerstoffspezies sind für
eine direkte Schädigung von Lipiden, Proteinen und DNS ebenso verantwortlich
wie für die Störung intrazellulärer Signaltransduktionswege. Da
auch suberythematogene UV-Dosen bereits die Bildung freier Radikale induzieren
und den endogenen Antioxidantienpool signifikant vermindern können (1), finden
Radikal-fangende Antioxidantien zunehmende Verwendung als aktive Wirkstoffe sowohl
in Sonnenschutzmitteln als auch Gesichtspflegeprodukten für den täglichen
Lichtschutz.
Zahlreiche antioxidative Substanzen werden seit Jahren in
Hautpflegeformulierungen zum Schutz der Haut vor oxidativen Schäden verwendet,
insbesondere Ester der Vitamine E und C sowie Betacarotin. Erst vor kurzem haben
sich die Flavonoide, eine Familie chemischer Substanzen botanischer Herkunft mit
ausgeprägten antioxidativen Eigenschaften, als effektive kosmetische Wirkstoffe
herausgestellt; so haben bestimmte Extrakte des Grünen Tees einige wissenschaftliche
und öffentliche Aufmerksamkeit erregt. Für eine definierte Monosubstanz,
alpha-Glucosylrutin (AGR), wurde eine extrem hohe antioxidative Wirksamkeit in
Screeningstudien unter Verwendung einer neuen Chemilumineszenz-Methode, der In-vivo-Radikaldetektion,
ermittelt (2). Die Substanz, die aus den Blättern des Pagodenbaumes gewonnen
und durch enzymatische Glykolisierung in ihrer Wasserlöslichkeit gesteigert
wird, zeigte in Ex-vivo-Studien auch eine unterstützende Wirkung auf den
endogenen Antioxidantienpool (3).
Zusammenfassend stellen die Flavonoide
und insbesondere AGR eine vielversprechende neue Wirkstoffgruppe für dermatologische
Hautpflegemittel mit nachgewiesener Schutzwirkung gegenüber UV-induzierten
Hautschäden und einem bedeutenden Potential in der Prävention der vorzeitigen
Hautalterung dar.
Literatur:
(1) Podda M., Traber M.G., Weber
C., Yan L.-J., Packer L.: UV-irradiation depletes antioxidants and causes oxidative
damage in a model of human skin. Free Rad. Biol. Med. 24, 55-65, 1998
(2)
Stäb F., Lanzendörfer G., Schönrock U., Wenck H. : Novel antioxidants:
new strategies in product stabilization and skin protection. SÖFW-Journal
10, 604-613, 1998
(3) Stäb F., Wolber R., Mundt C., Blatt T., Will K.,
Keyhani R., Rippke F., Max U., Schönrock H., Wenck H., Moll I., Hölzle
E., Wittern K.-P.: Alpha-Glucosylrutin – an innovative antioxidant in skin protection.
SÖFW-Journal 9, 2-8, 2001
|
Foto: Gesellschaft für Dermopharmazie |

Dr. med. Dipl. Chem.
Lothar W. Weber
Hautlipide:
Regeneration
nach Applikation von antiseptischen Handwaschlösungen
Institut
für Arbeits-, Sozial- und Umweltmedizin, Universitätsklinikum Ulm
Einleitung
Eine der primären
Funktionen der Haut ist die Abwehr von äußeren Noxen. Die äußerste
Barriere bildet dabei ein Hydrolipidfilm, der in einer Emulsion von Schweiß,
Hauttalg sowie Abbauprodukten aller Hornschichtanteile besteht. Die Abwehrkraft
dieses Films ist wegen zu geringer Barrierewirkung und nicht konstanter Pufferkapazität
verhältnismäßig gering. Die Schutzfunktion der Haut selbst ist
abhängig von ihrer Lokalisation, ihrem Alter, der Konzentration der vorhandenen
Lipide und dem Gehalt von wasserbindenden Anteilen in der Hornschicht.
Ein häufiges Waschen – insbesondere der Hände – bewirkt eine Extraktion
der natürlichen Schutzschicht. Dies gilt auch für die Verwendung flüssiger
Händedesinfektionsmittel. Sie enthalten für ihre biologische, keimtötende
Wirkung einen oder mehrere niedere Alkohole in höheren Konzentrationen. Um
den Hydrolipidfilm nach mehrmaligem Händewaschen nach Kontakt mit potentiell
infektiösem Patientenmaterial oder Schmutz zu erhalten bzw. wieder aufzubauen,
werden den Produkten rückfettende Begleitstoffe in geringen Mengen zugegeben.
Zusätzlich können Spuren von schwer flüchtigen Bestandteilen mit
desinfizierender Wirkung, Geruchsstoffe sowie mehrwertige Alkohole enthalten sein.
Beim Händewaschen werden bevorzugt hydrophile Stoffe, intercorneales Material
sowie ablösbare Hornschuppen mit der Waschlösung weggespült. Standardisierte
Methoden, mit denen diese komplexen Wechselwirkungen in der äußersten
Hautbarriere der Hände zu suchen sind, finden sich bislang nicht in der Literatur.
Methode
Um oberflächenaktive Komponenten in der Abwaschlösung
zu bestimmen, wird der physikalische Parameter Oberflächenspannung nach standardisierten,
okklusiven Abwaschversuchen an hautgesunden Probanden herangezogen. Somit kann
der Einfluss von Desinfektionsmitteln und deren Komponenten auf die Hautoberfläche
der Hände nach einmaliger und wiederholter Anwendung untersucht werden.
Reines Wasser besitzt als Waschmedium bei 30 °C, entspricht der Hauttemperatur,
eine herausragend hohe Oberflächenspannung von 71,1 mN/m. Niedere Alkohole,
wasserlösliche Rückfetter, natürliche Emulgatoren, Tensidspuren
sowie Geruchsstoffe können bereits in geringen Mengen die Oberflächenspannung
des Wassers um 10 – 20 mN/m senken. Wiederholte Waschungen einer normal gesunden,
unbehandelten Haut ergeben jedoch nur eine geringe Reduktion der Oberflächenspannung
des benutzten Wassers (0,6 – 1,6 mN/m).
Ergebnisse
Alkoholische
Händedesinfektionsmittel werden bis zur Trockenheit in die Hände eingerieben.
5, 10 und 15 Minuten später ergeben die nachfolgenden Wasserwaschungen für
das jeweilige Händedesinfektionsmittel spezifische, gleichbleibende Oberflächenspannungswerte.
Die reproduzierbare Oberflächenspannung in Waschlösungen mit unterschiedlicher
zeitlicher Distanz zur flüssigen Händedesinfektion zeigt, dass Alkoholreste
bereits 5 Minuten nach Beginn der Desinfektion keinen Einfluss auf die Oberflächenspannung
der Waschlösung haben. Bei aufeinanderfolgenden Abwaschungen, 5 min, 15 min,
30 min und 60 min nach Desinfektionsbeginn, zeigt die erste Abwaschflüssigkeit
jeweils die stärkste Erniedrigung der Oberflächenspannung, mit Abstand
gefolgt von der zweiten Abwaschflüssigkeit, usw. Spätere Abwaschungen
nähern sich bzw. erreichen die Werte des Kontrollkollektivs.
Rückfettende
Substanzen in Verdünnungsreihen bzw. aus Verdunstungsrückständen
beeinflussen unterschiedlich stark die Oberflächenspannung von Wasser. Werden
diese Referenzwerte mit den Messwerten aus In-vivo-Abwaschungen verglichen, lässt
sich die Elutionsrate des Rückfetters aus den gemessenen Oberflächenspannungen
ermitteln. Bei einigen Desinfektionsmitteln konnte eine Elutionsrate der Rückfetter
in der ersten Abwaschlösung zwischen 22 % und 41 % bestimmt werden, d.h.
ein Teil der eingesetzten Rückfetterkombinationen verbleibt in der Haut und
unterstützt damit die Hautlipidfunktion und den Hydrolipidfilm wirkungsvoll.
Schlussfolgerung
Die standardisierte Messung der Oberflächenspannung
von Wasser in entsprechenden In-vitro- und In-vivo-Prüfanordnungen erlaubt
es, hautschonende Eigenschaften von Händedesinfektionsmitteln auch nach wiederholtem
Gebrauch praxisnah zu definieren und möglichen Optimierungsbedarf für
die Beeinflussung der Hautlipide an der äußersten Grenzfläche
darzustellen.
| Foto: Gesellschaft für Dermopharmazie |

Dr. Karen Reimer
Indikationen herkömmlicher und neuartiger Zubereitungen
mit Povidon-Iod
Mundipharma GmbH, Limburg
Das mikrobizide Wirkspektrum von Povidon
(PVP) -Iod ist umfassend – auch nach kurzen Einwirkzeiten. Resistenzentwicklung
gibt es im Unterschied zu Lokalantibiotika und anderen antiseptischen Wirkstoffen
nicht. Von besonderer Bedeutung ist die hohe Effizienz gegenüber hochresistenten
grampositiven Erregern (z.B. MRSA), gegenüber Chlamydien und Sprosspilzen
ebenso wie die antivirale Aktivität gegen Herpes-, Adeno-, Entero- und HI-Viren.
So ergeben sich neben den klassischen Anwendungsgebieten, wie Haut und
Händedesinfektion, Schleimhautantiseptik und Wundbehandlung, auch nutzbringende
Indikationen des Wirkstoffes zur Körperhöhlenspülung, zur Anwendung
am Auge und nicht zuletzt auch zur postexpositionellen Prophylaxe bei Kontamination
mit infektiösem Material.
Eine pharmazeutische Innovation unter
Verwendung von PVP-Iod ist die Entwicklung eines liposomalen Komplexes. Die Wassertransportfunktion,
die gute Verträglichkeit und die gezielte topische Aktivität der Liposomen
sind mit der mikrobiziden Effektivität des antiseptischen Wirkstoffes so
verbunden, dass auf neuartige Weise die beiden Aspekte Infektionsverhütung
und Förderung der Gewebereparatur erfüllt werden. Eine Reihe von präklinischen
Daten, Tierversuchen und klinischen Untersuchungen bestätigt dies.
Die direkte Wundheilungsförderung durch die Verwendung des PVP-Iod-Liposomenkomplexes
in einer Hydrogelformulierung ermöglicht eine verbesserte Wundbehandlung
bei akuten wie chronischen Defekten.
|
Foto: Gesellschaft für Dermopharmazie |

Prof. Dr. Christel
Mueller-Goymann
Liberation und Permeation von Hydrocortison
aus Arzneibuchgrundlagen
Institut für Pharmazeutische Technologie der TU Braunschweig
Hydrocortison
wurde in verschiedene Grundlagen des Deutschen Arzneibuchs eingearbeitet: Hydrophile
Salbe (HS), Wasserhaltige Hydrophile Salbe (WHS), Wollwachsalkoholsalbe (WS),
Wasserhaltige Wollwachsalkoholsalbe (WWS) und Nichtionische Hydrophile Creme (NHC).
Je nach Affinität des Hydrocortisons zur jeweiligen Grundlage variierte die
Sättigungslöslichkeit des Arzneistoffs von 0,0012 % in WS bis 0,012
% in WHS und NHC (1). Damit resultierten bei einer eingearbeiteten Hydrocortison-Konzentration
von 1 % in allen Fällen Suspensionszubereitungen.
Auf ärztliche
Verordnung erfolgt häufig eine rezepturmäßige Verdünnung
von Corticosteroid-Zubereitungen. Daher wurden 1%ige Hydrocortison-Zubereitungen
in WHS, einer Creme des Typs O/W, außerdem in den Verhältnissen 1:1,
1:2 und 1:3 mit allen genannten Arzneibuchgrundlagen verdünnt. Die Beeinflussung
der Sättigungslöslichkeit des Arzneistoffs durch die Verdünnung
mit Grundlagen, die wasserfrei sind bzw. dem Typ W/O angehören, korrelierte
mit der Freigabegeschwindigkeit des Arzneistoffs aus der resultierenden Formulierung
(1). Je höher die Sättigungslöslichkeit des Hydrocortisons in der
Grundlage war, umso größer war die Liberationsgeschwindigkeit. Allerdings
wirkte sich eine unterschiedliche Liberationsgeschwindigkeit nicht auf die Hydrocortison-Permeation
durch exzidiertes humanes Stratum corneum (EHSC) aus, da die Permeationsgeschwindigkeit
als langsamster Schritt geschwindigkeitsbestimmend war (2). Eine Modifizierung
der Permeation im Zuge rezepturmäßiger Verdünnung von Formulierungen
war nur erfolgreich, wenn unterschiedliche Konzentrationen von Penetrationsförderern
eingearbeitet waren (2).
(1) Refai H., Mueller-Goymann C.C.: Larvated
incompatibilities of hydrocortisone cream preparations upon dilution with different
cream bases. Pharmazie 54, 754-758, 1999
(2) Mueller-Goymann C.C., Refai H.:
Dermale Rezeptur – Tuecken im Apothekenlabor. Pharm. Ztg. 145, 3025-3030, (2000)
Prof. Dr. Christel Mueller-Goymann
|
Foto: Gesellschaft für Dermopharmazie |

Prof. Dr. Rainer
H. Müller*
Nanostrukturierte Lipidcarrier (NLC):
Die
neue Generation der Lipid-Nanopartikel für dermale Anwendungen
PharmaSol GmbH, Berlin
Liposomen wurden 1986 als Träger in topischen Formulierungen
von dem Kosmetikhersteller Dior eingeführt. Das Produkt hieß „Capture“
und wurde als „der Sieg der Wissenschaft über die Zeit“ angekündigt.
Es dauerte dann noch ein halbes Jahrzehnt bis die ersten pharmazeutischen Produkte
auf der Basis von Liposomen auf den Markt kamen. Kein anderes neues topisches
Trägersystem fand so eine breite Anwendung im pharmazeutischen und insbesondere
kosmetischen Bereich, weder die multiplen Emulsionen (z. B. in kosmetischen Produkten
von Beiersdorf) noch die Mikroemulsionen (z. B. in Contrafugin®). Besonders
in der Öffentlichkeit wurde keinem anderen Trägersystem so viel Aufmerksamkeit
geschenkt. Der Ausdruck Liposom ist oder war vielen Kunden ein Begriff (natürlich
ohne genaueres Wissen darüber, worum es sich dabei handelt). Kurz: Liposomen
können – insbesondere auf dem kosmetischen Sektor – als Erfolgsgeschichte
bezeichnet werden. Seit der Einführung von Liposomen Mitte der 80er konnte
jedoch kein anderes neues Trägersystem einen ähnlichen Erfolg verzeichnen.
Es besteht also definitiv Bedarf für die Entwicklung eines neuen Systems.
Zu Beginn der 90er wurden die festen Lipid-Nanopartikel (SLN) entwickelt.
Die Herstellung erfolgte in unserer Arbeitsgruppe mit Hilfe der Hochdruckhomogenisation,
die Gruppe um Gasco in Turin/Italien verwendete eine Mikroemulsionstechnik. Im
Grunde sind SLN ein attraktiver Träger für Topika. Sie bestehen aus
gut verträglichen, akzeptierten Inhaltsstoffen, die aus dem Bereich der Emulsionen
und Liposomen bekannt sind. Gleichzeitig haben sie im Unterschied zu Emulsionen
und Liposomen eine feste Matrix, die den Schutz von chemisch labilen Stoffen ermöglicht
und eine Abwandlung der Freisetzung erlaubt. Innerhalb eines halben Jahrzehnts
begannen Arbeitsgruppen weltweit mit der Forschung an diesem System, hauptsächlich
jedoch auf pharmazeutischem Gebiet. Trotz ihrer Vorteile sind mit SLN jedoch einige
Einschränkungen verbunden, vor allem:
| Foto: Gesellschaft für Dermopharmazie |

Univ.-Prof. Dr. med.
Jean Krutmann
Neue Entwicklungen im Sonnenschutz: Actives
Direktor des
Institutes für Umweltmedizinische Forschung (IUF)
an der Heinrich-Heine-Universität
gGmbH, Düsseldorf
Aufgrund geänderter Lebensgewohnheiten
(z.B. zunehmende Freizeit, Urlaub in sonnenreichen Gegenden) wird es immer wichtiger,
die molekularen und photobiologischen Wirkungen zu untersuchen, die ultraviolette
Strahlung auf die menschliche Haut auszuüben vermag. Die hierbei gewonnenen
Informationen sind von eminenter Bedeutung für die Entwicklung wirksamer
Sonnenschutzstrategien. Neben der ständigen qualitativen Verbesserung klassischer,
UV-Filter-haltiger Sonnenschutzpräparate kommt der Entwicklung von Kombinationspräparaten,
die so genannte „Actives“ oder aktive Moleküle beinhalten, eine
stetig größer werdende Bedeutung zu. Diese „Actives“ können
in Kombination oder zusätzlich zu UV-Filtern eingesetzt werden, um eine bessere
Photoprotektion der menschlichen Haut zu erzielen. An Hand von zwei Beispielen
wird diese Entwicklung illustriert werden: (i) dem Einsatz von topisch applizierbaren
DNS-Reparatur-Enzymen zum Schutz der menschlichen Haut gegen UVB-induzierte Schäden
sowie (ii) der Entwicklung eines neuartigen Testsystems zum Nachweis mitochondrialer
DNS-Mutationen, das es erlaubt, die Wirksamkeit von „Actives“ beim Schutz
der menschlichen Haut gegenüber der Lichtalterung(= dem Photoaging) zu untersuchen
und neue „Actives“ zu entwickeln.
Literatur:
(1)
Stege H., Roza L., Vink A.A. et al: Enzyme plus light therapy to repair DNA damage
in ultraviolet-B-irradiated human skin. Proc Natl Acad Sci USA , 97, 1790-1795,
2000.
(2) Berneburg M., Plettenberg H., Krutmann J.: Photaging of human skin.
Photodermatol Photoimmunol Photomed 16, 239-244, 2000
(3) Berneburg M., Grether-Beck
S., Kürten V. et al: Singlet oxygen mediates the UVA-induced generation of
the photoaging-associated common deletion . J Biol Chem 274, 15345-15349, 1999
|
Foto: Gesellschaft für Dermopharmazie
|

Dr. Beate Hirrlinger,
Qualitätsrisiken von dermopharmazeutischen Ausgangsstoffen:
Erythromycin als Beispiel
Aug. Hedinger GmbH & Co. KG, Stuttgart
1998 mussten
Chargen von Erythromycin-Rezeptursubstanz zurückgerufen werden, da sie durch
Lösungsmittelrückstände verunreinigt waren.
Alle diese Chargen
waren mit Prüfzertifikaten in den Handel gekommen, welche die Arzneibuchkonformität
des Erythromycins bescheinigten. Auf diese Zertifikate muss sich der Apotheker
verlassen, da im Allgemeinen eine niedergelassene Apotheke nicht über die
analytischen Möglichkeiten zum Nachweis solcher Verunreinigungen verfügt.
Diese Rückrufe verdeutlichen die Bedeutung, die eine geschlossene GMP-Kette
für die Qualität eines Ausgangsstoffes besitzt. Diese Kette beginnt
bei der Synthese eines Ausgangsstoffs und muss sich bis zu Handel, Konfektionierung
und Vertrieb in die Apotheken erstrecken. Prüfzertifikate, hinter denen keine
solche geschlossene Kette steht, können die Qualität eines Ausgangsstoffes
nicht garantieren.


Dr. Ulrich Schäfer
Untersuchungen
zur Dermatopharmakokinetik
ex vivo und in vivo
unter Berücksichtigung von Hautäquivalenten
Universität des Saarlandes, Saarbrücken
In zunehmendem Maße
gewinnt die dermale und transdermale Applikation von Arzneistoffen an Bedeutung.
Aus ökonomischen Gründen ist es dabei wünschenswert, zur Überprüfung
der Machbarkeit und zur schnelleren Produktentwicklung In-vitro- Testsysteme zur
Verfügung zu haben. Eine der Voraussetzungen für den Einsatz solcher
Systeme ist jedoch eine In-vitro-/In-vivo-Korrelation.
Bei den vorgestellten
In-vitro-Versuchen wurde entweder die Franz-Zelle (FD-C) oder das Saarbrücker
Penetrationsmodell (SB-M) benutzt. Als Modellarzneistoff wurde Flufenaminsäure
in verschiedenen Präparationen eingesetzt. Die Menge an Arzneistoff im Stratum
corneum war bei beiden Modellen annähernd gleich. Für in vitro / in
vivo konnte für diese Testsysteme eine lineare Korrelation aufgestellt werden
(Tabelle 1a). Mittels eines spezielles Versuchsdesigns, bei dem die Haut des gleichen
Probanden benutzt wurde, konnte der Arzneistofftransport in die tieferen Hautschichten
sowohl in vitro als auch in vivo bestimmt werden. Hier ergab sich ebenfalls eine
In-vitro-/In-vivo- Korrelation (Tabelle 1b).
Für rekonstruierte Hautäquivalente
wird deren Barrierefunktion und die Lot-Lot-Variabilität gezeigt. Des Weiteren
war es möglich, die Flux-Daten der rekonstruierten Hautäquivalente mit
den Flux-Daten von hitzeseparierter Epidermis zu korrelieren.
Um die gefundenen
Korrelationen verallgemeinern zu können, müssen Experimente mit weiteren
Arzneistoffen und Formulierungen durchgeführt werden.
| Tabelle 1: In-vitro/In-vivo-Korrelation | |||
| Regressionsgleichungen mit m = Flufenaminsäure-Menge (ng/cm²) | |||
| a) Stratum corneum: | |||
| FD-C vs. in vivo: | min-vitro = 4,5 x min-vivo – 4578 | r = 0,990 | Proband (1) |
| min-vitro = 7,4 x min-vivo – 7998 | r = 0,892 | Proband (2) | |
| SB-M vs. in vivo: | min-vitro = 1,8 x min-vivo – 596 | r = 0,999 | Proband (1) |
| min-vitro = 2,1 x min-vivo – 946 | r = 0,959 | Proband (2) | |
| b) Tiefere Hautschichten: | |||
| FD-C vs. in vivo: | min-vitro = 1,78 x min-vivo – 300 | r = 0,927 | |
| SB-M vs. in vivo: | min-vitro = 3,23 x min-vivo + 70 | r = 0,909 | |
| Foto: Gesellschaft für Dermopharmazie |
| Foto: Gesellschaft für Dermopharmazie |


Dr. Karl-Heinz Nietsch
Wirksamkeit von Ciclopirox beim seborrhoischen Ekzem
Aventis Pharma Deutschland GmbH, Product Group Dermatology, Bad Soden
Seit der
ersten Beschreibung des seborrhoischen Ekzems durch Unna wurde den massenhaft
auf der Hautoberfläche vorkommenden lipohilen Hefen eine wichtige Rolle in
der Entstehung und der Aufrechterhaltung dieser Erkrankung zugeschrieben. Nach
heutiger Vorstellung wird eine Entzündungsreaktion auf Pityrosporum ovale
als direkte Ursache für das Auftreten der seborrhoischen Dermatitis diskutiert.
Es gibt widersprüchliche Daten, ob es sich um eine toxische oder eine immunologische
Reaktion handelt: Auf der einen Seite produzieren Pityrosporum Hefen eine Reihe
von potentiellen Irritantien, auf der anderen Seite können abgetötete
Organismen der seborrhoischen Dermatitis ähnliche Hautveränderungen
induzieren. Da die Erkrankung bei Patienten mit HIV-Infektionen häufiger
vorkommt, werden Schwächungen des Immunsystems als weiterer möglicher
pathogenetischer Faktor diskutiert.
Eine Behandlung des seborrhoischen
Ekzems mit Antimykotika senkt die Anzahl der lebensfähigen Pilzelemente und
vermindert parallel hierzu die klinischen Zeichen der Irritation. In verschiedenen
klinischen Studien wurde die Wirksamkeit von Azol-Antimykotika bei der Behandlung
des seborrhoischen Ekzems demonstriert. Für das Hydroxipyridon Ciclopirox
lagen bis heute keine kontrollierten Untersuchungen in dieser Indikation vor.
Deshalb wurde eine Reihe von Studien mit verschiedenen Zubereitungsformen (Gel,
Creme, Shampoo) eingeleitet. Im Folgenden wird über die Ergebnisse von zwei
ähnlichen Studien mit der Cremezubereitung berichtet.
Die Studien
wurden als doppelblinde, randomisierte Parallelgruppenvergleiche konzipiert und
in fünf Zentren in Deutschland und 14 Zentren in Australien bzw. Neuseeland
durchgeführt. In Studie 1 nahmen 165 Patienten und in Studie 2 189 Patienten
mit klinisch diagnostiziertem seborroischem Ekzem des Gesichts teil. Jeder Patient
applizierte Ciclopirox 1 % Creme, Ketoconazol 2 % Creme oder das korrespondierende
Vehikel zu Ciclopirox Creme einmal täglich (Studie 1) oder zweimal täglich
(Studie 2) in einem dünnen Film über einen Zeitraum von 4 Wochen auf
die betroffenen Hautareale. Gleichzeitige Anwendung von Glukokortikoiden, Antimykotika,
Antihistaminika oder Teerpräparaten war nicht erlaubt. In Studie 1 wurde
die Responderrate, definiert als „abgeheilt“ oder deutliche Verbesserung
des Ausmaßes der Ausbreitung und des Schweregrades der Erkrankung am Ende
der Behandlung, als Primärvariable gewählt. In Studie 2 wurde der Schweregrades
des Krankheitsbildes mit einem globaler Severity Score (4-Punkt Score) ermittelt.
Als Behandlungserfolg (Primärvariable) wurde der Rückgang im globalen
Severity Score um mindestens eine Kategorie definiert. In beiden Studien wurden
die typischen Symptome (Juckreiz, Brennen, Entzündungszeichen und Schuppung)
zusätzlich einzeln mit einem 4-Punkt-Sore bewertet. Kontrolluntersuchungen
wurden wöchentlich durchgeführt. Am Ende der Behandlung wurden Verträglichkeit
und kosmetische Akzeptanz von Prüfarzt und Patient gesondert bewertet.
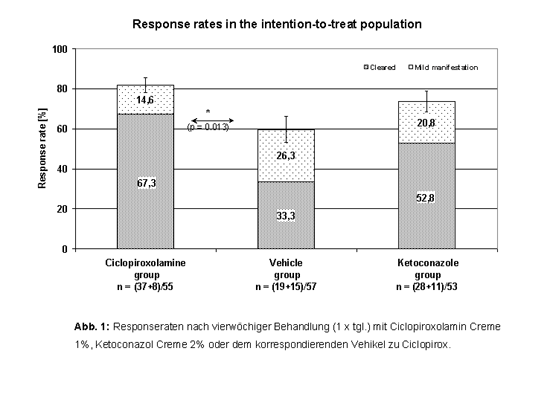
Ergebnisse: Die Responserate (ITT- Population) betrug in Studie 1 81,8 %
in der Ciclopiroxgruppe und 59.6 % in der Vehikelgruppe. Das Ergebnis war statistisch
signifikant (p = 0,013 – Fisher’s Exact Test) Die Responserate für Ketokonazol
betrug 73,6 %. Statitstisch war kein Unterschied zwischen Ciclopirox und Ketokonazol
zu finden (Abb. 1). Eine deskriptive Auswertung, in der „Abheilung“
als Kriterium für Response definiert, ergab folgendes Ergebnis: In der Ciclopiroxgruppe
betrug die Responserate 67,3 % , in der Vehikelgruppe 33,3 %. Dieser Unterschied
war statistisch signifikant (p = 0,0006). Die Responserate für Ketokonazol
betrug 52,8 % (p = 0,0536). Studie 2 ergab ähnliche Ergebnisse. Die Rate
für „Treatment Success“ betrug 73,9 % in der Ciclopiroxgruppe und
53,6 % in der Vehikelgruppe. Dieses Ergebnis war ebenfalls statistisch signifikant
(p = 0,003 – Mantel-Haenszel Test). Nebenwirkungen, die mit der Studienmedikation
in Zusammenhang standen, waren selten und betrafen ausschließlich Hauterscheinungen
wie Rötung oder Brennen.
Zusammenfassend ist festzustellen, dass
Ciclopirox 1 % Creme wirksam ist bei der Behandlung des seborrhoischen Ekzems
und gut vertragen wird. Dies wurde erstmals in zwei konfirmativen Studien nachgewiesen.
Literatur:
(1) Braun-Falco O., Plewig G., Wolff H.H.: Dermatologie
und Venerologie. 4. Aufl. Springer, Berlin, Heidelberg, 1996
(2) McGrath J.,
Murphy G.M.: The control of seborrhoeic dermatitis and dandruff by antipityrosporal
drugs. Drugs 41 (2), 178-184, 1991
(3) Hay R.J., Graham-Brown R.A.: Dandruff
and seborrhoeic dermatitis: causes and management. Clin Exp Dermatol 22 (1), 3-6,
1997
(4) Peter R.U., Korting H.C.: Treatment of seborrhoeic dermatitis with
ketoconazole as compared to a bland cream [in German]. Arzneimittelforschung 41
(8), 852-854, 1991
(5) Zienicke H., Korting H.C., Braun-Falco O. et al.: Comparative
efficacy and safety of bifonazole 1% cream and the corresponding base preparation
in the treatment of seborrhoeic dermatitis. Mycoses 36 (9-10), 325-331, 1993
(6) Nenoff P., Haustein U.F.: Effect of anti-seborrhea substances against Pityrosporum
ovale in vitro [in German]. Hautarzt 45 (7), 464-467, 1994
(7) Korting H.C.,
Grundmann-Kollmann M.: The hydroxypyridones: a class of antimycotics of its own.
Mycoses 40 (7-8), 243-247, 1997
|
Foto: Gesellschaft für Dermopharmazie |
| Foto: Gesellschaft für Dermopharmazie |


Prof. Dr. med. Roland
Niedner
Zulassungsrelevante Probleme bei Dermatika
Klinik für Dermatologie am Klinikum Ernst von Bergmann, Potsdam
Wenn ein neues
Dermatikum zugelassen werden soll oder sich der Wirkstoff oder die Formulierung
geändert hat, müssen ein Nachweis zur Wirksamkeit und Verträglichkeit
sowie gegebenenfalls Daten zur Dosisfindung erbracht werden. Die Prüfung
der Verträglichkeit erfolgt immer mit der Originalformulierung. Parallel
dazu müssen Kontrollen mitlaufen, sowohl mit dem Referenzprodukt als auch
mit der Grundlage. Eine Verträglichkeits-Testung wird mit dem klassischen
Irritationspatchtest vorgenommen. Die Auswertung kann durch Ermittlung des Primären
Irritations Index (PII) gemäß ISO 10993-10 vorgenommen werden, der
eine Zuordnung der Verträglichkeit in bestimmte Kategorien erlaubt. Darüber
hinaus kann auch die Notwendigkeit bestehen, das Sensibilisierungspotenzial an
Meerschweinchen zu bestimmen, auch muss u.U. die Photosicherheit nachgewiesen
werden durch entsprechende Phototirriations- oder Photoallergen-Testungen.
Wenn Äquivalenz zu einem schon bekannten Präparat nachzuweisen
ist, reicht es nicht aus, nur die Unterschiede zum Placebo heraus zu arbeiten,
man muss vielmehr entsprechende Untersuchungen zu Bioverfügbarkeit/Bioäquivalenz
durchführen, mit Ermittlung von Daten zur Pharmakodynamik und Pharmakokinetik,
mit vergleichenden klinischen Studien und gegebenenfalls auch mit In-vitro-Studien.
Dermatopharmakokinetische Untersuchungen werden ergänzt durch den Nachweis
der Arzneimittelliberation aus dem Externum, der Penetration durch und Aufnahme
in die Haut, durch die Bestimmung der Konzentration in ihrem zeitlichen Ablauf
und den steady state level. Auch die Messung der Arzneimittelelimination aus dem
Stratum corneum kann notwendig werden.
Besonderheiten liegen beim Wirksamkeitsnachweis
zur Wundheilung vor, da hier zum einen die Verbesserung der Wundheilung, zum andern
die Verbesserung der Wundbehandlung zu bestimmen ist. Dies erfolgt durch Messung
der Zeit bis zum kompletten Wundverschluss. Eine nur partielle Wundheilung reicht
nicht zum Wirksamkeitsnachweis aus, sondern dient lediglich seiner Unterstützung.
Messparameter zum Verfolg des Wundheilungsprozesses wären die Wundinfektion,
das Debridement sowie der Schmerz zur Überprüfung der Wundsicherheit.
Es existiert eine Vielzahl von Wundmodellen, wobei die epidermale Wundheilung
im Cantharidin-Wundmodell verfolgt werden kann, die subepidermale Wundheilung
im Saugblasenmodell nach Kiistala, epidermale/subepidermale Wunden durch Spalthautentnahme
und schließlich die alle Schichten durchsetzende full thickness wound durch
Exzision. Die Messung der jeweiligen Wundgröße kann durch Planimetrie
oder Diametrie vorgenommen werden, neuerdings wird zunehmend auch die Volumetrie
eingesetzt.
Je nach Wirksamkeit und Rezidivfreiheit liegen die
mittleren jährlichen direkten Kosten für die verschiedenen Verfahren
des modernen Bioengineerings zwischen 8.000 und 20.000 Mark Unter verschiedenen
Wirksamkeitsmodellen ist die Transplantation kultivierter autologer Keratinozyten
gegenüber konservativen Verfahren dann kosteneffektiver, wenn die Behandlung
ambulant durchgeführt werden kann und die Rezidivfreiheit diejenige der konservativen
Behandlung signifikant übersteigt. Nach eigenen, präliminären Daten
an 42 Patienten ist dies der Fall. Die Literaturdaten hierzu sind uneinheitlich.
Besonders einfach gelagert ist der Nachweis der Bioäquivalenz von
topischen Kortikoiden, da das Ausmaß der Vasokonstriktion ein direktes Maß
für die Bioverfügbarkeit/Bioäquivalenz ist. Die Datenerfassung
des Vasokonstriktionstestes erfolgt auf sehr akribische Weise. Erforderlich sind
drei Untersuchungsschritte, mit einem Vorversuch zur Ermittlung der ED50, und
der D1- und D2-Dosis, mit der Messung der Kortikoidantwort auf die Referenzsubstanz
bei allen Probanden des Hauptversuches sowie mit dem eigentlichen Hauptversuch
von Prüf- und Referenzsubstanz an 40 bis 60 Probanden. Die Bewertung der
Vasokonstriktion wird ausschließlich chromametrisch vorgenommen, die visuelle
Erfassung wird trotz guter Datenlage wegen der mangelnden Objektivität zunehmend
verlassen. Die ehemals relativ einfach durchzuführende Studie zur Vasokonstriktion
ist zwar mittlerweile ein hochkompliziertes Verfahren geworden, dafür sind
die ermittelten Daten allerdings auch sehr gut reproduzierbar und sicher.
|
Foto: Gesellschaft für Dermopharmazie |
| Foto: Gesellschaft für Dermopharmazie |


Prof. Dr. med. Max
Gloor
Standardisierte
Rezepturen aus dermatologischer Sicht:
Dermatikagrundlagen und Arzneistoffe
Hautklinik am Städt. Klinikum Karlsruhe, Karlsruhe
Standardisierte Rezepturen
sollten grundsätzlich bevorzugt werden gegenüber freien Rezepturen wegen
der geprüften Galenik und der sicheren Stabilität. Freie Rezepturen
sind nur noch in Einzelfällen erforderlich, zumal in den letzten Jahren im
NRF wesentliche Lücken gefüllt wurden. Anliegen des Referates ist es
zu zeigen, welche vor allem neue NRF-Rezepturen von großem praktischen Nutzen
in der Dermatologie sind. Zu nennen ist die lipophile Cremegrundlage NRF 11.104.
Sie stellt eine ideale Rezepturgrundlage für den Neurodermitiker dar wegen
ihres hohen Wassergehaltes, ihrer dementsprechend geringen Okklusion und ihres
W/O-Typs. Abgeleitet von dieser Grundlage finden sich einige hervorragende Rezepturen
im NRF, so die hydrophobe Triclosancreme 2 % NRF 11.122, die lipophile Polidoconalcreme
5 % mit Harnstoff NRF 11.120 und die lipophile Tretinoinsalbe 0,025, 0,05 und
0,1 % NRF 11.123. Triclosan ist ein Antiseptikum, für das es keine Spezialität
gibt, desgleichen ist keine Alternative unter Spezialitäten vorhanden für
die lipophile Tretinoinsalbe NRF 11.123. Besonderen Nutzen kann der Dermatologe
außerdem aus dem umfänglichen Angebot an O/W-Emulsionen aus dem NRF
ziehen, das durch die Übernahme einer Reihe von SR-Rezepturen stark erweitert
wurde. Das Spektrum der angebotenen Emulsionen unterscheidet sich stark bezüglich
des Lipidgehaltes, des Glyceringehaltes und der Konsistenz. Schließlich
wird auch noch auf einige hervorragende andere NRF- Rezepturen eingegangen, für
die es unter Spezialitäten keine Alternative gibt und die die therapeutischen
Möglichkeiten des Dermatologen wesentlich bereichern.
|
Foto: Gesellschaft für Dermopharmazie |

Dipl. Kfm. Apotheker
Thomas Müller-Bohn
Ist
die magistrale Rezeptur pharmakoökonomisch sinnvoll?
Süsel
Ob die magistrale Rezeptur pharmakoökonomisch sinnvoll ist,
hängt davon ab, aus welcher Perspektive sie betrachtet und wie sie eingesetzt
wird. In den meisten deutschen Apotheken werden weniger als 20 Rezepturen pro
Woche hergestellt, was eine rationelle Arbeitsweise unmöglich macht. Eine
durchschnittliche Herstellung dauert 24 Minuten, nur bei weniger als 10,1 Minuten
könnte sie kostendeckend sein. Standardisierung und gezielter Einsatz von
Defekturen sind daher geboten. Über günstige Einkaufspreise würde
dies auch die Rezepturpreise verringern und damit die Kostenträger bzw. Arztbudgets
entlasten. Patienten und Gesellschaft können zudem profitieren, wenn die
Rezeptur gezielt genutzt wird, um Lücken im Fertigarzneimittelprogramm zu
füllen. Pharmazeutischer und ökonomischer Nutzen der Rezeptur hängen
davon ab, wie die Verordner sie nutzen.
Dipl. Kfm.
Apotheker Thomas Müller-Bohn
| Foto: Gesellschaft für Dermopharmazie |

Dr. Ursula Schöffling
Konservieren
mit Verstand: Wann, wie, womit ?
Trier
Die Konservierung mikrobiell anfälliger dermatologischer
Zubereitungen ist als Normalfall anzusehen und kann durch sauberes Arbeiten nicht
ersetzt werden. Die Entscheidung über einen ausreichenden mikrobiellen Schutz
der Zubereitung liegt in der Verantwortung der Apotheke. Abgabemenge und Aufbrauchfrist
sind aufeinander abzustimmen, um über-flüssiges Konservieren zu vermeiden.
Ein ärztlicher Rezeptvermerk „konservierungsstoff-frei“ verbietet
die Konservierung einer Rezepturzubereitung. Abgabemenge und Auf-brauchfrist sind
in Einklang zu bringen.
Aus standardisierten Vorschriften sowie den Hinweisen
und Tabellen des NRF lassen sich praktische Orientierungshilfen für frei
rezeptierte analoge Zubereitungen entnehmen, ein-geschlossen die GD-Hygienerichtlinie
vom 19.01.2000.
Mikrobiell instabil und konservierungsbedürftig
sind wasserhaltige Dermatika, wie hydrophile Cremes O/W, teilweise hydrophobe
Cremes W/O, Hydrogele, Emulsionen und Suspensionen, sofern sie keine antimikrobiellen
Wirk- oder Hilfsstoffe enthalten. Überflüs-siges Konservieren, z. B.
unter Verwendung einer vorkonservierten Cremegrundlage, gilt es möglichst
zu vermeiden.
Bei Magistralrezepturen sollte man sich auf wenige, gut
bekannte Substanzen aus dem Arzneibuch oder DAC beschränken, die das in Frage
kommende pH-Spektrum abdecken und nur ein einziges Konservierungsmittel einsetzen,
das in Wasser gelöst und ausrei-chend hoch dosiert vorliegt. Im sauren Bereich
unter pH 5,5 werden vorzugsweise Sor-binsäure und teilweise Benzoesäure
mit ihren leicht löslichen und besser zu handhaben-den Alkalisalzen, Kaliumsorbat
oder Natriumbenzoat, in Dermatika eingesetzt. Jedoch ist ein Ansäuern mit
Citronensäure im Verhältnis 2:1 oder Ammoniumcitrat-Puffer zur sauren
pH-Einstellung erforderlich. Im sauren, neutralen und schwach basischen Bereich
(pH 4-8) sind PHB-Ester oder ihre Natriumsalze geeignet, sofern sie nicht in Cremes
durch ihren ungünstigen Verteilungskoeffizienten ausscheiden oder wegen ihres
allergischen Potentials. Eine Einwaagekorrektur für die Salze ist in der
Konservierungsmittel-Tab. aufgeführt.
Propylenglycol wirkt mit 20
% (m/m) bezogen auf die Wasserphase pH-unabhängig kon-servierend und schützt
alkalische Rezepturen mit Erythromycin oder Basiscreme DAC vor mikrobiellem Verderb.
Bei wässrigen Verdünnungen von Basiscreme ist an eine Ergän-zung
von Propylenglycol zu denken. Vergleichbare antimikrobielle Wirkung zeigen Etha-nol
und 2-Propanol ab ca. 15 % in Gelen oder flüssigen Dermatika.
Kriterien
für die Auswahl von Konservierungsmitteln sind insbesondere: pH-Wert der
Zu-bereitung, Wasserlöslichkeit, Stabilität, Verteilungskoeffizient
Octanol/Wasser, Primär-packmittel. Vorgestellt werden Konservierungsbeispiele
aus standardisierten Rezepturen des NRF und Rezepturgrundlagen der Pharmahersteller.
nach oben
Dr. Bernd Hünerbein
Leitlinien
der Dermatologischen Rezeptur
Löwen-Apotheke, Naumburg
Die Leitlinien verbinden die Belange der dermatologischen
Verordnung und Arzneimitteltherapie mit den Grundsätzen einer guten pharmazeutischen
Praxis im Rahmen der gültigen Rechtsnormen. Das therapeutische Konzept, das
jeder Arzt für eine Therapie erstellt, muss vom Pharmazeuten bei der Herstellung
und Abgabe unterstützt werden. Nur so ist die Compliance des Patienten zu
gewährleisten. Dafür ist eine Zusammenarbeit von Arzt und Apotheker
unerlässlich. Der Pharmazeut trägt die volle Verantwortung für
die von ihm verarbeiteten Rezepturgrundstoffe. Auch im Zuge der Globalisierung
ist das ein zunehmend wichtiger Punkt der Qualitätssicherung. Bedenkliche
Bestandteile sind mit Sicherheit auszuschließen. Stoffkombinationen müssen
stabil und therapeutisch sinnvoll sein. Die Anwendungssicherheit der Produkte
im vorgesehenen Anwendungszeitraum muss von Arzt und Apotheker gemeinsam gewährleistet
werden. Für den speziellen Anwendungszweck geeignete Verpackungen erhöhen
die Compliance. Während die Konservierung von Dermatika immer wieder ein
umstrittener Punkt, der eine besonders intensive Zusammenarbeit von Arzt und Apotheker
erfordert, ist die Herstellungshygiene eine ganz wichtige Aufgabe des Pharmazeuten.
Um dem Rechnung zu tragen, hat die Fachgruppe Magistralrezepturen der GD Hygienerichtlinien
erarbeitet und veröffentlicht. Sie umfassen konkrete Maßnahmen zur
Personal- und Herstellungshygiene sowie Checklisten zur Selbstinspektion. Schwerpunkte
der Individualrezeptur sind Zubereitungen mit geringer Lagerfähigkeit, speziellen
Wirkstoffkonzentrationen und speziellen Hilfsstoffkombinationen. Die Sachkenntnis
des Pharmazeuten bei der Arzneiformenherstellung wird hier durch Standardwerke
wie z. B. das NRF unterstützt. Standardisierte Zubereitungen sind in ihrer
Sicherheit den Fertigarzneimitteln vergleichbar. Methoden der Herstellungskontrolle
und ihre Dokumentation haben im Rahmen des QMS auch in der Apothekenrezeptur einen
zunehmend wichtigen Platz bei der Qualitätssicherung. Durch entsprechende
Informationen bei der Abgabe der Produkte unterstützt der Apotheker die Anwendungssicherheit
beim Patienten. Er muss dafür Sorge tragen, dass der Patient alle notwendigen
Informationen erhält. Ohne enge Zusammenarbeit mit dem Arzt und entsprechende
Informationen im Rahmen des therapeutischen Konzepts ist diese Arbeit nicht zu
leisten. Mit hohem Engagement werden seit Jahren standardisierte Rezepturvorschriften
im Rahmen des NRF erarbeitet und eine immer breitere Palette von Arznei- und Hilfsstoffen
mit Arzneimittelqualität im Rahmen der Arzneibücher und des DAC zur
Verfügung gestellt. Die Zusammenarbeit von Ärzten, Apothekern und den
Arzneimittelkommissionen garantiert eine große Sicherheit auch im Bereich
der Magistralrezeptur. Eine wichtige Grundlage für die Realisierung all dieser
Qualitätsschwerpunkte sind gemeinsame Veranstaltungen der Aus-, Weiter- und
Fortbildung von Dermatologen und Pharmazeuten.

Dr. Holger Reimann
Rezepturen
an den Grenzen der Therapiefreiheit
Pharmazeutisches Laboratorium des Neuen Rezeptur-Formulariums (NRF), Eschborn
Nationales
und übernationales Recht autorisieren und verpflichten den Arzt zu einer
medizinischen Behandlung Kranker. Hierfür benötigte Arzneimittel, die
keine zugelassenen Fertigarzneimittel sind, müssen in der Apotheke hergestellt
und abgegeben werden. Der Apotheker ist nach § 17 Abs. 4 ApBetrO zur unverzüglichen
Herstellung auf Verschreibung verpflichtet, allerdings vorbehaltlich mehrerer
Einschränkungen:
| Foto: Gesellschaft für Dermopharmazie |

Apothekerin Rosemarie
Eifler-Bollen * und
Apothekerin Michaela Tünnermann **
* Pharmazeutisches Laboratorium des Neuen Rezeptur-Formulariums (NRF), Eschborn
**Apotheke am Ponzelar, Krefeld
Rezepturen
zum Anfassen:
Vermeidung von Inkompatibilitäten und standardisierte Rezepturen
Unverträglichkeiten (Inkompatibilitäten)
zwischen zwei oder mehreren Rezepturbestandteilen eines Dermatikums können
vielfältige Ursachen haben. Häufig sind durch Salzbildung bedingte Schwerlöslichkeit,
Wirkungsverlust, chemische oder physikalische Instabilität die Ursache. Viele
Unverträglichkeitsreaktionen sind bereits während oder nach der Herstellung
zu erkennen, wie beispielsweise an Fällungen und Konsistenzveränderungen,
an Verfärbungen oder im Brechen der Emulsion. Im Gegensatz dazu gibt es Unverträglichkeiten,
die bei visueller Prüfung nicht ohne weiteres zu erkennen sind, wie beispielsweise
die Beeinträchtigung pH-abhängiger Wirkungen von Arznei- und Hilfsstoffen.
Diese werden auch als „larvierte Inkompatibilität“ bezeichnet.
Die Vermeidung entsprechender Unverträglichkeiten setzt in jedem Fall die
sichere Kenntnis der Einzelbestandteile voraus. Diesbezüglich unproblematisch
sind standardisierte Rezepturen.
So muss bei der Ausoleeignete alternative
Grundlage vorschlagen. Die Auswahl muss in Abhängigkeit
Durch die Zusammenarbeit von Arzt und Apotheker lässt sich die Rezeptur verbessern, sicherer und einfacher machen.
Apothekerin
Rosemarie Eifler-Bollen
| Foto: Gesellschaft für Dermopharmazie |
| Foto: Gesellschaft für Dermopharmazie |


Dr. med. Petra Staubach-Renz
Therapeutisches
Konzept aus der Sicht des Arztes und des Apothekers
Universitäts-Hautklinik Mainz
Dermatologische Rezepturen ermöglichen eine
individuelle Dermatotherapie. Der Arzt erstellt ein Therapiekonzept, das sich
aus der Diagnose, dem Ausmaß der betroffenen Hautveränderungen und
dem individuellen Hautzustand ergibt. Die Forderung des Dermatologen, Wirkstoff
und Vehikel individuell abgestimmt einsetzen zu können, kann durch die Anwendung
bestimmter Rezepturen mit ausgewählten Wirkstoffen und Grundlagen erfüllt
werden, wenn die Grundregeln der Galenik und Dermatopharmakologie berücksichtigt
werden. Dazu muss der Apotheker das gewünschte therapeutische Konzept bei
der Herstellung und Abgabe verfolgen und überwachen, insbesondere unter Beachtung
der Unbedenklichkeit der Bestandteile, der Wechselwirkungen bestimmter Inhaltsstoffe,
der Einhaltung von Maximaldosierungen, der Verträglichkeit, der Applizierbarkeit,
der Hygiene, der Kennzeichnung und der Verpackung der Rezeptur. Eine gute Zusammenarbeit
setzt voraus, dass der Apotheker das therapeutische Ziel des Arztes erkennt und
unterstützt, was das Vertrauen und die Compliance des Patienten in beide
Richtungen fördert.
| Foto: Gesellschaft für Dermopharmazie |

Priv.-Doz. Dr. Ulrike
Heinrich
Anforderungen
an dermokosmetischen Sonnenschutz
DermaTronnier, Institut für Experimentelle Dermatologie, Universität Witten/Herdecke, Witten
Der Begriff Dermokosmetika oder dermopharmazeutische
Produkte wurde von der Gesellschaft für Dermopharmazie (GD) klar definiert.
Dermokosmetika stellen keine neue Produktklasse dar, sondern erfüllen besondere
Anforderungen hinsichtlich ihrer Qualität und Dokumentation. Danach sollen
die kosmetischen Mittel als Dermokosmetika bezeichnet werden, bei denen
der Anwendungszweck unter Mitberücksichtigung dermatologischer und pharmazeutischer
Gesichtpunkte erreicht wird (Lit.: DermoTopics 2001, 1, 92). Einen speziellen
Vertriebsweg z. B. exklusiv über Apotheken, schließt diese Definition
nicht ein.
Welche Anforderungen ergeben sich für einen dermokosmetischen
Sonnenschutz?
Gemäß der oben genannten Definition sollten dermokosmetische
Sonnenschutzprodukte bestimmten Qualitätsanforderungen genügen.
Hierzu gehören: Ausreichende Dokumentation der galenischen Eigenschaften,
der Inhalts- bzw. Wirkstoffe, der Hautverträglichkeit und der Wirksamkeit
bezüglich des Sonnenschutzes. Diese umfasst einen ausreichenden Schutz sowohl
im UVA- als auch im UVB-Bereich. Wird ein besonderer Schutz bei Lichtdermatosen
ausgelobt, so muss dieser durch spezielle Prüfungen nachgewiesen sein.
Zielgruppe für dermokosmetischen Sonnenschutz sind alle besonders zu
schützenden Anwendergruppen, wie Kinder, sehr hellhäutige Personen (Lichttyp
I und II), Sportler sowie Personen mit Lichterkrankungen oder solche, die beruflich
starker Sonneneinstrahlung ausgesetzt sind. Ferner Patienten, die Medikamente
mit möglicher phototoxischer Nebenwirkung einnehmen.
Bislang existieren
zwar Normen für die Bestimmung des Sonnenschutzfaktors im UVB-Bereich (Colipa,
DIN, FDA, australischer Standard etc.), aber es gibt kein einheitliches, interdisziplinär
abgestimmtes Konzept über wichtige Kriterien.
Die Fachgruppe Dermokosmetik
der Gesellschaft für Dermopharmazie e. V. hat sich daher als unabhängige
Organisation die Aufgabe gestellt, wichtige Kriterien über dermokosmetischen
Sonnenschutz zu erarbeiten, um die Mindestanforderungen hinsichtlich der Qualität
und Dokumentation zu fixieren.
Ziel der Fachgruppe ist es, eine systematisch
erarbeitete Empfehlung in Form einer Leitlinie zum dermokosmetischen Sonnenschutz
unter Auswertung der international relevanten Literatur zu erstellen. Diese Leitlinie
ist als Hilfestellung für alle gedacht, die mit dermokosmetischem Sonnenschutz
der Haut befasst sind. Gesetzliche Änderungen für Dermokosmetika werden
hierbei nicht angestrebt. Die bestehende Einstufung als kosmetische Mittel wird
als ausreichend erachtet.
Die Verabschiedung und Veröffentlichung der
GD-Leitlinie „Dermokosmetischer Sonnenschutz“ ist für das Frühjahr
2003 vorgesehen.
Dipl.-Ing. Peter
Finkel
Der
Markt der kosmetischen Lichtschutzmittel:
Historische Entwicklung – Meilensteine
– Marktsituation 2001 – Trends
Sara Lee Houshold and Body Care Deutschland GmbH, Düsseldorf
Historische
Entwicklung – Meilensteine
Der wichtigste Meilenstein der modernen
Lichtschutzmittel wurde in den 30er Jahren des letzten Jahrhunderts gesetzt: Die
UV-Filter wurden als Wirkstoffe für dermal anzuwendende Sonnenschutzmittel
entdeckt. An die Stelle von abdeckenden Pudern oder mit Make-up vergleichbaren
Produkten traten damit erstmals transparente und trotzdem sehr wirksame Formulierungen.
Die breite Einführung des Lichtschutzfaktors (SPF) in den 70er Jahren war
ein weiterer wichtiger Meilenstein. Die eher allgemein gehaltene Beschreibung
der Schutzleistung wurde durch eine genaue Zahlenangabe ergänzt. Damit wurde
der Markt für den Konsumenten hinsichtlich der Produktleistung transparent.
Ein wahrlich revolutionärer Schritt in dem sich überwiegend emotional
differenzierenden kosmetischen Produktumfeld. Der Lichtschutzfaktor setzte sich
in den 70er und 80er Jahren weltweit durch. Die 90er Jahre brachten eine regelrechte
SPF-Inflation, die schließlich 1998 zum SPF-Gipfel von SPF 123 in Japan
führte. Um diese wenig sinnvolle Entwicklung zu beenden und mehr Transparenz
für den Konsumenten zu schaffen, sollen in Europa den SPF-Zahlenwerten Schutzklassen
zugeordnet und ein Maximum von SPF 50+ eingeführt werden. Derzeit wird über
die Industrieverbände an einer weltweiten Harmonisierung des SPF-Systems
gearbeitet Ein weiterer Meilenstein in der Geschichte des kosmetischen Sonnenschutzes
zeichnet sich ab.
Marktsituation 2001
Der Weltmarkt der
kosmetischen Sonnenschutzmittel 2001 wird auf ca. 3.6 Mrd Euro geschätzt.
Nach den USA ist Deutschland der zweitgrößte nationale Markt. Die führenden
europäischen Marken sind Nivea (BDF), Ambre Solaire (L’Oreal), delial (Sara
Lee) und Piz Buin (Johnson & Johnson). Bei den Formulierungstypen wird der
Markt eindeutig von den flüssigen Emulsionen (Milch) dominiert. Nach Wert
haben jeweils etwa die Hälfte der Produkte Lichtschutzfaktoren bis 15 bzw.
darüber. Schutzfaktoren von über 30 haben nur geringe Marktbedeutung.
Trends
Der Trend zu höheren Lichtschutzfaktoren
wird sich auch in den nächsten Jahren fortsetzen. Neue Erkenntnisse aus der
Hautforschung und daraus abgeleitete Prüfmethoden werden es ermöglichen,
Produkte hinsichtlich des Schutzes vor Immunosuppression, Hautalterung und Hautkrebs
zu optimieren. In diesem Zusammenhang wird der UVA-Schutz eine besondere Rolle
spielen. Sonnenschutzmittel werden zukünftig verstärkt zusammen mit
anderen Maßnahmen (Tragen von Sonnenbrillen, Schutz vor UV-Strahlung durch
Textilien, Informationen zur täglichen UV-Strahlung über Medien) ein
integrales Schutzkonzept bilden. Nicht zuletzt werden Aufklärung und Information
den Konsumenten zu einem stärker vernunftorientierten Umgang mit der Sonne
führen. Dies wird der wichtigste und Erfolg versprechende Schritt zur Optimierung
des kosmetischen Sonnenschutzes sein.
| Foto:
Gesellschaft für Dermopharmazie |

Dr. Heiner Gers-Barlag
(unter Mitarbeit von V. Wendel und E. Klette)
Ein
neues Verfahren zur Prüfung des UVA-Schutzes in vitro
Beiersdorf AG, Hamburg
Aufgrund der steigenden Kenntnisse über
UVA induzierte Hautschäden besitzt der Schutz gegenüber dieser Strahlung
eine zunehmende Bedeutung bei der Entwicklung von modernen Sonnenschutzprodukten.
Derzeit gibt es aber keine offiziell anerkannte Methode, wie dieser UVA-Schutz
gemessen werden kann. In der vorliegenden Studie wurde ein neues Messverfahren
entwickelt, welches einerseits die exzellente Reproduzierbarkeit einer standardisierten
Transmissionsmessung besitzt und auf der anderen Seite eine relevante Aussage
über die Schutzleistung des Produktes auf der menschlichen Haut zulässt,
wie es bisher nur für In-vivo-Methoden angenommen wird.
Der Messvorgang
sieht vor, dass eine Schicht eines Sonnenschutzmittels auf eine angeraute Unterlage
aus Plexiglas (PMMA) mit dem Finger ausgestrichen wird. Die Auftragsmenge sollte
dabei so gewählt werden, dass bei der Transmissionsmessung im UV-Bereich
der Absorptionswert von 2 nicht überschritten wird. Die resultierende, charakteristische
Schutzkurve wird über eine Konstante so angepasst, dass der In-vitro-SP-Wert
dem in vivo gemessenen SPF entspricht. Weiterführend wird dann ein In-vitro-PPD-Schutzfaktor
errechnet.
Anhand von vergleichenden In-vivo- und In-vitro-Messungen
an insgesamt 45 Sonnenschutzprodukten, die repräsentativ für den europäischen
und amerikanischen Markt sind, konnte eine sehr gute Korrelation aufgezeigt werden.
Daraus ergibt sich, dass die Methode als allgemeine Messmethode zur Bestimmung
des UVA-Schutzes geeignet ist.
| Foto: Gesellschaft für Dermopharmazie |

Birgit Huber
Gesetzliche
Bestimmungen zu Sonnenschutzfiltern
Industrieverband Körperpflege- und Waschmittel e.V. (IKW), Frankfurt am Main
Definition
kosmetischer Mittel
In der Europäischen Union sind kosmetische
Mittel seit 1976 in der EG-Kosmetik-Richtlinie geregelt. Die Definition kosmetischer
Mittel beschreibt die möglichen Funktionen. Diese sind: Reinigen, Parfümieren,
Aussehen verändern, Körpergeruch beeinflussen, Schützen und in
gutem Zustand halten. Da Sonnenschutzmittel die überwiegende Zweckbestimmung
haben, die Haut vor den schädlichen UV-Strahlen zu schützen und in gutem
Zustand zu halten sind dies Produkte in der Europäischen Union eindeutig
unter diese Definition einzuordnen, und daher gelten für diese Produkte die
gesetzlichen Bestimmungen der EG-Kosmetik-Richtlinie. Weiterhin ist dort festgeschrieben,
dass kosmetische Mittel die Gesundheit des Verbrauchers nicht schädigen dürfen.
Gesetzliche Anforderungen in der Kosmetik-Richtlinie
Hierzu
gilt es die allgemeinen Anforderungen der Richtlinie zu befolgen. Die Kosmetik-Verordnung
setzt die EG-Kosmetik-Richtlinie in deutsches Recht um. Sie enthält eine
Negativliste mit Stoffen, die zur Verwendung in kosmetischen Mitteln verboten
sind, wie z.B. Urocaninsäure. Weiterhin gibt es sogenannte Positivlisten.
Stoffe, die unter Positivlisten fallen, sind Farbstoffe, Konservierungsstoffe
und UV-Filter. Für diese Stoffgruppen gilt, dass nur die in den Positivlisten
aufgeführten Stoffe zu diesem jeweiligen Anwendungszweck erlaubt sind. Um
die Zulassung eines Stoffes zu erlangen, bedarf es der Bewertung umfangreicher
toxikologischer Daten durch das Wissenschaftliche Komitee Kosmetologie und Nichtlebensmittelprodukte
und anschließender Zulassung durch die Mitgliedstaaten der EU (SCCNFP).
Darüber hinaus enthält die Kosmetik-Richtlinie noch eine Vielzahl weiterer
Anforderungen, die auch für Sonnenschutzprodukte zu erfüllen sind. Hierzu
gehören die Erstellung von Produktangaben mit umfangreichen Informationen
über das jeweilige kosmetische Mittel inklusive einer Sicherheitsbewertung
durch einen entsprechenden Experten, umfangreiche Kennzeichnungsvorschriften,
wie z.B. die Deklaration der Inhaltsstoffe nach INCI etc..
Regelungen
von UV-Filtern
Im Anhang VII der EG-Kosmetik-Richtlinie sind
derzeit 24 UV-Filter endgültig zugelassen. Es kann davon ausgegangen werden,
dass sich diese Zahl in Kürze um ca. drei weitere Stoffe erhöht, da
schon seit längerer Zeit ein Vorschlag einer Anpassungs-Richtlinie diskutiert
wird, der die Zulassung dieser Stoffe vorsieht.
UV-Filter
sind nach der Kosmetik-Verordnung Stoffe und Zubereitungen, die überwiegend
zu dem Zweck zugefügt werden, UV-Strahlen zu filtern, um diese vor bestimmten
schädlichen Einwirkungen dieser Strahlen zu schützen.
Darüber hinaus wird dort hervorgehoben, dass andere UV-Filter, die in kosmetischen
Mitteln nur zum Schutz der Erzeugnisse gegen UV-Strahlen verwendet werden, nicht
auf dieser Liste stehen. Das heißt, dass die im Anhang VII geregelten Stoffe
auch zum Produktschutz eingesetzt werden können, allerdings die Möglichkeit
besteht, auch andere UV-Filter zu diesem Zwecke einzusetzen.
Lange war
fraglich, wie die beiden Stoffe Titandioxid und Zinkoxid im Rahmen dieser Regelungen
zu bewerten sind. Zunächst war man davon ausgegangen, dass diese beiden Stoffe
das UV-Licht nur reflektieren. Vor einigen Jahren gab es dann allerdings in der
wissenschaftlichen Literatur Publikationen, aus denen klar hervorgeht, dass die
beiden Stoffe nicht nur reflektieren, sondern das UV-Licht auch filtern. Aufgrund
dieser neuen Erkenntnisse war es notwendig geworden, die beiden Stoffe im Rahmen
des Anhangs VII zu regeln. Die deutsche Regierung hat hierzu einen entsprechenden
Vorstoß in Brüssel unternommen und bereits in der deutschen Kosmetik-Verordnung
eine entsprechende Regelung vorgesehen. Inzwischen wurden für beide Stoffe
auch Dossiers beim SCCNFP eingereicht, und für Titandioxid gibt es bereits
eine positive Bewertung. Titandioxid ist einer der oben genannten Stoffe, der
in Kürze EU-weit mit einer maximalen Konzentrationsbeschränkung von
25 % zugelassen werden wird. Bei dem hier eingesetzten Titandioxid handelt es
sich um einen Stoff mit einer sehr kleinen Körnchengröße, der
zusätzlich chemisch behandelt wurde, um diese Anforderungen zu erfüllen.
Mit einer Bewertung des entsprechenden Dossiers für Zinkoxid durch das SCCNFP
wird noch in diesem Jahr gerechnet.
| Foto:
Gesellschaft für Dermopharmazie |

Dipl. Bio-Ing. Stephan
Bielfeldt
Methoden
in der Sonnenschutzfaktortestung:
Stand der Normung
proDERM Institut für Angewandte Dermatologische Forschung, Schenefeld
In
dem Vortrag wird ein Überblick über die genormten Sonnenschutzfaktor-Methoden,
die weltweit zur Anwendung kommen, gegeben. Der Schwerpunkt liegt dabei auf der
COLIPA-Methode von 1994, die für den europäischen Raum maßgeblich
ist. Beschrieben werden weiterhin die verschiedenen Methoden der Wasserresistenzprüfung
und der derzeitige Stand der Normung auf diesem Gebiet sowie verschiedene In-vivo-
und In-vitro-Prüfverfahren zur Messung des UV-A-Schutzes. Auch für diese
Methoden wird der Stand der Normung beschrieben. Als Blick in die Zukunft wird
diskutiert, wie weit die internationale Harmonisierung, insbesondere mit den USA,
fortgeschritten ist und welche Methoden sich voraussichtlich in Zukunft weltweit
durchsetzen werden.
Dipl.
Bio-Ing. Stephan Bielfeldt
| Foto: Gesellschaft für Dermopharmazie |

Prof. Dr. med. Eckhard-Wilhelm
Breitbart (unter Mitarbeit von R. Greinert)
Sonne
und Haut:
Biologische Wirkungen der UV-Strahlung
Dermatologisches Zentrum Buxtehude
Ohne die Sonne wäre ein Leben
auf der Erde nicht möglich. Allerdings bewirkt der UV-Anteil im Strahlungsspektrum
der Sonne molekulare und zelluläre Veränderungen in der Haut, die letztendlich
zu Hautschädigungen und Hautkrebs führen können.
Die Wirkungen
der UV-Strahlung auf die Haut können in zwei große Bereiche eingeteilt
werden: Akute und chronische Wirkungen. Zu den akuten Wirkungen zählen die
Vit. D3 -Synthese, die Bräunung, das Erythem, die Erzeugung der Lichtschwiele
und die UV-vermittelte Immunsuppression. Chronische Wirkungen sind die (UVA-bedingte)
Hautalterung und die Photokarzinogenese. Das Auftreten bestimmter Wirkungen ist
Wellenlängen-abhängig und mit unterschiedlichen UV-Expositionsmustern
korreliert.
Für den Hautkrebs, welcher weltweit den Krebs mit der
höchsten Inzidenz darstellt, belegen eine Vielzahl von epidemiologischen
und experimentellen In-vitro- und In-vivo-
Untersuchungen einen eindeutigen
Zusammenhang mit der UV-Exposition. Dabei scheinen unterschiedliche UV-Expositionsmuster
mit dem Auftreten der verschiedenen Hautkrebsarten zusammenzuhängen:
| Plattenepithelkarzinom, SCC | (kumulative UV-Exposition) |
| Basalzellkarzinom, BCC | (kumulative und/oder intermittierende UV-Exposition) |
| Malignes Melanom, MM | (intermittierende UV-Exposition) |
Die molekularen Mechanismen der
Photokarzinogenese sind noch nicht vollständig geklärt, jedoch ist u.a.
bekannt, dass bestimmte UV-induzierte „signature mutations“ (z.B im
p53-Gen, SCC), Veränderungen im „hedgehog-pathway“ (BCC) und chromosomale
Rearrangements (beim MM) von Bedeutung sind. Eigene, neue Untersuchungen weisen
auf die Bedeutung schwer UV-geschädigter epidermaler (Stamm-) Zellen in der
Ätiologie der nicht melanozytären Hautkrebse (SCC, BCC) hin.
Wegen der Beeinträchtigung der Lebensqualität und seiner hohen Inzidenz
stellt der Hautkrebs ein ernst zu nehmendes gesundheitliches und gesundheitspolitisches
Problem dar, bei dem die induzierten hohen Kosten eine nicht zu vernachlässigende
Belastung der finanziellen Ressourcen im Gesundheitswesen bedingen. Allerdings
kann dieser Problematik mit kontinuierlichen Maßnahmen der primären
und sekundären Prävention begegnet werden.
Prof.
Dr. med. Eckhard-Wilhelm Breitbart
| Foto: Gesellschaft für Dermopharmazie |

W. Wigger- Alberti
(1), M. Keskin (1), G. Feistkorn (2), K.P. Wilhelm (1)
Assessment
of patch test reactions due to hair dyes with the Laser doppler perfusion scanning
technique
(1)
proDERM Institute for Applied Dermatological Research GmbH, D 22869 Schenefeld,
Germany
(2) Wella AG, D 64295 Darmstadt, Germany
Introduction:
The interpretation of test reactions of epicutaneous patch tests might
be difficult in cases where coloured test products such as hair dyes have to be
assessed. The subjective clinical scoring is influenced by the colour and even
the benefit of colorimeters is limited. The aim of the present study was to investigate.the
usefulness of the laser Doppler perfusion technique to investigate skin irritation
alter application of hair dyes with different irritant potential.
Methods:
In order to basically test the practicability of this approach SLS was
added to a hair dye at different concentrations (0.5%, 1%, 2%). Products were
applied to the forearms of 15 volunteers. On day 1 and 3 visual sconng and instrumental
measurements (chromametry, TEWL and Laser Doppler perfusion technique) were performed.
Results:
With visual scoring a significant difference was only detected an areas
without dye, between 0.5% SLS and 2% SLS. With TEWL and LDI measurements significant
differentes were detected between the dye without irritant and all test products
with dye and 1% or 2% SLS. Chromametry, however, did not show differentes that
could plausibly be correlated to the irritation potential of the test products.
Conclusion:
Dependent an the type of irritant TEWL and Laser Doppler perfusion imaging
are recommended as the methods of choice when evaluating skin irritation potential
of coloured test products.
Kockott, D.*, Tronnier,
H.‘, Hölzner, B.**, Heinrich, U.**
Automatic in Vitro
Evaluation of Suncare Products
*
UV Technik, 63456 Hanau, Germany
** Institute for Experimental Dermatology,
University Witten/Herdecke, 58455 Witten, Germany
State of
technology:
With all in vitro methods used at present, the spectral transmittance
of suncare products is measured in a spectral photometer. From the spectral transmittance,
characteristic values for the protective effect in UV13 and UVA are derived. The
protective effect of a sun care product regarding the erythema is described by
the SPF (Sun Protection Factor).
Measuring method and device:
The sample is irradiated by simulated solar radiation. The radiation source is
a Xe lamp, whose radiaions is filtered by two selectively reflecting mirrors and
different filters such that the spectral distribution in the wavelength range
290 nm < X:5 400 nm corresponds to the norm sun of COLIPA and DIN 67501.
Behind the sample there are two radiation receivers which are used alternatively
for UVA and UVB and are automatically driven into the path of the rays.
Objective of a new method and device:
The new device (Sunscreen Tester)
used for measuring the protective effect of suncare products realizes the irradiation
conditions analogous to a normal in vivo measurement. During the irradiation process
it continuously measures both the SPF and the spectral transmittance behind the
sample. From the latter, further protection parameters are calculated. Information
about the stability of a suncare product is automatically obtainable.
Results and conclusions:
The presented in vitro method and the accompanying
device Sunscreen Tester allow a fast and automatic determination of all factors
characterizing the protective effect of suncare products during irradiation.
For a number of commercial suncare products with sun protection factors between 4 and 30, the SPF was determined by both the in vivo method and the new in vitro method presented. Both SPFs correspond to each other within an error range of ± 20%.
It is also possible to calculate other characteristic values, such as the critical wavelength k, according to Diffey and the ratio of protective effect UVA/UVB from the spectral absorptance.
References
1. H.
Tronnier, D. Kockott, B. Meick, N. Hani, U. Heinrich: Zur in vitro Bestimmung
des SPF; Parfümerie und Kosmetik, 77.326 329 (1996)
2. H. Tronnier, B.
Hölzner, U. Heinrich, D. Kockott, B. Reubke Gothe: Zur Praxis der in vitro
Bewertung von Sonnenschutzmitteln; Kosmetische Medizin 18.344 350 (1998)
3.
D. Kockott: In vitro Bewertungen von Sonnenschutzmitteln; Kosmetische Medizin
19.290 293 (1998)
4. U. Heinrich, H. Tronnier Ein neues in vitro Verfahren
zur Bestimmung des UVA Schutzes von Lichtschutzpräparaten; SÖFW Journal
12.40 41 (1999)
A. Claaßen*,
A. Klotz*, A. zur Mühlen*, B. Thörner*
Einfluss
von Hautschutzprodukten auf die Eigenschaften von Schutzhandschuhen
*Degussa, Skin Care, Krefeld,
Deutschland
In vielen Berufen wie z.B. Friseurhandwerk, Heil
und Pflegeberufen und lebensmittelverarbeitender Industrie werden enganliegende,
feuchtigkeitsundurchlässige Schutzhandschuhe zur Vermeidung berufsbedingter
Hauterkrankungen getragen.
Durch das Tragen dieser Handschuhe kommt es
zu Okklusionseffekten. Dieser Feuchtigkeits und Wärmestau führt zur
Quellung der Hornschicht. („Waschfrauenhände“). Durch diese Mazeration
wird die Widerstandsfähigkeit der Haut gegenüber äußeren
Einflüssen herabgesetzt [1].
Im Markt sind verschiedene kosmetische
Produkte erhältlich, die eine Verringerung der Hautmazeration beim Handschuhtragen
bewirken. Allerdings wird immer wieder diskutiert, dass Inhaltsstoffe von Hautschutzpräparaten
Handschuhmaterialien beeinflussen können [2].
Es gibt verschiedene
DIN Methoden, mit denen die physikalischen Eigenschaften von Handschuhmaterialien
untersucht werden. Durch Modifikation dieser Testdesigns können die Wechselwirkungen
zwischen Hautschutzprodukt und Schutzhandschuh untersucht werden. Hier bieten
sich die DIN Methoden 455 Teil 1 (Dichtigkeit) und Teil 2, Pkt 5.2 (Reißkraft)
an.
Des weiteren gibt es ein Prüfverfahren für Kondome aus
Naturkautschuklatex (DIN EN 4074), in dem die Dichtheit von Kondomen bestimmt
wird. Durch Modifikation dieser Methode kann der Einfluss von Hautschutzpräparaten
auf Schutzhandschuhe bestimmt werden [3].
Ziel der Untersuchung war
es mittels der Reißfestigkeitsmethode (DIN EN 455 Teil 2) und einer elektrischen
Messung (lonenpermeabilität) in Anlehnung an DIN EN 4074 den Einfluss eines
Hautschutzgels auf die physikalischen Eigenschaften eines Nitril Untersuchungshandschuhs
zu bewerten. Mit der Methode der Reißfestigkeit konnte ein zeitabhängiger
Einfluss eines Hautschutzgeles auf die physikalischen Eigenschaften der Handschuhe
nachgewiesen werden. Die Messung der lonenpermeabiltiät scheint dagegen weniger
sensitiv zu sein, da kein signifikanter Unterschied zwischen den unbehandelten
und den mit einem Hautschutzgel behandelten Handschuhen erkennbar war.
[1] TAGES 531, 1996
[2] Chemical Resistente Volume Il Therrnoplastic Elastomers,
Thermosets and Bohrers. Second Edition es. 1994, Norwich, NI: Plastik Design Library
[3] Helfrich et at., Einfluss von Hautschutzpräparaten auf die Eigenschaften
von Latexhandschuhen. Hofmann, Reschauer, Stößel, Arbeitsmedizin im
Gesundheitsdienst, Be. 14, Edition ABGAS, 2001
H. Tronnier, M. Wiebusch,
U. Heinrich
Frictiometry on human skin
Institute for Experimental Dermatology,
University Witten/Herdecke, 58455 Witten, Germany
Background:
The state and function of human skin can be quantified by numerous non invasive
test methods (1).
There are, however, still no valid methods to measure the
tactile properties of the skin surface and thus to quantify the state of the skin
an the one hand, and to determine the negative and positive effects of tactile
influences an the other hand.
Objective:
In the following, a
measuring device with variable parameters is described. With this device the afore
mentioned objectives are to be reached and examples for the practical application
of the method will be given. If need be, this can be done in combination with
a method for the determination of the skin physiologically relevant surface parameters
(2).
Methods:
The measuring device (Friktiometer®) (Producer:
Courage und Khazaka, electronik GmbH, Mathias Brüggen Str. 91, 50829 Köln)
consists of a sensor, which is to be placed onto the skin, a steering unit and
a monitor.
The measuring head contains a DC micro motor, which is controlled rotationally (50 80 revolutions/min) onto which a variable Teflon sensor head (0 10 mm) can be placed via an exchangeable spring. The skin contact force of the rotating sensor is determined inductively with the spring constant and the compression. The torque, i.e. the circular friction an the skin surface, is measured via the motor load current and is shown as a voltage drop.
Results:
Depending an the surface structure there are higher values for dry and wrinkly
skin than for normal skin.
While water increases the frictionary resistance of the skin, depending an their galenic (lipid proportion) skin care products lead to „smoothing“ of the skin. This is more pronounced an dry than an normal skin.
The frictionary resistance an dry skin is lower than an moist skin.
The effect of a W/O emulsion is not only greater, but it also lasts longer than the effect of an O/W emulsion.
Conclusion:
A new measuring device for the defined friction of the skin (Friktiometer°)
is described and its possible applications are shown with examples. There were
the following findings: The frictionary resistance of the skin is determined by
the state of its surface structure. Skin care products improve the frictionary
resistance time dependently.
The frictionary resistance is increased an moist skin.
Depending an the material and e.g. their moistness, textiles, fleeces, etc. increase the frictionary resistance of the skin.
In comparison to an untreated sample, paper tissues containing additives, for instance, can reduce the frictionary resistance and thus also irritation.
The SELS procedure facilitates a differentiated analysis of friction irritations.
References:
1. J. Serup, G.B.E.Jemec (Herausgeber): Handbook of non invasive Methods and the
skin; CRC Press (1995)
2. H. Tronnier: Ergebnisse der Hautoberflächenanalyse
mit SELS; Kosm. Medizin 19.278 283 (1998)
3. H. Tronnier, M. Wiebusch, U.
Heinrich: Friktiometrie an der menschlichen Haut; Kosm. Medizin 22.228 235 (2001)
Wolfgang Pittermann
(1 )Olaf Lammerschop (1), Marcel Roth (1) Michael Schmitt (1), Manfred Kietzmann
(2)
Oil and waterbased formulations containing nanoparticles
The
dermal behaviour after topical application under in vitro conditions (BUS Model)
1 Henkel KGaA, D 40191 Duesseldorf,
2 Institute for Pharmacology, Toxicology and Pharmacy, Veterinary School
Hannover, D 30559 Hannover
Fragestellung: Beeinflußen bestimmte Nanopartikel (4 unterschiedliche Ferrofluide) typische Charakteristika von öloder wasser basierten, topischen Formulierungen?
Methode: Hautpenetration (Hornschicht) und aktivierung (PGE2/ MTT) im in vitro BUS Modell nach verschiedenen Einwirkzeiten und Applikationsformen (mit / ohne Massage).
Ergebnis: Die typischen Formulierungscharakteristika werden durch Ferrofluide nicht wesentlich verändert. Ferrit wird in unterschiedlicher Menge in die Hornschicht und in die oberen Haarfollikelabschnittel eingebracht.
Bei allen Ferrofluiden
kommt es zu einer üblichen, transienten Hautaktivierung der Formulierung
entsprechend. Negativer Einfluss auf die Hautverträglichkeit ist auch aus
den Ergebnisse mit verlängerter Expositionszeit (5,0 h) und Massage nicht
zu erkennen. Massage begünstigt die Hornschichtpenetration und fördert
erwartungsgemäß die Hautaktivierung.
Oil-
and waterbased formulations containing nanoparticles
The dermal behaviour
after topical application under in-vitro conditions (BUS-Model)
Wolfgang Pittermann 1, Olaf Lammerschop 1,
Marcel Roth 1, Michael Schmitt 1 and
Manfred Kietzmann2
1 Henkel KGaA, 40191 Duesseldorf,
2 Institute for Pharmacology,
Toxicology and Pharmacy, Veterinary School Hannover
| Introduction |
| Oil- and water-based formulations were frequently used for cosmetic
and dermatological treatments or as process chemicals. It is well known that the
specific behaviour concerning the dermal penetration and irritation potential
will be modified during and after the course of application due to supersaturated
solutions by evaporization of water and other volatile components (1). It can
also be influenced by ingredients of which the distribution coefficient is not
known before. The aim of this in-vitro skin study was to learn the dermal behaviour of newly developed ferrofluides (nanoparticles) dispersed in water- and oil-based formulations under different application conditions. |
| Material and Methods |
| Ferrofluids are nanoparticles either magnetic or non-magnetic dis-persed in solvent (Fig. 1, Fig. 2). Two water-based products (product 1, 3) contain magnetite-particles coated by polyacrylic acid and lauric acid (product 3*) respectively. The other two samples (magnetite or zinc-ferrit) are based on the emollient dicaprylyl ether as vehicle and isostearic acid (Cognis Deutschland) as coating material. The product 4 contains zinc-ferrit instead of magnetite. |
| To achieve long-term stability in water and organic solvents respectively, the particle size has been adjusted to 5 – 20 nm and the particle surface has been modified to adapt the polarity of the particles to the dispersing agent. The core of the nanoparticles consists of non-toxic iron oxide and was synthesised by precipitation of ferric salt precursors. A suspension of these particles is long-term stable especially by applying a magnetic field. The surface modification consists of fatty acids which shows a good adhesion to iron oxide. |
| The isolated perfused bovine udder skin (BUS) is regarded as a viable
in-vitro model (Fig. 3). Using unimpaired
natural skin it takes into account active skin barrier properties and cutaneous
metabolic processes, so that it be used to study for both, penetration and irritation
induced by ingredients or formulations (2, 3, 4, 5). The open application (2 – 4 g / 100 cm2) was performed in four independent studies (Fig. 4) either by the means of glass spatula (conventional) or a intensive finger massage (1 minute) of the skin. After the exposure periods of 1.0 h and 5.0 h the repeated horny layer stripping method (10 times) was used (Tesa 4204, BDF, Hamburg, 19 mm × 100 mm) for studying the penetration of Fe. For the irritation assays a short term exposure period of 0.5 h was added to the periods of 1.0 h and 5.0 h. Whole skin biopsies were prepared for the MTT-assay (cytotoxicity) and the determination of the PGE2-tissue concentration (irritancy) compared to untreated sites. |
| Additionally a new technique for a precise histochemical
determination of six different layers of the skin was introduced (Fig.
4). In contrast to the standard preparation of the whole skin biopsies this
procedure (V-max-technique, HistoServe GmbH, Münster, Germany) allows to
assay the activities of certain intracellular enzymes in freely selected regions
of epidermal or dermal layers. |
| Results and Discussion |
| Penetration
Calculated up-take (%) |
| The percentual up-take was at the maximum approx. 10 % – 12 % (Fig.
5). As expected the 1st strips of all groups exhibited more Fe-content (>
1.0 %) than each of the following nine strips at both exposure periods. Irritation (cytotoxicity / irritancy) For the irritation assay a very short exposure period of 0.5 h was included into the study design additionally. The degree of irritation is demonstrated by the score value combined from the relative MTT-result (cytoxicity, irreversible) and the PGE2-concentration (irritancy, reversible) (6, 7). All columns in Fig. 6 consist of both, the singular score for irritancy on the basis and for the cytotoxicity on the top. |
| Only after the very short exposure period of 0.5 h a difference between
the water- or oil-based formulations could be observed. The score value of the
oil-based formulations (product 2, 4) was more than twofold compared to the value
of the water-based formulations. As expected intensive massage application induces an increased score level compared to the conventional application due the intensified release of PGE2. Under massage conditions the change from the formulation-related profile at the exposure period of 0.5 h to the individual product profile after additional 30 minutes was very similar to the results obtained after the conventional application. Generally the massage procedure also altered the relationship between cytotoxic and irritant action of all products independently from the type. The mechanical skin treatment by the massage induced an increase of the PGE2-tissue concentration by about 70 %, whereas simultaneously the cytotoxic activity of the formulations was decreased by approx. 50 %. Although the tape stripping did not result in the complete removal
of all of the stratum corneum and contents of the hair follicles the material
recovered should be treated as representative fraction of that present in the
horny layer due to the extra large size of the strips. |
| The results shown in the Figures 5 and 6 are combined in Fig. 8 for direct comparison. Clearly the penetration potential (up-take) into the horny layer is differently profiled than the irritation potential (score). |
| The results (Fig. 9, relative units) of the V-max-technique showed no altered activity for the enzyme SDH with its main activity in SB. However, the massage treatment induced a slight decrease of activity of LDH in SB, SS and SG, but not in the horny and dermal layers. |
| Conclusion |
|
| References |
| 1Th. Förster, W. Pittermann, M. Schmitt and M. Kietzmann; Skin penetration properties of cosmetic formulations using a perfused bovine udder model; J. Cosmet. Sci. 50, 147-157 (1999) 2 M. Kietzmann, W. Löscher, D. Arens, P. Maaß and D. Lubach; The Isolated Perfused Bovine Udder as an in Vitro Model of Percutaneous Drug Absorption. Skin Viability and Percutaneous Absorption of Dexamethasone, Benzoyl Peroxide and Etofenamate; J. Pharm.Toxicol. Meth. 30, 75-84 (1993) 3 W. Pittermann, B. Jackwerth and M. Schmitt (1997); The Isolated Perfused Bovine Udder Skin Model: In Vitro Model for the Assessment of Skin Penetration & Irritation; In Vitro Toxicol. 10, 17-21 (1/1997) 4W. Bäumer and M. Kietzmann; The isolated Perfused Bovine Udder as a Model of Dermal Eicosanoid Releaser; ATLA 28,123-134 (2000) 5 Ch. Hammes, M. Schmitt, Th. Förster and W. Pittermann; „Bioaktive Wirkstoffe – Nachweis der Penetration“ in Innovative Analytik in der Kosmetik; 14. DGK-Symposium; Proceedings 91-93 (2001). 6 Nicotera, P.; Alteration of Cell Signalling in Chemical Toxicity; Arch. Toxicol. (suppl. 18) pp 3-11; Springer Verlag, Berlin, Heidelberg (1996) 7 Ponec, M.: In vitro models to predict Skin Irritation in The Irritant Contact Dermatitis Syndrom (edited by P.G.M. van der Valk, H.I.Maibach) pp 335-341; CRC Press, Boca Raton (1995) |





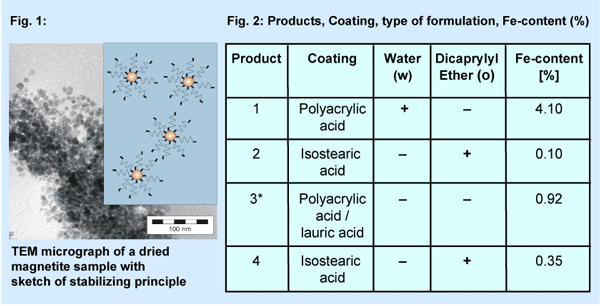
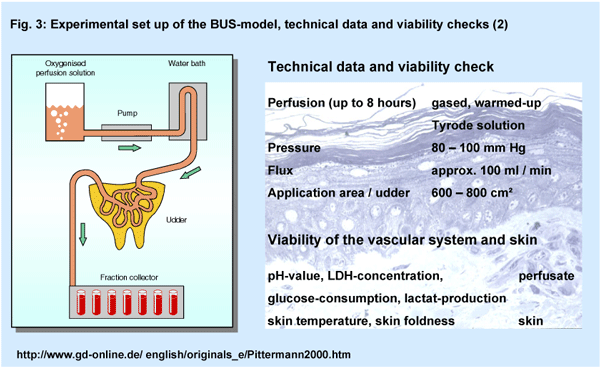
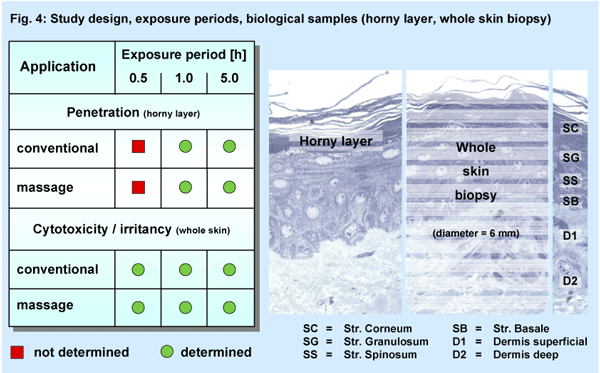
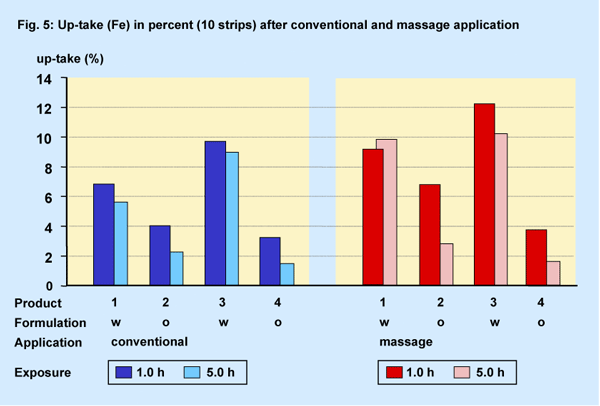
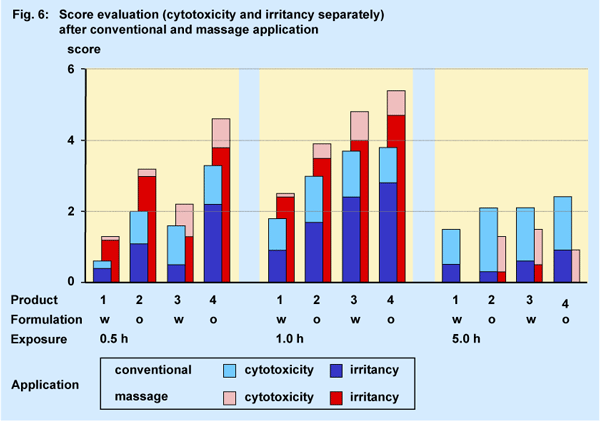

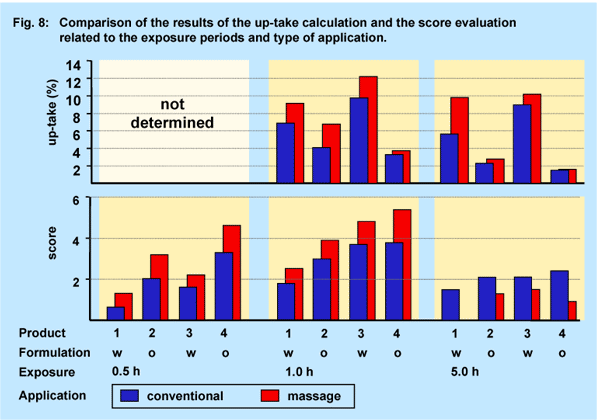
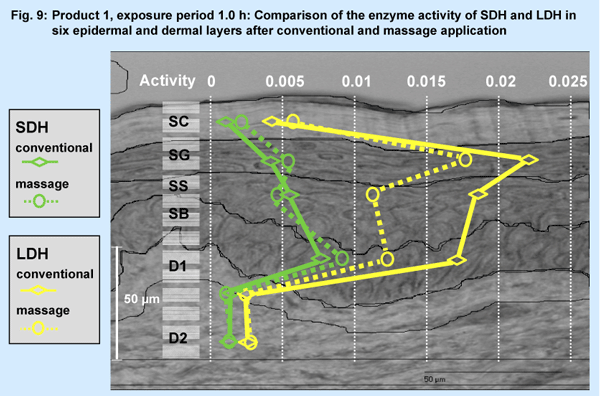
Hoffmann, C., Winkler,
A., Müller Goymann, C.C.
Organotypische Hautäquivalente
für Permeationsuntersuchungen von Arzneistoffen aus dermalen Zubereitungen
Institut für Pharmazeutische
Technologie, Technische Universität Braunschweig,
Mendelssohnstr. 1,
D 38106 Braunschweig
In vitro Untersuchungen über
das Penetrations und Permeationsverhalten von Arzneistoffen aus dermalen Zubereitungen
können sowohl mit tierischen und menschlichen Hautspenden als auch mit einem
organotypischen Hautäquivalent durchgeführt werden. Geschlecht und Alter
des Spenders sowie die Körperregion, aus der die Spende entnommen wurde,
haben zumeist deutlichen Einfluß auf die Barriereeigenschaft der Haut und
somit auf die Aussagekraft der gewonnenen Ergebnisse. Durch standardisierte Kultivierung
der Hautäquivalente mit homogenem Zellmaterial können diese Schwierigkeiten
bei in vitro Tests vermieden werden.
Nach [1] konnte ein 3 dimensionales organotypisches Hautäquivalent entwickelt bzw. nach [2] modifiziert werden. Es besteht aus humanen dermalen in einem Kollagengel eingebetteten Fibroblasten und HaCaT Zellen als Epidermisäquivalent.
Die Hautäquivalente wurden in Permeationsuntersuchungen mit verschiedenen Arzneistoffen im Vergleich zum humanen Stratum corneum eingesetzt. Mit Hilfe der modifizierten Franz Zelle wurde zeitabhängig die Menge an Arzneistoff mittels HPLC Analytik bestimmt, die aus der Zubereitung die Haut permeiert. Untersuchungen mit Ibuprofensäure aus Ibutop Creme (IC) als Donator und Phosphatpuffer pH 7,4 als Akzeptormedium zeigten einen Unterschied im Permationskoefizienten KP zwischen Hautäqivalent und humanen Stratum corneum um den Faktor 19 [2]. Für weitere Untersuchungen dienten als Donator jeweils 10%ige Zubereitungen von 8 Aminolävulinsäure (ALA) und ihrem Butylester (ABE) in Excipiah‘ Fettcreme und als Akzeptor ein Phosphatpuffer pH 5.0. Der Permeationskoeffizient lag für das Hautäquivalent bei ALA sogar um Faktor 64 bzw. bei ABE um Faktor 142 höher als für das humane Stratum corneum [3].
| KP (Stratum corneum) [ cm/s ] | KP (ASC) [ cm/s ] | |
| ALA aus [3] | 3,01 10 ‚° +/ 7,44 10 “ | 1,91 10 g +/ 1,71 10 9 |
| ABE aus [3] | 3,00 10 9 +/ 8,04 10 10 | 4,26 10 ‚ +/ 4,19 10 8 |
| Ibuprofen aus IC | 3,70 10 aus [4] | 7,04 10 ‚ +/ 0.20 10 ‚ aus [2] |
Die Untersuchungen mit Stratum corneum zeigen, dass bei den oben genannten Arzneistoffen die Permeationskoeffizienten abhängig von ihren physikochemischen Eigenschaften in der Reihenfolge ALA<ABE<Ibuprofen zunehmen. Für die Steigerung der Permeationskoeffizienten des Hautäquivalents gegenüber Stratum corneum ergeben sich aber deutlich unterschiedliche Faktoren. Das Hautäquivalent zeigt für alle untersuchten Arzneistoffe eine deutlich höhere Permeabilität, die für jeden Arzneistoff spezifisch zu sein scheint.
Lit.:
[1] Specht. C., Müller Goymann, C.C., Proc. 2°d
World Meeting APGI/APV, Paris 1998, pp 1039 40
[2] Wassermann. K., Müller
Goymann, C.C., Abstract, Arch. Pharm. Pharm. Med. Chem. 333 (Suppl. 1) (2000)
34
[3] Winkler. A., Müller Goymann, C.C., Comparative permeation studies
for 8 aminolevulinic acid and its n butyl ester through stratum corneum and artificial
skin constructs, European Journal of Pharmaceutics and Biopharmaceutics (2002)
in press
[4] Specht et al.. Comparative investigaions to evaluate the use
of organotypic cultures of transformed and native dermal and epidermal cells for
permeation studies, European Journal of Pharmaceutics and Biopharmaceutics, 46
(1998) 273 278
Eden, G., Tronnier,
H., Heinrich, U.
Testing of sunscreens using improved
reflectance spectroscopy
U.
Institute for Experimental Dermatology, University Witten/Herdecke, 58455 Witten,
Germany
Background and Objective:
When comparing
in vivo tests of sun protection products an the human skin and in vitro transmission
analyses, a fundamental problem consists of the difference between the skin and
(smooth or roughened) quartz slides and the question of the skin’s possible influence
an the sun protection products. The reflectance spectroscopy has the advantage
of being a noninvasive method and thus, of being ethically unquestioned. Measurements
can be easily performed and within short time intervals.
Material
and Methods:
Using a reflectance spectrometer (Multiscan OS20, MBR
Messtechnik) the spectral reflectance of human skin was measured before and alter
application of sunscreen products. Seven sunscreens and one sunscreen base without
UV filters were applied an the volar side of the forearm in an even surface density
of 2 mg/cmZ, since the published SPF is related to this value. The spectral working
range was between 260 470 nm. By means of a novel algorithm developed by us, the
spectral reflectance of the skin treated with the sunscreen base was subtracted,
and the special irradiance of terrestrial sunlight (E) as well as the erythemal
effectiveness (CIE) of skin were multiplied to the absorbance differences. Measurements
were made in vivo and in vitro before and immediately after application, and alter
elapse of additional 30 minutes, 2, 4 and 6 hours after application. Reflectance
spectra were used to determine the SPF for every tested sunscreen product reliant
an the whole UV range.
Results:
1. There is a close correlation
between biological and reflectionphotometric determination of the SPF.
2.
An essential biological influence of the sun protection substances during an expected
period of exposure does not occur.
3. The method offers a chance for the
testing of water resistance of sun protection products.
Conclusion:
The reflectionphotometric evaluation of sun protection products can
complement in vitro transmission measurements and shows values comparable to biological
SPF determination.
The reflectance spectroscopy has the advantage of being
a non invasive method.
Measurements can be easily performed and within short
time intervals.
It provides a very good reproducibility, while taking the
physiologically important parameters into account.
References:
1. Diffey, B.L., Robson, J.: A new substrate to measure sunscreen protection
factors throughout the ultraviolet spectrum; J Soc Cosmet Chem, 1989; 40:127 133
2. Tronnier, H.: Practice of the in vitro estimation of suncare products; Kosm
Med 18; Doppelheft 5/6, Dez 97/Jan 98: 344 350
3. Kockott, D.: In vitro Bewertung
von Sonnenschutzmitteln; Kosm Med, 1998; 19/5:290 293
4. McKinlay, A.F., Diffey,
B.L.: A reference action spectrum for ultraviolet induced erythema in human skin;
CIE Journal, 1987; 6:17 22
5. Stokes, R.P., Diffey, B.L.: The water resistance
of sunscreen and day care products; Br J Dermatol, 1999; 140:259 263
6. Sayre,
R.M., Agin, P.P., LeVee, G., Marlowe, E.: A comparison of in vivo and in vitro
testing of Sunscreening formulas; Photochem Photobiol, 1979; Vol 29:559 566
Koppmann S.*, Daniels
R.#, Schulz J.*, Gers Barlag H.*
Untersuchung zur Stabilität von Pickering Emulsion, Stabilisiert
durch Oberflächenmodifiziertes Titanoxid
*
Beiersdorf AG, Hamburg
# Technische Universität Carolo Wilhelmina zu
Braunschweig, Institut für Pharmazeutische Technologie, Mendelssohnstrasse
1, D 38106 Braunschweig
Stichworte: Pickeringemulsion, Titandioxid, Oberflächenbehandlung, Lichtschutz,
Elektronenmikroskopie
Titandioxid wird heutzutage aufgrund seines breiten UV Absorptionsspektrums und seiner optischen Akzeptanz sehr häufig in kosmetischen Sonnenschutzemulsionen eingesetzt. Zusätzlich zu seiner UV absorptiven Wirksamkeit ist Titandioxid in der Lage, sogenannte „Drei Phasen Emulsionen“ zu stabilisieren. Dadurch können emulgatorfreie, dermatologische Sonnenschutzemulsionen hergestellt werden, die besonders für die Anwendung bei allergiegefährdeter Haut geeignet sind. In neuen Publikationen beschreibt Binks et al. DreiPhasen Emulsionen, die durch verschiedene Feststoffe wie z.B. Silica und Latex Partikel stabilisiert werden [ 1 ] [2].
Die vorliegende Arbeit beschäftigt sich mit der Stabilität und Lichtschutzleistung emulgatorfreier Drei Phasen Emulsionen, bestehend aus mit Alumiumoxid und Simethicone beschichtetem Titandioxid, mittelkettigen Triglyceriden sowie Wasser als Hauptkomponenten. Die mittlere Partikelgröße des Titandioxid Pigments liegt bei 10 15nm. Verschiedene analytische Methoden, wie Elektronenmikroskopie und statische Lichtstreuung wurden benutzt um die Emulsionssysteme zu charakterisieren.
Die Ergebnisse zeigen, dass stabile Pickering Emulsionen [3][4] durch Einsatz nanometergroßer Titandioxide erhalten werden können. Besonders stabile Systeme lassen sich durch den Einsatz oberflächenmodifizierter Titandioxide formulieren, wobei sich v.a. eine Beschichtung mit Aluminiumoxid und Simethicone als besonders vorteilhaft erwiesen hat. Es lassen sich unabhängig von der Art der Herstellung in untersuchten Systemen v.a. stabile O/W Emulsionen herstellen.
[ 1 ] BINKS, B.P.; LUMSDON,
S.O.: Langmuir 16 (2000), p. 8622 8631
[2] BINKS, B.P.; LUMSDON, S.O.: Langmuir
17 (2001), p. 4540 4547
[3] PICKERING, Spencer U.: J. Chem. Soc. Trans. 91
(1907), p. 2001 2021
[4] MUKERJEE, L.N.; SRIVASTAVA, S. N.: Kolloid Z. 150
(1957), p. 144 148
Birgit Huber
Inhalte
der Kosmetik Gesetzgebung unter Berücksichtigung der neuesten Änderungen
Industrieverband Körperpflege und Waschmittel e.V. (IKW), Frankfurt am Main
Der Aufbau der Kosmetik Richtlinie
1976 war ein einschneidendes Jahr für die Kosmetikindustrie, da dort die europaweite Gesetzgebung für kosmetische Mittel verankert wurde. Hierbei handelt es sich um eine Richtlinie der EG, die von den Mitgliedstaaten in nationales Recht umgesetzt werden muss. In der deutschen Umsetzung der Richtlinie von 1976 im Lebensmittel und Bedarfsgegenständegesetz bzw. der Kosmetik Verordnung wurden drei wichtige Eckpunkte verankert:
Definition
kosmetischer Mittel, die heute sechs verschiedene Verwendungszwecke zulässt,
nämlich reinigen, parfümieren, Aussehen verändern, Körpergeruch
beeinflussen, schützen und in gutem Zustand halten. Dort ist auch festgelegt,
dass kosmetische Mittel dazu bestimmt sind, äußerlich angewandt zu
werden oder mit den Zähnen und den Schleimhäuten der Mundhöhle
in Berührung zu kommen. Einer Liste beispielhafter Produkte ist auch zu entnehmen,
dass neben Shampoo, Duschbädern, Dauerwellen, Hautpflegeprodukten auch z.B.
Antifaltencremes, Sonnenschutzmittel sowie Zahnpflegeprodukte als kosmetische
Mittel einzustufen sind.
„Kosmetische Mittel dürfen
bei normaler oder vernünftigerweise vorhersehbarer Verwendung die
menschliche Gesundheit nicht schädigen, insbesondere unter Berücksichtigung
der Aufmachung des Produkts, seiner Etikettierung, gegebenenfalls der Hinweise
für seine Verwendung und der Anweisungen für seine Beseitigung sowie
aller sonstigen Angaben oder Informationen.“ Mit dieser Anforderung wird
die Verantwortung für das gesamte Produkt dem Hersteller übertragen,
und dieser Herausforderung müssen sich die Hersteller der Produkte seit dieser
Veröffentlichung tagtäglich stellen.
Der Hersteller muss darüber
hinaus Sorge tragen, dass der Verbraucher durch die Aufmachung seiner Produkte
nicht getäuscht wird. Hieraus ergibt sich, dass einem kosmetischen
Mittel nur solche Wirkversprechen zugeschrieben werden können, die auch belegbar
sind.
Stoffregelungen sieht die EG Kosmetik Richtlinie ebenfalls vor. Es gibt Stoffe, die verboten sind zur Verwendung, solche die eingeschränkt sind, und für bestimmte Produktgruppen sind nur die in so genannten Positivlisten (für Konservierungsstoffe, UV Filter, Farbstoffe) zugelassenen Stoffe erlaubt.
Produktangaben
Das Kosmetik Recht enthält noch eine Vielzahl weiterer Anforderungen, wie z.B. die Erstellung von Produktangaben, Notifizierung des Herstellungsortes, Meldung an die Giftinformationszentralen, die Kennzeichnung der Inhaltsstoffe, um nur einige Beispiele herauszugreifen, die dazu beitragen, dass kosmetische Mittel weiter auf hohem Niveau hergestellt werden.
Vor allem die Erstellung der Produktangaben, die für jedes kosmetische Mittel an einem Ort in der EU zur Einsicht für die Überwachungsbehörden bereitgehalten werden müssen, ist mit großem Aufwand verbunden. Folgende Informationen werden unter den Produktangaben zusammengefasst:
die qualitative und quantitative Zusammensetzung des Erzeugnisses
physikalisch chemische und mikrobiologische Spezifikationen der Ausgangsstoffe und des Fertigerzeugnisses sowie die Kriterien für Reinheit und mikrobiologische Kontrollen des kosmetischen Mittels
Herstellungsweise gemäß der „Guten Herstellungspraxis“ die Bewertung der Sicherheit des Fertigerzeugnisses für die menschliche Gesundheit
Name und Anschrift der Person, die für die Sicherheitsbewertung verantwortlich ist r bekannte Daten über unerwünschte Nebenwirkungen sowie
der Nachweis der für das kosmetische Mittel angepriesenen Wirkung
Kennzeichnungsvorschriften
Im Artikel 6 der EG Kosmetikrichtlinie bzw. der Kosmetikverordnung ist eine Vielzahl von Kennzeichnungsvorschriften für kosmetische Mittel festgelegt. Die folgenden Angaben müssen deutlich sichtbar, leicht lesbar und unverwischbar auf der Verpackung des Behälters des kosmetischen Mittels angegeben sein:
Herstellerangabe
Nenninhalt
Mindesthaltbarkeitsdatum sowie
Warnhinweise bzw. Anwendungsgebiet
und Bedingungen gemäß den Anhängen die Chargenkodierung und der
Verwendungszweck.
Die Angabe des Mindesthaltbarkeitsdatums kann entfallen, wenn das kosmetische Mittel länger als 30 Monate haltbar ist. Die Angabe des Verwendungszweckes ist eine neue Anforderung, die ein weiterer Schritt zur Information des Verbrauchers darstellt.
Anstehende neue Regelungen
Nach umfangreichen Beratungen durch die Mitgliedsstaaten hat kurz vor Jahresende die belgische Ratspräsidentschaft einen Kompromissvorschlag zur siebten Änderungsrichtlinie verabschiedet.
Dieser sieht ein sofortiges Testverbot am Tier vor, sobald von der Europäischen Union entsprechende Alternativen anerkannt sind, und ein Vermarktungsverbot für am Tier getestete Inhaltsstoffe bzw. deren Produkte, sobald Alternativen von der OECD (Organisation for Economic Co operation and Development) weltweit bestätigt sind.
Das vom Europäischen Parlament ursprünglich vorgesehene Vermarktungsverbot von Produkten bzw. Inhaltsstoffen wurde von den Mitgliedsstaaten der Europäischen Union abgelehnt.
Der Text, der jetzt
in Form eines Gemeinsamen Standpunktes dem Europäischen Parlament zur Beratung
vorgelegt wird, enthält weiterhin einen Passus, dass künftig bestimmte
Bestandteile von Riechstoffen im Rahmen der INCI Deklaration gekennzeichnet werden
sollen. Darüber hinaus soll künftig vorgeschrieben werden, dass ein
Mindesthaltbarkeitsdatum auf allen Kosmetika mit Monat und Jahr angegeben werden
soll.
| Fotos: Gesellschaft für Dermopharmazie |


Ludger Neumann
Nachweis
der Wirksamkeit von kosmetischen Mitteln
L’Oréal GmbH, Düsseldorf
Eine Arbeitsgruppe des europäischen Kosmetikverbandes COLIPA hat im Jahre 2001 Leitlinien für die Bewertung der Wirksamkeit von kosmetischen Mitteln erarbeitet. Die Leitlinien stützen sich auf Bestimmungen im europäischen Kosmetikrecht sowie auf nationale Bestimmungen zum Schutz der Verbraucher und bilden eine Brücke zur Bewertung von Werbeaussagen. Die Leitlinien gelten in der gesamten EU im Sinne des freien Warenverkehrs für die Bewertung von Werbeaussagen durch Kosmetikhersteller, die staatliche Kosmetiküberwachung und die Rechtssprechung.
Werbeaussagen sind öffentliche Informationen zu Inhalt, Art, Eigenschaft oder Wirkung von kosmetischen Mitteln, die in Form von Sprache, Text, Bildern oder Beschreibungen auf den Produkten oder in der Werbung erscheinen. Eine Werbeaussage darf nicht irreführend sein, wobei die Verbrauchererwartungen gemäß dem europäischen Verbraucherleitbild und dem Gesamteindruck des Produkts beurteilt werden müssen. Wirksamkeitsnachweise erfolgen am Produkt oder am Rohstoff. Werbeaussagen müssen durch einwandfreie, relevante und eindeutige Wirksamkeitsnachweise belegt werden.
Drei gleichberechtigte Arten von Wirksamkeitsnachweisen können eingesetzt werden, um eine Werbeaussage zu belegen.
1. Allgemein anerkannte Daten: Dazu gehören selbstverständliche Produktwirkungen aufgrund der Funktion wie die parfümierende Wirkung eines Eau de Toilette, Literaturbelege und Lehrmeinungen wie die Wirkung von Vitamin E gegen freie Radikale.
2. Experimentelle Studien: Lange bekannt und gut dokumentiert sind instrumentelle Methoden ohne und mit Probanden. Ohne Probanden lassen sich die Nasskämmbarkeit an Haarsträhnen oder Penetrationsuntersuchungen an künstlicher Haut durchführen. Mit Probanden werden Corneometermessungen zur Bestimmung der Hautfeuchtigkeit oder Messungen mit FOITS oder PRIMOS zur Hautglättung durchgeführt. Zu experimentellen Studien als Wirksamkeitstests gehören aber auch Anwendungstests mit Beurteilung durch einen Experten, der z.B. die Bewertung von Haarpflegeprodukten im Halbseitentest durchführt, oder durch ein trainiertes Expertenpanel, das z.B. das Einziehen von Emulsionen auf der Haut beurteilt.
3. Bewertung durch den Verbraucher: Zu dieser Art von Wirksamkeitstests gehören Bewertungen durch ein nicht trainiertes kleines Verbraucherpanel, das z.B. die Frisierbarkeit von Haaren bewertet, sowie Verbrauchertests mit großen Gruppen, die z.B. die Anwendungseigenschaften einer Creme bewerten.
Die Studien für alle Wirksamkeitsnachweise müssen relevant, zuverlässig und reproduzierbar sein. Ethische Normen bei Studien an Probanden müssen respektiert werden. Die Verantwortung dafür trägt jeder Hersteller selbst. Die Verwendung einer Kontrolle beim Test (vorher/nachher, behandelt/unbehandelt, gegen Benchmark, gegen internen Standard) kann zur Unterstützung der Werbeaussage dienen. Der Placebobegriff ist dagegen nicht relevant, weil bei einem kosmetischen Mittel alle Inhaltsstoffe einen Beitrag zur Gesamtwirkung haben. Zu den Prüfberichten und zur statistischen Auswertung geben die Leitlinien detaillierte Informationen.
Die
Beurteilung, ob ein Wirksamkeitsnachweis angemessen ist, bleibt Verantwortung
des Herstellers. Dabei bilden die drei Arten von Werbeaussagen gleichwertig anerkannte
Säulen zur Stützung für Wirksamkeitsnachweise. Je nach Werbeaussage
können eine, zwei oder alle drei der Säulen den Wirksamkeitsnachweis
stützen.
| L. Neumann (rechts) Fotos: Gesellschaft für Dermopharmazie |


Walter Sterzel
Strategien
zur Absicherung kosmetischer Mittel
Henkel KGaA, Düsseldorf
Bei der Vielzahl der uns umgebenden Stoffe ist es eine Grundverpflichtung, davon möglicherweise ausgehende Gefahren für den Menschen zu identifizieren und damit einhergehende Risiken zu beschreiben. Dieser Anspruch wird auch durch die einschlägige Kosmetikgesetzgebung in Form der 6. Änderung der EG Kosmetik Richtlinie aufgegriffen. Diese fordert, dass eine Bewertung der Sicherheit des kosmetischen Erzeugnisses für die menschliche Gesundheit unter Berücksichtigung des allgemeinen toxikologischen Profils der Bestandteile, ihres chemischen Aufbaus und des Grades der Exposition vorgenommen werden soll. Basierend darauf wurde eine Strategie zur Sicherheitsbewertung kosmetischer Mittel entwickelt, die sich in vier Teilaspekte auffächert:
o Identifikation schädlicher Eigenschaften
o Dosis Wirkungsanalyse
o Ermittlung der Exposition
o Sicherheitsbewertung
Für die Identifikation schädlicher Eigenschaften der verwendeten Inhaltsstoffe existieren eindeutig festgelegte Methoden, die in Form der OECD Methodensammlung eine internationale Standardisierung und Akzeptanz gefunden haben. Der Umfang der erforderlichen Daten wird wesentlich durch die vorgesehene Anwendung bestimmt. In den überwiegenden Fällen genügen Basisdaten zur akuten Toxizität, zur Haut und Schleimhautverträglichkeit, zur Sensibilisierung, In vitro Daten zur Mutagenität sowie eine Abschätzung der dermalen Penetration. Weitergehende Untersuchungen zur Langzeittoxizität, Reproduktionstoxizität und zusätzliche Mutagenitätsuntersuchungen sind dann erforderlich, wenn Inhaltsstoffe dermal, inhalativ oder oral aufgenommen werden können.
Wesentlich flexibler und stärker an die Anwendungssituation angelehnt ist die Ermittlung der Exposition. Sie folgt und beschreibt die reale Anwendungssituation und den daraus erwachsenden Kontakt mit dem zu beurteilenden Produkt. Eine wertvolle Richtschnur stellen hier die Guidelines des SCC/NFP dar, die Anhaltspunkte über im Mittel applizierte Gesamtmenge, Frequenz, Art der Anwendung sowie die Dauer des Kontaktes vermitteln.
Mit Hilfe der beschriebenen Toxizitäts und Expositionsdaten kann nunmehr eine Sicherheitsbewertung für den vorgesehenen Einsatzzweck erstellt werden. Hierbei werden die Schwellenkonzentrationen für die Auslösung von Schadwirkungen den Expositionsmengen gegenübergestellt. Für sichere Kosmetikerzeugnisse ist die derart ermittelte tolerable Dosis stets größer als die ermittelte Exposition.
Die Verantwortung des Herstellers für die Sicherheit seiner Produkte endet nicht mit deren Vermarktung. Eine umfassende Sicherheitsstrategie muss vielmehr ein sorgfältiges Monitoring des Geschehens am Markt einschließen.
Unerwünschte Nebenwirkungen kosmetischer Mittel lassen sich häufig auf Fehlanwendungen zurückführen und sind gemessen an der millionenfachen Anwendung der Produkte selten. Dies belegen auch die Statistiken der Hersteller, die gemäß Kosmetikverordnung zur Dokumentation von Unverträglichkeitsreaktionen verpflichtet sind.
Zusammenfassend ist festzustellen, dass die heute verwendete Absicherungsstrategie
einen wesentlichen Beitrag zur hohen Akzeptanz und Sicherheit kosmetischer Mittel
leistet.
| W. Sterzel (links) Fotos: Gesellschaft für Dermopharmazie |


Dr. Karsten Albert
Qualität
der Ausgangsstoffe
Zentrales Prüflaboratorium des Deutschen Arzneimittel-Codex (DAC), Eschborn
Nach den Grundsätzen der Apothekenbetriebsordnung dürfen
zur Herstellung von Arzneimitteln nur Ausgangsstoffe verwendet werden, die hinsichtlich
ihrer Qualität strenge Normen erfüllen. Die Forderungen an Identität,
Reinheit und Gehalt sind vor allem im Europäischen Arzneibuch (Ph.Eur.),
im Deutschen Arzneibuch (DAB) und im Deutschen Arzneimittel-Codex (DAC) enthalten.
In der Apothekenpraxis wird die Qualität der Ausgangsstoffe mit Hilfe
einer Vorprüfung beim Hersteller gesichert, deren Ergebnisse in einem Zertifikat
nachzuweisen sind. Darüber hinaus muss in der Apotheke vor der Verarbeitung
jedes Stoffes mindestens der Identitätsnachweis durchgeführt werden.
Im Vortrag wird die Qualität der Grundstoffe aus pharmazeutischer Sicht behandelt,
und es werden Möglichkeiten aufgezeigt, wie sie unter Praxisbedingungen sichergestellt
werden kann. Außerdem werden aktuelle Probleme beim Bezug von Ausgangsstoffen
angesprochen.
| Foto: Gesellschaft für Dermopharmazie |
