Prof. Dr. Victoria
Kolb-Bachofen
unter Mitarbeit von C.V. Suschek, O. Schnorr, A.
Kuhn, D. Bruch-Gerharz, und T. Ruzicka
Stickoxid
als neues therapeutisches Prinzip
Institut für Immunbiologie, Heinrich-Heine-Universität, Düsseldorf
Relativ hohe Konzentrationen von Stickstoff-Monoxid (NO) können
auch in der Haut lokal gebildet werden als Folge von entzündlichen Situationen
(1, 2), bei denen durch Zytokine die de novo Expression der induzierbaren NO-Synthese
(iNOS) ausgelöst wird. Diese hohe NO-Synthese benötigt die Aminosäure
L-Arginin und wurde als Verstärker der Gewebezerstörung angesehen,
aber neuere Untersuchungen zeigen, dass diese Sicht zu einfach war. Tatsächlich
gehen von diesem kleinen radikalischen Molekül wichtige Regulatorfunktionen
aus. Neueste Publikationen belegen, dass dem iNOS-synthetisierten NO eine wichtige
Funktion in der Hautphysiologie zukommt. So hatten wir bereits früher zeigen
können, dass die iNOS-Expression eine normale Antwort auf UV-Bestrahlung
der menschlichen Haut ist (3), und das Fehlen dieser Antwort zur richtigen Zeit
einen Krankheitsmarker bei Patienten mit cutanem Lupus darstellt. Auch fanden
wir, dass Kultur von primären humanen Keratinozyten in Gegenwart eines
NO-donors das Wachstum reguliert. Bei niedrigen Konzentrationen wird das Wachstum
beschleunigt und bei höheren Konzentrationsen die Differenzierung induziert
(4). Wir können auch zeigen, dass die endogene iNOS-Aktivität in diesen
Zellen ebenfalls eine Differenzierung auslöst, eine Antwort, die aber essentiell
von der vorhandenen Arginase-1-Aktivität abhängt. Untersuchungen an
Hautbiopsien von Psoriasis-Patienten bestätigen, dass in vivo in den Läsionen
die iNOS nicht ausreichend aktiv ist, in Korrelation zur gefundenen Arginase
Überexpression (5). Des Weiteren konnten wir auch demonstrieren, dass eine
iNOS-vermittelte NO-Synthese, aber auch exogen zugeführtes NO, zu einem
vollständigen Schutz vor apoptotischem Zelltod durch UVA-Bestrahlung führt.
Dieser potente Schutz läuft über zwei unterschiedliche Wege. NO verhindert
die UVA-induzierte Lipid-Peroxidation und trägt so zur Aufrechterhaltung
der Membranintegrität bei (6). Zusätzlich finden wir auch eine enge
Korrelation mit einer NO-vermittelten Verstärkung des anti-apoptotisch
wirkenden Proteins Bcl-2 (7). Dieser NO-vermittelte Schutz vor UV-induziertem
Zelltod ist abhängig von der Verfügbarkeit der Aminosäure L-Arginin,
die das Enzymsubstrat für die NO-Synthese darstellt (8). Eine kleine Versuchserie
an 6 gesunden Probanden hat gezeigt, dass eine topisch applizierte NO enthaltende
Creme während der UV-Bestrahlung das Erythem reduziert und gleichzeitig
die Hautpigmentierung etwas verstärkt.
(1) Bruch-Gerharz D., Fehsel K., Suschek C., Michel G., Ruzicka T. und Kolb-Bachofen
V.: J. Exp. Med. 184, 2007-2012,1996
(2) Bruch-Gerharz D., Ruzicka T. und Kolb-Bachofen V.: J Invest. Dermatol. 110,
1-7, 1998
(3) Kuhn A., Fehsel K., Lehmann P., Krutmann J., Ruzicka T. und Kolb-Bachofen
V.: J. Invest. Dermatol. 111, 101-105, 1998
(4) Krischel, V., Bruch-Gerharz, D., Suschek, C., Kröncke, K.-D., Ruzicka,
T. und Kolb-Bachofen, V.: J. Invest. Dermatol. 111, 286-291, 1998
(5) Schnorr O., Bruch-Gerharz D., Suschek C., Beck K.-F., Pfeilschifter J.,
Ruzicka T. und Kolb-Bachofen V.: Am. J. Pathol. 162, 203-211, 2003
(6) Suschek, C. V., Bribiva, K., Bruch-Gerharz, D., Sies, H., Kröncke,
K.-D. und Kolb-Bachofen, V.: Cell Death Diff. 8, 515-527, 2001
(7) Suscheck, C.V., Schuy, V., Bruch-Gerharz, D., Berenji, D., Krutmann, J.,
Kröncke, K.-D. und Kolb-Bachofen, V. : J. Biol. Chem. 274, 6130-6137, 1999
(8) Suschek C., Schnorr O., Hemmrich K., Aust O., Klotz L.-O., Sies H. und Kolb-Bachofen
V. : Circulation, 2003 in press
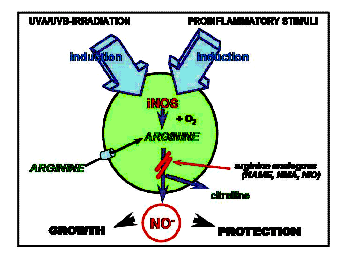
Graphik zur iNOS-Induktion und –Enzymaktivität

 Foto: GD Gesellschaft für Dermopharmazie |